பேரியம் புளோரைடு
| |
| இனங்காட்டிகள் | |
|---|---|
| 7787-32-8 | |
| ChemSpider | 56421 |
| யேமல் -3D படிமங்கள் | Image |
| பப்கெம் | 62670 |
| வே.ந.வி.ப எண் | CQ9100000 |
SMILES
| |
| பண்புகள் | |
| BaF2 | |
| வாய்ப்பாட்டு எடை | 175.34 கி/மோல் |
| தோற்றம் | வெண்ணிற கனசதுரப் படிகங்கள் |
| அடர்த்தி | 4.893 கி/செமீ3 |
| உருகுநிலை | 1,368 °C (2,494 °F; 1,641 K) |
| கொதிநிலை | 2,260 °C (4,100 °F; 2,530 K) |
| 0.16 கி/100 மிலி (20 °செ) | |
| கரைதிறன் | மெத்தனால், எத்தனால் ஆகியவற்றில் கரையும் |
| -51.0·10−6 செமீ3/மோல் | |
| ஒளிவிலகல் சுட்டெண் (nD) | 1.455 |
| கட்டமைப்பு | |
| படிக அமைப்பு | புளோரைட்டு (கனசதுரம்), cF12 |
| புறவெளித் தொகுதி | Fm3m, No. 225 |
| தீங்குகள் | |
| ஈயூ வகைப்பாடு | Harmful (Xn) |
| R-சொற்றொடர்கள் | R20/22 |
| S-சொற்றொடர்கள் | (S2), S28 |
| தீப்பற்றும் வெப்பநிலை | எளிதில் தீப்பற்றாதது |
| Lethal dose or concentration (LD, LC): | |
LD50 (Median dose)
|
250 மிகி/கிகி, வாய்வழி (எலி) |
| தொடர்புடைய சேர்மங்கள் | |
| ஏனைய எதிர் மின்னயனிகள் | பேரியம் குளோரைடு பேரியம் புரோமைடு பேரியம் அயோடைடு |
| ஏனைய நேர் மின்அயனிகள் | பெரிலியம் புளோரைடு மெக்னீசியம் புளோரைடு கால்சியம் புளோரைடு இசுட்ரோன்சியம் புளோரைடு |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
| | |
| Infobox references | |
பேரியம் புளோரைடு (Barium fluoride) (BaF2) பேரியம் மற்றும் புளோரின் ஆகிய தனிமங்கள் இணைந்த வேதிச் சேர்மம் ஆகும். இது ஒளி ஊடுருவக்கூடிய திண்மம் ஆகும். இது இயற்கையில் பிரான்க்டிக்சோனைட்டு கனிமூலமாக இயற்கையில் காணப்படுகிறது.[1]
அமைப்பு[தொகு]
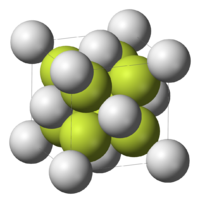
இத்திண்மம் புளோரைட்டின் அமைப்பையும் உயர் அழுத்தத்தில் காரீய குளோரைடு அமைப்பையும் கொண்டுள்ளது.[2] ஆவி நிலையில் BaF2 மூலக்கூறானது தோராயமாக F-Ba-F 108° கோண அளவைக் கொண்ட நேர்கோடல்லாத அமைப்பைக் கொண்டுள்ளது.[3] இது வலுவளவு ஒட்டு இலத்திரன் சோடிகளின் தள்ளுகைக் கொள்கையின்படி நேர்கோட்டு வடிவத்தைக் கொண்டிருக்க வேண்டும் என்பதற்கு மாறாக விதிவிலக்கான அமைப்பைக் கொண்டுள்ளது. தொடக்கத்திலிருந்து வந்த கணிப்புக்கள், இணைதிறன் கூடுகளுக்கு உட்புறமாக உள்ள d ஆர்பிட்டால்களிலிருந்து வந்த பங்களிப்புகளைச் சார்ந்ததாக முன்மொழியப்பட்டுள்ளது.[4] மற்றொரு கோட்பாடானது பேரியம் அணுவின் இலத்திரன் கருவின் முனைவுறு தன்மையானது Ba-F பிணைப்புகளுடன் இடைவினைபுரிந்து மின்சுமையானது தோராயமாக நான்முகி வடிவ பகிர்வை உருவாக்கலாம் என்கிறது.[5]
பயன்கள்[தொகு]
அலுமினிய சுத்திகரிப்பு செயல்முறையில் ஒரு சேர்க்கைப் பொருளாகப் பயன்படுகிறது. பூச்சுக்களிலும், பற்றவைப்புக்கான உலோகப்பொடிகள் மற்றும் உலோகக்கம்பிகளிலும் பகுதிப்பொருளாகப் பயன்படுகிறது. ஒரு இளக்கியாகவும், ஒளிபுகாத்தன்மையை உருவாக்கும் காரணியாகவும் பயன்படுகிறது.[6]
மேற்கோள்கள்[தொகு]
- ↑ Radtke A.S., Brown G.E. (1974). "Frankdicksonite, BaF2, a New Mineral from Nevada". American Mineralogist 59: 885–888. http://www.minsocam.org/ammin/AM59/AM59_885.pdf.
- ↑ A.F Wells (1984). Structural inorganic chemistry -5th Edition. Oxford: Clarendon Press. பன்னாட்டுத் தரப்புத்தக எண்:0-19-855370-6. https://archive.org/details/structuralinorga0000well_m8i1.
- ↑ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ). Butterworth-Heinemann. பன்னாட்டுத் தரப்புத்தக எண்:0080379419.
- ↑ Seijo, Luis; Barandiarán, Zoila; Huzinaga, Sigeru (1991). "Ab initio model potential study of the equilibrium geometry of alkaline earth dihalides: MX2 (M=Mg, Ca, Sr, Ba; X=F, Cl, Br, I)". The Journal of Chemical Physics 94 (5): 3762. doi:10.1063/1.459748.
- ↑ Bytheway, Ian; Gillespie, Ronald J.; Tang, Ting-Hua; Bader, Richard F. W. (1995). "Core Distortions and Geometries of the Difluorides and Dihydrides of Ca, Sr, and Ba". Inorganic Chemistry 34 (9): 2407. doi:10.1021/ic00113a023.
- ↑ https://www.solvay.com/en/markets-and-products/featured-products/Barium-fluoride.html
