கோபால்ட்(III) புளோரைடு
| |
| பெயர்கள் | |
|---|---|
| வேறு பெயர்கள்
கோபால்ட் முப்புளோரைடு
கோபால்ட்டிக் புளோரைடு கோபால்ட் புளோரைடு கோபால்ட்டிக் முப்புளோரைடு | |
| இனங்காட்டிகள் | |
| 10026-18-3 | |
| ChemSpider | 59593 |
| EC number | 233-062-4 |
| யேமல் -3D படிமங்கள் | Image |
| பப்கெம் | 66208 |
SMILES
| |
| பண்புகள் | |
| CoF3 | |
| வாய்ப்பாட்டு எடை | 115.928 கி/மோல் |
| தோற்றம் | பழுப்புநிறத் தூள் |
| அடர்த்தி | 3.88 கி/செ.மீ3 |
| உருகுநிலை | 92 °C (198 °F; 365 K) |
| வினைபுரியும் | |
| கட்டமைப்பு | |
| படிக அமைப்பு | அறுகோணம் |
| தீங்குகள் | |
| தொடர்புடைய சேர்மங்கள் | |
| ஏனைய எதிர் மின்னயனிகள் | கோபால்ட்(III) ஆக்சைடு, கோபால்ட்(III) குளோரைடு |
| ஏனைய நேர் மின்அயனிகள் | இரும்பு(III) புளோரைடு, ரோடியம்(III) புளோரைடு |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
| | |
| Infobox references | |
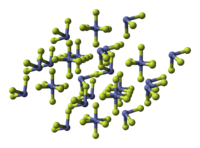
கோபால்ட்(III) புளோரைடு (Cobalt(III) fluoride) என்பது CoF3 என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட ஒரு கனிம வேதியியல் சேர்மமாகும். அதிக வினைத்திறன் மிக்க இச்சேர்மம் பழுப்பு நிறத்தில் நீருறிஞ்சும் திறனுடன் காணப்படுகிறது. கரிம புளோரின் சேர்மங்களைத் தொகுப்பு முறையில் தயாரிக்க கோபால்ட்(III) புளோரைடு பயன்படுகிறது[1] . மேலும் வலிமைமிக்க புளோரினேற்றும் முகவராக இருக்கும் இச்சேர்மம் CoF2 வை உடன் விளைபொருளாக வெளிவிடுகிறது.
தயாரிப்பு[தொகு]
ஆய்வகத்தில் கோபால்ட்(II) குளோரைடுடன் (CoCl2) 250 பாகை வெப்பநிலையில் புளோரின் வாயுவைச் சேர்த்து வினைபுரியச் செய்தால் கோபால்ட்(III) புளோரைடு உருவாகிறது:[2]
- CoCl2 + 3/2 F2 → CoF3 + Cl2.
இவ்வேதி மாற்றம் ஒரு ஆக்சிசனேற்றவொடுக்க வினையாகும்.: Co2+ மற்றும் Cl− அயனிகள் முறையே Co3+ மற்றும் Cl2 வாக ஆக்சிசனேற்றம் அடைகின்றன. அதேவேளையில் F2 ஆனது F− ஆக ஒடுக்கமடைகிறது. கோபால்ட்(II) ஆக்சைடு (CoO) மற்றும் கோபால்ட்(II) புளோரைடு (CoF2) போன்றனவற்றையும் புளோரினைப் பயன்படுத்தி கோபால்ட் (III) புளோரைடாக மாற்ற முடியும்.
வினைகள்[தொகு]
தண்ணீருடன் வினை புரிய நேரிட்டால் CoF3 சிதைவடைந்து ஆக்சிசனைக் கொடுக்கிறது.
- 4 CoF3 + 2 H2O → 4 HF + 4 CoF2 + O2
நீர் உறிஞ்சும் தன்மையுடன் உள்ள CoF3 ஒரு இருநீரேற்றாக உருவாகிறது.(சி.ஏ.எசு.எண் #54496-71-8). புளோரைடு மூலங்களுடன் வினைபுரிந்து [CoF6]3−, என்ற எதிர்மின் அயனியைத் தருகிறது. உயர்சுழற்சி எண்முக கோபால்ட்(III) அணைவுச் சேர்மத்திற்கு இதுவொரு அரிய உதாரணமாகும்.
பயன்கள்[தொகு]
அரை திரவநிலை வேதிப்பொருளாக இச்சேர்மம் பயன்படுகிறது. ஐதரோகார்பன்களை CoF3 பெர்புளோரோகார்பன்களாக மாற்றுகிறது.
- 2CoF3 + R-H → 2CoF2 + R-F + HF
இத்தகைய வினைகள் சில சமயங்களில் மறுசீராக்கல் அல்லது வேறு வினைகளுடன் உடன் நிகழ்கின்றன. தொடர்புடைய வினைப்பொருளான KCoF4 அதிகமாக தேர்ந்தெடுக்கப்படுகிறது.[3]
மேற்கோள்கள்[தொகு]
- ↑ Coe, P. L. "Cobalt(III) Fluoride" in Encyclopedia of Reagents for Organic Synthesis (Ed: L. Paquette) 2004, J. Wiley & Sons, New York. எஆசு:10.1002/047084289X.rc185.
- ↑ Priest, H. F. "Anhydrous Metal Fluorides" Inorganic Syntheses McGraw-Hill: New York, 1950; Vol. 3, pages 171-183. எஆசு:10.1002/9780470132340.ch47
- ↑ Coe, P. L. "Potassium Tetrafluorocobaltate(III)" in Encyclopedia of Reagents for Organic Synthesis (Ed: L. Paquette) 2004, J. Wiley & Sons, New York. எஆசு:10.1002/047084289X.rp251.

