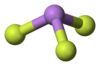
ஆர்சனிக் முப்புளோரைடு
| |||
| பெயர்கள் | |||
|---|---|---|---|
| ஐயூபிஏசி பெயர்
ஆர்சனிக்(III) புளோரைடு
| |||
| வேறு பெயர்கள்
ஆர்சனிக் முப்புளோரைடு, முப்புளோரோ ஆர்சேன்
| |||
| இனங்காட்டிகள் | |||
| 7784-35-2 | |||
| ChemSpider | 22975 | ||
InChI
| |||
| யேமல் -3D படிமங்கள் | Image | ||
| பப்கெம் | 24571 | ||
| வே.ந.வி.ப எண் | CG5775000 | ||
SMILES
| |||
| பண்புகள் | |||
| AsF3 | |||
| வாய்ப்பாட்டு எடை | 131.9168 கி/மோல் | ||
| தோற்றம் | நிறமற்ற திரவம் | ||
| அடர்த்தி | 2.666 கி/செ.மீ3[1] | ||
| உருகுநிலை | -8.5 ˚செ | ||
| கொதிநிலை | 60.4 ˚செ | ||
| சிதைவடையும் | |||
| கரைதிறன் | ஆல்ககால், ஈதர், பென்சீன் மற்றும் அமோனியா கரைசல்களில் கரைகிறது | ||
| தீங்குகள் | |||
| முதன்மையான தீநிகழ்தகவுகள் | நச்சு மற்றும் அரிப்புத் தன்மை | ||
| R-சொற்றொடர்கள் | R23/25, R50/53 | ||
| S-சொற்றொடர்கள் | (S1/2), S20/21, S28, S45, S60, S61 | ||
| வெப்பவேதியியல் | |||
| Std enthalpy of formation ΔfH |
-821.3 கியூ/மோல் | ||
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |||
| | |||
| Infobox references | |||
ஆர்சனிக் முப்புளோரைடு ( Arsenic trifluoride ) என்பது AsF3 என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட ஒரு வேதிச் சேர்மம்ஆகும். நிறமற்ற நீர்மமாக இருக்கும் இச்சேர்மம் தண்ணீருடன் உடனடியாக வினைபுரிகிறது[2].
தயாரிப்பு மற்றும் பண்புகள்[தொகு]
ஆர்சனிக் மூவாக்சைடுடன் ஐதரசன் புளோரைடு சேர்த்து வினைப்படுத்துவதன் மூலமாக ஆர்சனிக் முப்புளோரைடு தயாரிக்க முடியும்.
- 6HF + As2O3 → 2AsF3 + 3H2O
வாயு நிலையில் பட்டைக்கூம்பு மூலக்கூறு வடிவில் உள்ள இச்சேர்மம் திண்ம நிலையிலும் காணப்படுகிறது. வாயு நிலையில் உள்ள போது As-F பிணைப்பு நீளம் 170.6 பை.மீ மற்றும் F-As-F பிணைப்புக் கோணம் 96.2° ஆகவும் உள்ளது[3].
அலோக குளோரைடுகளை, புளோரைடுகளாக புளோரினேற்றம் செய்ய ஆர்சனிக் முப்புளோரைடு பயன்படுகிறது. இச்செயலின் அடிப்படையில் நோக்கும் போது இது ஆண்டிமனி முப்புளோரைடை விட வினைத்திறன் குறைந்ததாக உள்ளது[2].
AsF4− என்ற எதிர்மின் அயனிகள் கொண்ட சேர்மங்களையும் வேதி வினைகளின் மூலம் தயாரிக்க முடியும்[4]. உதாரணம் CsAsF4.பொட்டாசியம் புளோரைடு மற்றும் ஆர்சனிக் முப்புளோரைடு சேர்ந்து உருவாகும் பொட்டாசியத்தின் KAs2F7 உப்பில் AsF4− மற்றும் AsF3 அயனிகள் இடைவினையுடன் காணப்படுகின்றன[5].
SbF5 உடன் வினைபுரிகையில் அயனக் கூட்டுப் பொருள் AsF2+ SbF6− உருவாகிறது[6]
மேற்கோள்கள்[தொகு]
- ↑ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 0-07-049439-8
- ↑ 2.0 2.1 Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ). Butterworth-Heinemann. பன்னாட்டுத் தரப்புத்தக எண்:0080379419.
- ↑ Wells A.F. (1984) Structural Inorganic Chemistry 5th edition Oxford Science Publications ISBN 0-19-855370-6
- ↑ New alkali metal and tetramethylammonium tetrafluoroarsenates(III), their vibrational spectra and crystal structure of cesium tetrafluoroarsenate(III)Klampfer P, Benkič P, Lesar A, Volavšek B, Ponikvar M , Jesih A., Collect. Czech. Chem. Commun. 2004, 69, 339-350 எஆசு:10.1135/cccc20040339
- ↑ Alkali-metal heptafluorodiarsenates(III): their preparation and the crystal structure of the potassium salt, Edwards A.J., Patel S.N., J. Chem. Soc., Dalton Trans., 1980, 1630-1632, எஆசு:10.1039/DT9800001630
- ↑ Fluoride crystal structures. Part XV. Arsenic trifluoride–antimony pentafluoride, Edwards A. J., Sills R. J. C. J. Chem. Soc. A, 1971, 942 - 945, எஆசு:10.1039/J19710000942