பிசுமத் பென்டாபுளோரைடு

| |

| |
| பெயர்கள் | |
|---|---|
| வேறு பெயர்கள்
பிசுமத்(V) புளோரைடு
| |
| இனங்காட்டிகள் | |
| 7787-62-4 | |
| ChEBI | CHEBI:30426 |
| ChemSpider | 21172752 |
InChI
| |
| யேமல் -3D படிமங்கள் | Image |
| பப்கெம் | 123260 |
SMILES
| |
| பண்புகள் | |
| BiF5 | |
| வாய்ப்பாட்டு எடை | 303.97 கி மோல்−1 |
| தோற்றம் | வெண்மை ஊசிகள்,[1] நிறமற்ற திண்மப் படிகங்கள்[2] |
| அடர்த்தி | 5.40 கி செ.மீ−3[1] |
| உருகுநிலை | 151.4 °C (304.5 °F; 424.5 K) ,[2] 154.4 °C[1] |
| கொதிநிலை | 230 °C (446 °F; 503 K)[1][2] |
| கட்டமைப்பு | |
| ஒருங்கிணைவு வடிவியல் |
எண்முகம் Bi |
| தீங்குகள் | |
| தொடர்புடைய சேர்மங்கள் | |
| ஏனைய எதிர் மின்னயனிகள் | பிசுமத் முக்குளோரைடு, பிசுமத் முப்புரோமைடு, பிசுமத் மூவயோடைடு, |
| ஏனைய நேர் மின்அயனிகள் | பாசுபர பென்டாபுளோரைடு, ஆர்சனிக் பென்டாபுளோரைடு, |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
| Infobox references | |
பிசுமத் பென்டாபுளோரைடு (Bismuth pentafluoride) என்பது BiF
5 என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட ஒரு கரிம வேதியியல் சேர்மமாகும். வெண்மை நிறத்திண்மமாக காணப்படும் இச்சேர்மம் உயர் வினைத்திறன் கொண்டுள்ளது. குறிப்பிட்ட ஒரு பண்பு என்றில்லாமல், இச்சேர்மம் ஆய்வாளர்களின் கவனத்தை பெரிதும் ஈர்த்து வருகிறது.
கட்டமைப்பு[தொகு]
மாறுபக்க மூலைகலைப் பகிர்ந்து கொள்ளும் BiF6 எண்முகங்களால் ஆன ஒரு பரிமாணச் சங்கிலிகள் கொண்டிருக்கும் பலபடிசார் கட்டமைப்பை BiF5 சேர்மம் ஏற்றுள்ளது. [1][3] This is the same structure as α-UF5.[1]
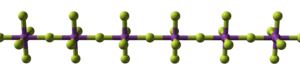  |
  |
தயாரிப்பு[தொகு]
பிசுமத் முப்புளோரைடுடன் (BiF3) புளோரினை 500 பாகை செல்சியசு வெப்பநிலைக்கு சூடுபடுத்தினால் பிசுமத் பென்டாபுளோரைடு உருவாகிறது [2].
- BiF3 + F2 → BiF5
மற்றொரு மாற்று தொகுப்பு முறையில் குளொரின் முப்புளோரைடு (ClF3) 350 பாகை செல்சியசு வெப்பநிலையில் ஒரு புளோரினேற்றும் முகவராகச் செயல்பட்டு பிசுமத் பென்டாபுளோரைடு உருவாகிறது.
- BiF3 + ClF3 → BiF5 + ClF
வினைகள்[தொகு]
நெடுங்குழு 15 தனிமங்களில் அதிக வினைத்திறம் மிக்க சேர்மமாகவும் மிக வலிமையான புளோரினேற்றும் முகவராகவும் பிசுமத் பென்டாபுளோரைடு காணப்படுகிறது. தண்ணீருடன் தீவிரமாக வினைபுரிந்து அல்லது அறைவெப்ப நிலையி கந்தகம் அல்லது அயோடின் உடன் வினைபுரிந்து ஓசோனையும் ஆக்சிசன் இருபுளோரைடையும் கொடுக்கிறது.
BiF5 பாரபீன் எண்ணெய்களுடன் வினைபுரிந்து 50 பாகை செல்சியசு வெப்பநிலைக்கு மேல் புளோரினேற்றம் செய்து புளோரோகார்பன்களைக் கொடுக்கிறது. 150 ° செ வெப்பநிலையில் UF4 சேர்மத்தை UF6 ஆகவும்180 ° செ வெப்பநிலையில் Br2 வை BrF3 ஆகவும், Cl2 வை ClF.ஆக்வும் ஆக்சிசனேற்றம் செய்கிறது. [1] காரவுலோக புளோரைடுகளுடன் BiF5 வினைபுரிந்து எக்சாபுளோரோபிசுமத்தேட்டு எதிர்மின் அயனிகள் [BiF6]−.கொண்ட எக்சாபுளோரோபிசுமத்தேட்டு M[BiF6] உருவாகிறது [2].
மேற்கோள்கள்[தொகு]
- ↑ 1.0 1.1 1.2 1.3 1.4 1.5 1.6 Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ). Butterworth–Heinemann. பக். 561–563. பன்னாட்டுத் தரப்புத்தக எண்:0080379419.
- ↑ 2.0 2.1 2.2 2.3 2.4 Holleman, A. F.; Wiberg, E. (2001), Inorganic Chemistry, San Diego: Academic Press, pp. 769–770, ISBN 0-12-352651-5
- ↑ C. Hebecker (1971). "Zur Kristallstruktur von Wismutpentafluorid". Z. anorg. allg. Chem. 384 (2): 111–114. doi:10.1002/zaac.19713840204.
- ↑ A. I. Popov; A. V. Scharabarin; V. F. Sukhoverkhov; N. A. Tchumaevsky (1989). "Synthesis and properties of pentavalent antimony and bismuth fluorides". Z. anorg. allg. Chem. 576 (1): 242–254. doi:10.1002/zaac.19895760128.
