கால்சியம் புளோரைடு
| |||

| |||
| இனங்காட்டிகள் | |||
|---|---|---|---|
| 7789-75-5 | |||
| ChEBI | CHEBI:35437 | ||
| ChemSpider | 23019 | ||
| EC number | 232-188-7 | ||
| யேமல் -3D படிமங்கள் | Image | ||
| பப்கெம் | 24617 | ||
| வே.ந.வி.ப எண் | EW1760000 | ||
SMILES
| |||
| UNII | O3B55K4YKI | ||
| பண்புகள் | |||
| CaF2 | |||
| வாய்ப்பாட்டு எடை | 78.07 g·mol−1 | ||
| தோற்றம் | வெண்ணிறப் படிகத் திண்மம் (தனித்த படிகங்கள் ஒளி ஊடுருவும் பண்புடையவை) | ||
| அடர்த்தி | 3.18 கி/செமீ3 | ||
| உருகுநிலை | 1,418 °C (2,584 °F; 1,691 K) | ||
| கொதிநிலை | 2,533 °C (4,591 °F; 2,806 K) | ||
| 0.015 கி/லி (18 °செ) 0.016 கி/லி (20 °செ) | |||
கரைதிறன் பெருக்கம் (Ksp)
|
3.9 × 10−11 [1] | ||
| கரைதிறன் | அசிட்டோனில் கரைவதில்லை அமிலத்தில் சிறிதளவு கரையும் | ||
| -28.0·10−6 செமீ3/மோல் | |||
| ஒளிவிலகல் சுட்டெண் (nD) | 1.4338 | ||
| கட்டமைப்பு | |||
| படிக அமைப்பு | கன சதுர அமைப்பு, cF12[2] | ||
| புறவெளித் தொகுதி | Fm3m, #225 | ||
| ஒருங்கிணைவு வடிவியல் |
Ca, 8, கனசதுரம் F, 4, நான்முகி | ||
| தீங்குகள் | |||
| முதன்மையான தீநிகழ்தகவுகள் | அடர் சல்பூரிக் அமிலத்தில் கரைந்து வினைபுரிந்து ஐதரோபுளோரிக் அமிலத்தைத் தருகிறது. | ||
| பொருள் பாதுகாப்பு குறிப்பு தாள் | ICSC 1323 | ||
| R-சொற்றொடர்கள் | R20, R22, R36, R37, R38 | ||
| S-சொற்றொடர்கள் | S26, S36 | ||
| தீப்பற்றும் வெப்பநிலை | எளிதில் தீப்பற்றாதது | ||
| Lethal dose or concentration (LD, LC): | |||
LDLo (Lowest published)
|
>5000 மிகி/கிகி (வாய்வழி, கினிப் பன்றி) 4250 மிகி/கிகி (வாய்வழி, எலி)[3] | ||
| தொடர்புடைய சேர்மங்கள் | |||
| ஏனைய எதிர் மின்னயனிகள் | கால்சியம் குளோரைடு கால்சியம் புரோமைடு கால்சியம் அயோடைடு | ||
| ஏனைய நேர் மின்அயனிகள் | பெரிலியம் புளோரைடு மக்னீசியம் புளோரைடு இசுட்ரோன்சியம் புளோரைடு பேரியம் புளோரைடு | ||
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |||
| | |||
| Infobox references | |||
கால்சியம் புளோரைடு (Calcium fluoride) என்பது கால்சியம் மற்றும் புளோரின் ஆகிய தனிமங்கள் இணைந்த CaF2 என்ற மூலக்கூற்று வாய்ப்பாட்டை உடைய ஒரு கனிமச் சேர்மம் ஆகும். இது வெண்ணிறத்தை உடைய, நீரில் கரையாத ஒரு திண்மம் ஆகும். இது தன்னில் கலந்துள்ள மாசுகளின் காரணமாக, அடர்ந்த நிறமுடைய புளோரைட்டு (ஃபுளோர்ஸ்பார் எனவும் அழைக்கப்படுகிறது) என்ற கனிமூலத்தில் கிடைக்கப் பெறுகிறது.
வேதியியல் அமைப்பு[தொகு]
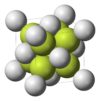
இந்தச் சேர்மமானது ஒரு கன சதுர வடிவ அலங்கார வடிவமான புளோரைட்டு வடிவத்தில் படிகமாகிறது.

Ca2+ அயனியானது எட்டு ஈந்திணைவுக்கோளத்தின் மையத்தில், எட்டு F− அயனிகளாலான கனசதுரப் பெட்டியின் மையமாக உள்ளது. ஒவ்வொரு F− அயனி மையமும் நான்கு Ca2+ மையங்களோடு அணைவுப்பிணைப்பில் உள்ளது.[5] மிகவும் சரியான முறையில் கூட்டிணைக்கப்பட்ட படிக மாதிரிகள் நிறமற்றவையாக இருப்பினும், கனிமூலமானது பெரும்பாலும் F-மையங்கள் இருப்பின காரணமாக அடர் நிறமுடையவையாக இருக்கின்றன. இதே படிக அமைப்பானது, CeO2, கனசதுர ZrO2, யுரேனியம் டைஆக்சைடு(UO2), தோரியம் டை ஆக்சைடு(ThO2), மற்றும் புளூட்டோனியம் டை ஆக்சைடு (PuO2) போன்ற AB2 என்ற மூலக்கூற்று வாய்ப்பாட்டை உடைய சேர்மங்கள் யாவிலும் காணப்படுகிறது.
தயாரிப்பு[தொகு]
ஐதரோபுளோரிக் அமிலத்தின் முன்னோடியாக உள்ள வகையில் விரும்பத்தக்க புளோரைட்டு கனிமூலமானது மிகுதியாகவும், பரவலாகவும் கிடைக்கிறது. ஆகையைால், சிறிதளவு ஊக்குவிப்பானது CaF2 தொழிலக தயாரிப்பிற்காக நிலைத்திருக்கிறது. மிகுந்த துாய்மையான CaF2 கால்சியம் கார்பனேட்டு மற்றும் ஐதரோபுளோரிக் அமிலம் ஆகியவற்றை வினைபுரியச் செய்வதன் மூலம் தயாரிக்கப்படுகிறது:[6]
- CaCO3 + 2 HF → CaF2 + CO2 + H2O
பயன்பாடுகள்[தொகு]
பலதரப்பட்ட வேதிவிளைபொருட்களைத் தயாரிக்கப் பயன்படும் ஐதரசன் புளோரைடு தயாரிப்பதற்கான இயற்கையான முதன்மை மூலப்பொருளாக CaF2 இருக்கிறது. கால்சியம் புளோரைடு புளோரைட்டு நிலையில் வணிகவியல் முக்கியத்துவம் வாய்ந்த புளோரைடின் மூலப்பொருளாக இருக்கிறது.[7] கனிமூலத்தின் மீது அடர் கந்தக அமிலம் செயல்படுவதன் விளைவாக ஐதரசன் புளோரைடு விடுவிக்கப்படுகிறது.[8]
- CaF2 + H2SO4 → CaSO4(திண்மம்) + 2 HF
பாதுகாப்பு[தொகு]
கந்தக அமிலத்துடன் வினைப்படுத்தும் போது நச்சுத்தன்மையுள்ள ஐதரோபுளோரிக் அமிலத்தை வெளியிடுகிறது. இருப்பினும் கூட இது CaF2 ஆபத்தற்றது என்று வகைப்படுத்தப்பட்டுள்ளது. தொழில்முறை பாதுகாப்பு மற்றும் நலத்திற்கான தேசிய நிறுவனம் காற்றில் புளோரின் கொண்டுள்ள தூசுகள் உட்சுவாசிப்பதற்கான நிர்ணயிக்கப்பட்ட அளவாக 2.5 மிகி/மீ3 [6] என்பதைப் பரிந்துரைத்துள்ளது.
மேற்கோள்கள்[தொகு]
- ↑ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, பன்னாட்டுத் தரப்புத்தக எண் 0-07-049439-8
- ↑ X-ray Diffraction Investigations of CaF2 at High Pressure, L. Gerward, J. S. Olsen, S. Steenstrup, M. Malinowski, S. Åsbrink and A. Waskowska, Journal of Applied Crystallography (1992), 25, 578-581 எஆசு:10.1107/S0021889892004096
- ↑ "Fluorides (as F)". Immediately Dangerous to Life and Health. National Institute for Occupational Safety and Health (NIOSH).
- ↑ Burr, P. A.; Cooper, M. W. D. (2017-09-15). "Importance of elastic finite-size effects: Neutral defects in ionic compounds". Physical Review B 96 (9): 094107. doi:10.1103/PhysRevB.96.094107. https://link.aps.org/doi/10.1103/PhysRevB.96.094107.
- ↑ G. L. Miessler and D. A. Tarr “Inorganic Chemistry” 3rd Ed, Pearson/Prentice Hall publisher, பன்னாட்டுத் தரப்புத்தக எண் 0-13-035471-6.
- ↑ 6.0 6.1 Aigueperse, Jean; Mollard, Paul; Devilliers, Didier; Chemla, Marius; Faron, Robert; Romano, René; Cuer, Jean Pierre (2000). Fluorine Compounds, Inorganic. doi:10.1002/14356007.a11_307.
- ↑ Aigueperse, Jean; Mollard, Paul; Devilliers, Didier; Chemla, Marius; Faron, Robert; Romano, Renée; Cuer, Jean Pierre (2005), "Fluorine Compounds, Inorganic", Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, p. 307, doi:10.1002/14356007.a11_307.
- ↑ Holleman, A. F.; Wiberg, E. "Inorganic Chemistry" Academic Press: San Diego, 2001. பன்னாட்டுத் தரப்புத்தக எண் 0-12-352651-5.