கால்சியம் சல்பேட்டு
| |

| |
| பெயர்கள் | |
|---|---|
| வேறு பெயர்கள் | |
| இனங்காட்டிகள் | |
| 7778-18-9 10034-76-1 (அரைநீருடையி) 10101-41-4 (dihydrate) | |
| ChEBI | CHEBI:31346 |
| ChemSpider | 22905 |
| யேமல் -3D படிமங்கள் | Image |
| KEGG | D09201 |
| பப்கெம் | 24928 |
| வே.ந.வி.ப எண் | WS6920000 |
SMILES
| |
| UNII | E934B3V59H |
| பண்புகள் | |
| CaSO4 | |
| வாய்ப்பாட்டு எடை | 136.14 g/mol (anhydrous) 145.15 g/mol (hemihydrate) 172.172 g/mol (dihydrate) |
| தோற்றம் | white solid |
| மணம் | odorless |
| அடர்த்தி | 2.96 g/cm3 (anhydrous) 2.32 g/cm3 (dihydrate) |
| உருகுநிலை | 1,460 °C (2,660 °F; 1,730 K) (anhydrous) |
| 0.21g/100ml at 20 °C (anhydrous)[1] 0.24 g/100ml at 20 °C (dihydrate)[2] | |
கரைதிறன் பெருக்கம் (Ksp)
|
4.93 × 10−5 mol2L−2 (anhydrous) 3.14 × 10−5 (dihydrate) [3] |
| கிளிசரால்-இல் கரைதிறன் | slightly soluble (dihydrate) |
| காடித்தன்மை எண் (pKa) | 10.4 (anhydrous) 7.3 (dihydrate) |
| கட்டமைப்பு | |
| படிக அமைப்பு | orthorhombic |
| வெப்பவேதியியல் | |
| Std enthalpy of formation ΔfH |
-1433 kJ/mol[4] |
| நியம மோலார் எந்திரோப்பி S |
107 J·mol−1·K−1 [4] |
| தீங்குகள் | |
| பொருள் பாதுகாப்பு குறிப்பு தாள் | ICSC 1589 |
| தீப்பற்றும் வெப்பநிலை | Non-flammable |
| அமெரிக்க சுகாதார ஏற்பு வரம்புகள்: | |
அனுமதிக்கத்தக்க வரம்பு
|
TWA 15 mg/m3 (total) TWA 5 mg/m3 (resp) [for anhydrous form only][5] |
பரிந்துரைக்கப்பட்ட வரம்பு
|
TWA 10 mg/m3 (total) TWA 5 mg/m3 (resp) [anhydrous only][5] |
உடனடி அபாயம்
|
N.D.[5] |
| தொடர்புடைய சேர்மங்கள் | |
| ஏனைய நேர் மின்அயனிகள் | Magnesium sulfate Strontium sulfate Barium sulfate |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
| | |
| Infobox references | |
கால்சியம் சல்பேட்டு (calcium sulphate) CaSO4 என்ற மூலக்கூறு வாய்ப்பாடுடைய கால்சியத்தின் நீரேறி கனிமச் சேர்மமாகும். γ-அன்ஹைட்ரைட் வடிவத்தில் (நீரொழிந்த வடிவம்), இது ஈரமுறிஞ்சியாகப் பயன்படுத்தப்படுகின்றது. ஒரு குறிப்பிட்ட வகை நீரேறி பாரிசு பூச்சாகவும் மற்றொரு வகை இயற்கையாகக் கிடைக்கும் ஜிப்சமும் ஆகும். இதற்கு தொழில்துறையில் பல பயன்பாடுகள் உள்ளன. அனைத்து வடிவங்களுமே வெள்ளை திண்மமாகவும் நீரில் எளிதில் கரையாதும் கிடைக்கின்றன.[6]
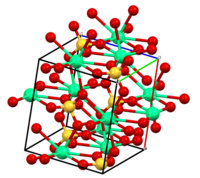
கட்டமைப்புகள்[தொகு]
இந்தச் சேர்மம் மூன்று நிலையிலான நீரேற்றத்துடன் கிடைக்கின்றன:
- நீரொழிந்த வடிவம் (கனிமப் பெயர்: "அன்ஹைட்ரைட்"), மூலக்கூறு வாய்ப்பாடு: CaSO4.[7]
- இருநீருடையி (கனிமப் பெயர்: "ஜிப்சம்") மூலக்கூறு வாய்ப்பாடு: CaSO4(H2O)2.[8]
- அரைநீருடையி, மூலக்கூறு வாய்ப்பாடு: CaSO4(H2O)0.5. குறிப்பிட்ட அரைநீருடையிக்கள் சிலசமயங்களில் ஆல்ஃபா-அரைநீருடையி, பீட்டா-அரைநீருடையி என அடையாளப்படுத்தப்படுகின்றன.[9]
மேற்சான்றுகள்[தொகு]
- ↑ S. Gangolli (1999). The Dictionary of Substances and Their Effects: C. Royal Society of Chemistry. பக். 71. பன்னாட்டுத் தரப்புத்தக எண்:0-85404-813-8. http://books.google.com/books?id=s4YittJrOsAC&pg=PA71.
- ↑ American Chemical Society (2006). Reagent chemicals: specifications and procedures : American Chemical Society specifications, official from January 1, 2006. Oxford University Press. பக். 242. பன்னாட்டுத் தரப்புத்தக எண்:0-8412-3945-2. http://books.google.com/books?id=JXO-HdRnTl0C&pg=PA242.
- ↑ D.R. Linde (ed.) "CRC Handbook of Chemistry and Physics", 83rd Edition, CRC Press, 2002
- ↑ 4.0 4.1 Zumdahl, Steven S. (2009). Chemical Principles 6th Ed.. Houghton Mifflin Company. பக். A21. பன்னாட்டுத் தரப்புத்தக எண்:0-618-94690-X. https://archive.org/details/chemicalprincipl0000zumd_u9g0.
- ↑ 5.0 5.1 5.2 "NIOSH Pocket Guide to Chemical Hazards #0095". National Institute for Occupational Safety and Health (NIOSH).
- ↑ Franz Wirsching "Calcium Sulfate" in Ullmann's Encyclopedia of Industrial Chemistry, 2012 Wiley-VCH, Weinheim. எஆசு:10.1002/14356007.a04_555
- ↑ Morikawa, H.; Tomita, T.; Minato, I.; Iwai, S. I. "Anhydrite: a Refinement" Acta Crystallographica B (24,1968-38,1982) (1975) 31, p2164-p2165.
- ↑ A .refinement of the Crystal Structure of gypsum CaSO4(H2O)2" Cole, W. F.; Lancucki, C.J. Acta Crystallographica B 1982, volume 24, pp.1968.
- ↑ H F W Taylor, Cement Chemistry, Academic Press, 1990, பன்னாட்டுத் தரப்புத்தக எண் 0-12-683900-X, pp. 186-187
