பெரிலியம் குளோரைடு

| |
| பெயர்கள் | |
|---|---|
| ஐயூபிஏசி பெயர்
பெரிலியம் குளோரைடு
| |
| இனங்காட்டிகள் | |
| 7787-47-5 | |
| ChemSpider | 22991 |
| யேமல் -3D படிமங்கள் | Image |
| பப்கெம் | 24588 |
| வே.ந.வி.ப எண் | DS2625000 |
SMILES
| |
| பண்புகள் | |
| BeCl2 | |
| வாய்ப்பாட்டு எடை | 79.9182 g/mol |
| தோற்றம் | வெள்ளை அல்லது மஞ்சள் நிறபடிகங்கள் |
| அடர்த்தி | 1.899 g/cm3, திண்மம் |
| உருகுநிலை | 399 °C (750 °F; 672 K) |
| கொதிநிலை | 482 °C (900 °F; 755 K) |
| 15.1 g/100 mL (20 °C) | |
| கரைதிறன் | ஆல்ககால், ஈதர், பென்சீன், மற்றும் பிரிடின் ஆகியனவற்றில் கரையும் குளோரோஃபார்ம் மற்றும் கந்தக டைஆக்சைடு ஆகியனவற்றில் சிறிதளவு கரையும். |
| கட்டமைப்பு | |
| படிக அமைப்பு | அறுங்கோணம் |
| மூலக்கூறு வடிவம் | |
| வெப்பவேதியியல் | |
| Std enthalpy of formation ΔfH |
−6.136 kJ/g or -494 kJ/mol |
| Std enthalpy of combustion ΔcH |
16 kJ/mol |
| நியம மோலார் எந்திரோப்பி S |
63 J/mol K |
| வெப்பக் கொண்மை, C | 7.808 J/K or 71.1 J/mol K |
| தீங்குகள் | |
| Lethal dose or concentration (LD, LC): | |
LD50 (Median dose)
|
86 mg/kg (எலி, வாய்வழி) |
| தொடர்புடைய சேர்மங்கள் | |
| ஏனைய எதிர் மின்னயனிகள் | பெரிலியம் புளோரைடு பெரிலியம் புரோமைடு பெரிலியம் அயோடைடு |
| ஏனைய நேர் மின்அயனிகள் | மக்னீசியம் குளோரைடு கால்சியம் குளோரைடு இசிடிரான்சியம் குளோரைடு பேரியம் குளோரைடு ரேடியம் குளோரைடு |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
| | |
| Infobox references | |
பெரிலியம் குளோரைடு (Beryllium chloride) என்பது பெரிலியம் மற்றும் குளோரின் இணைந்து உருவாகும் ஒரு வேதிச் சேர்மமாகும். இதன் மூலக்கூற்று வாய்பாடு BeCl2 ஆகும் நிறமற்ற நிலையில் நீரை உறிஞ்சும் தன்மை கொண்ட திண்மமாகக் காணப்படும் இச்சேர்மம் முனைவுக் கரைப்பான்கள் பலவற்றிலும் கரைகிறது. பெரிலியம் அலுமினியத்துடன் மூலைவிட்டத் தொடர்பு கொண்டிருப்பதால் அலுமினியம் குளோரைடின் பண்பு்களுடன் பெருமளவு ஒத்திருக்கிறது.
கட்டமைப்பும் தொகுத்தலும்[தொகு]
உயர் வெப்பநிலையில் பெரிலியம் குளோரினுடன் வினைபுரிந்து பெரிலியம் குளோரைடு தயாரிக்கப்படுகிறது:[1]. .
- Be + Cl2 → BeCl2
பெரிலியம் ஆக்சைடை குளோரின் முன்னிலையில்[2] வெப்பம்சார் கார்பன் ஒடுக்கம் செய்தும், பெரிலியத்தை ஐதரசன் குளோரைடுடன் சேர்த்து வினைப்படுத்தியும் கூட பெரிலியம் குளோரைடைத் தயாரிக்க இயலும்.
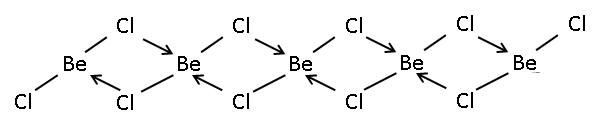
திண்மநிலை பெரிலியம் குளோரைடு, கூர்முனை நாற்பட்டகத்தைப் பெற்றுள்ள ஒரு பரிமான பலபடியாகும்[3] . இதற்கு நேர்மாறாக பெரிலியம் புளோரைடு என்பது படிகக்கல் வகைக் கனிமம் குவார்ட்சு போல ஒரு முப்பரிமான பலபடியாகும். வாயு நிலையில் இது நேரியல் ஒற்றைப்படி மற்றும் இரண்டு குளோரின்கள் இணைந்த இணைப்பு இரட்டைப்படி ஆகிய இரண்டு நிலைகளிலும் காணப்படுகிறது. இங்கு பெரிலியம் மூன்று ஆயங்களுடன் உள்ளது[4] . ஒற்றைப்படிகளின் நேரியல் வடிவத்தை வலுவளவு ஓட்டு இலத்திரன் சோடிகளின் தள்ளுகைக் கொள்கை முன்கணித்துக் கூறியது. இரண்டாவது தொகுதியில் உள்ள சில கன உலோகங்களின் நேரியல் வடிவத்துடன் இது மாறுபாடு கொண்டுள்ளது. உதாரணமாக CaF2 SrF2, BaF2, SrCl2, BaCl2, BaBr2, மற்றும் BaI2, ஆகியன நேரியல் வடிவமில்லாதவை ஆகும்.
வினைகள்[தொகு]
உலர்ந்த காற்றில் பெரிலியம் குளோரைடு நிலைப்புத்தன்மையுடன் காணப்படுகிறது. இதுவொரு இலூவிக்கமிலம் என்பதால் சில வேதி வினைகளில் வினையூக்கியாகப் பயன்படுத்துகிறார்கள். மேலும் இது நீராற் சிதைக்கப்பட்டு ஐதரசன் குளோரைடாக மாறுகிறது.
BeCl2 + 2H2O → Be(OH)2 + 2 HCl
இச்சேர்மம் நான்ம ஐதரேட்டாகவும் உருவாகிறது.BeCl2•4H2O ([Be(H2O)4]Cl2). BeCl2 ஆக்சிசனேறிய கரைப்பானான ஈதரில் கரைகிறது.[5][6]
பயன்கள்[தொகு]
மின்னாற்பகுப்பு முறையில் பெரிலியம் தயாரிப்பதற்கு பெரிலியம் குளோரைடு மூலப்பொருளாக உள்ளது. பிரீடல் கிராப்ட்சு வினையின் பொழுது இது வினையூக்கியாகப் பயன்படுகிறது.
மேற்கோள்கள்[தொகு]
- ↑ Irving R. Tannenbaum "Beryllium Chloride" Inorganic Syntheses, 1957, vol. 5, p. 22. எஆசு:10.1002/9780470132364.ch7
- ↑ Cotton, F. A.; Wilkinson, G. (1980) Advanced Inorganic Chemistry John Wiley and Sons, Inc: New York, பன்னாட்டுத் தரப்புத்தக எண் 0-471-02775-8.
- ↑ Wells, A. F. (1984) Structural Inorganic Chemistry, Oxford: Clarendon Press. பன்னாட்டுத் தரப்புத்தக எண் 0-19-855370-6.
- ↑ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ). Butterworth-Heinemann. பன்னாட்டுத் தரப்புத்தக எண்:0080379419.
- ↑ Lide, David R., தொகுப்பாசிரியர் (2006). CRC Handbook of Chemistry and Physics (87th ). Boca Raton, FL: CRC Press. பன்னாட்டுத் தரப்புத்தக எண்:0-8493-0487-3.
- ↑ Holleman, A. F.; Wiberg, E. (2001) Inorganic Chemistry Academic Press: San Diego, பன்னாட்டுத் தரப்புத்தக எண் 0-12-352651-5
வெளி இணைப்புகள்[தொகு]
- Beryllium chloride at IPCS INTOX databank
- Properties of BeCl2 from NIST