பாதரச(I) குளோரைடு

| |

| |
| பெயர்கள் | |
|---|---|
| ஐயூபிஏசி பெயர்
டைமெர்குரி டைகுளோரைடு
| |
| வேறு பெயர்கள்
மெர்குரசு குளோரைடு
கலோமல் | |
| இனங்காட்டிகள் | |
| 10112-91-1 | |
| ChEBI | CHEBI:33050 |
| ChemSpider | 16740467 |
| EC number | 233-307-5 |
| யேமல் -3D படிமங்கள் | Image |
| பப்கெம் | 24956 |
| வே.ந.வி.ப எண் | OV8750000 |
| |
| UNII | J2D46N657D |
| UN number | 3077 |
| பண்புகள் | |
| Hg2Cl2 | |
| வாய்ப்பாட்டு எடை | 472.09 கி/மோல் |
| தோற்றம் | வெண் திண்மம் |
| அடர்த்தி | 7.150 கி/செ.மீm3 |
| உருகுநிலை | 525 °C (977 °F; 798 K) (மும்மைப் புள்ளி) |
| கொதிநிலை | 383 °C (721 °F; 656 K) (பதங்கமாகும்) |
| 0.2 மி.கி/100 மி.லி | |
| கரைதிறன் | எத்தனால், ஈதர் போன்றவற்றில் கரையாது |
| −26.0•10−6 செ.மீ3/மோல் | |
| ஒளிவிலகல் சுட்டெண் (nD) | 1.973 |
| தீங்குகள் | |
| பொருள் பாதுகாப்பு குறிப்பு தாள் | ICSC 0984 |
| ஈயூ வகைப்பாடு | நஞ்சு (T) தீங்கானது (Xn) சுற்றுச்சூழலுக்கு அபாயம் (N) |
| R-சொற்றொடர்கள் | R22, R36/37/38, R50/53 |
| S-சொற்றொடர்கள் | (S2), S13, S24/25, S46, S60, S61 |
| தீப்பற்றும் வெப்பநிலை | தீப்பற்றாது |
| Lethal dose or concentration (LD, LC): | |
LD50 (Median dose)
|
210 மி.கி/கி.கி (எலி, வாய்வழி)[1] |
| வெப்பவேதியியல் | |
| Std enthalpy of formation ΔfH |
−265 கி.யூ•மோல்−1[2] |
| நியம மோலார் எந்திரோப்பி S |
196 யூல்•மோல்mol−1•K−1[2] |
| தொடர்புடைய சேர்மங்கள் | |
| ஏனைய எதிர் மின்னயனிகள் | பாதரச(I) புளோரைடு பாதரச(I) புரோமைடு பாதரச(I) அயோடைடு |
| ஏனைய நேர் மின்அயனிகள் | பாதரச(II) குளோரைடு |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
பாதரச(I) குளோரைடு (Mercury(I) chloride) என்பது Hg2Cl2 என்ற மூலக்கூற்று வாய்ப்பாட்டால் விவரிக்கப்படும் ஒரு கனிம வேதியியல் சேர்மமாகும்.பாதரசம் மற்றும் குளோரின் தனிமங்கள் சேர்ந்து இச்சேர்மம் உருவாகிறது. பாதரசம்(I) சேர்மத்திற்கு இதுவே முதன்மையான உதாரணமாகும். இச்சேர்மம் கலோமல்[3] அல்லது மெர்குரசு குளோரைடு என்ற பெயரில் மிகவும் அரிய பாதரசத்தின் கனிமமாகவும் அறியப்படுகிறது. அடர் வெண்மை நிறம் அல்லது மஞ்சள் கலந்த வெண்மை நிறத்தைக் கொண்டு நெடியற்ற திண்மமாக பாதரச(I) குளோரைடு காணப்படுகிறது. மின்வேதியியலில் நிறைவுற்ற தரவு மின்முனையின் ஒரு பகுதிக்கூறாக இச்சேர்மம் பயன்படுத்தப்படுகிறது [4][5].
வரலாறு
[தொகு]அழகு, கருப்பு மற்றும் இனிப்புச் சுவை ஆகிய பொருள்கள் கொண்ட கிரேக்க மொழிச் சொற்களிலிருந்து கலோமல் என்ற சொல் உருவாக்கப்பட்டுள்ளது[3] வெண்மை நிறங்கொண்ட இச்சேர்மத்திற்கு கருப்பு நிறம் என்ற பொருள் கொண்ட சொல்லைப் பயன்படுத்தியது ஆச்சரியமானதாக இருக்கலாம். அநேகமாக அமோனியாவுடன் இச்சேர்மம் ஈடுபடும் விகிதச்சமனிலாத வினையில் அற்புதமான கருப்பு நிறத்துடன் சிதறிய பாதரசத்தை முன்னிறுத்தியதாக கருதலாம். மேலும் ஆர்ன் குயிக்சில்வர் அல்லது ஆர்ன் மெர்க்குரி என்ற பாதரசக் கனிமத்தைக் குறிப்பதாகவும் இருக்கலாம்.[3].
ஒரு மலமிளக்கியாகவும் [3] கிருமி நீக்கியாகவும் 1801 ஆம் ஆண்டில் ஐக்கிய இராச்சியத்தின் மூன்றாம் ஜார்ஜ்| ஐக்கிய இராச்சியத்தின் மூன்றாம் சியார்ச்சுக்கு]] சிகிச்சையளிக்க கலோமல் உள்மருந்தாகப் பயன்படுத்தப்பட்டது. 20 ஆம் நூற்றாண்டின் முற்பகுதி வரை கிரந்தி நோய்க்கான சிகிச்சையிலும் கலோமல் பயன்படுத்தியுள்ளனர். மேலும் ஒரு தோட்டக்கலை பூசணமாகவும் குறிப்பாக பிராசிகேசியே குடும்பப் பயிர்களின் வேரை அமிழ்த்தி வேர்வீக்கம் ஏற்படுவதை தடுக்கவும் பயன்படுத்தப்பட்டுள்ளது[6].
பல்வேறு உடல் மற்றும் மன நோய்களுக்கு மருந்தாகப் பயன்படுத்தப்பட்டு பாதரசம் ஒரு பிரபலமான நோய்த்தீர்வாக மாறியது. நோயாளிகளின் உடலில் உள்ள அசுத்தங்களை நீக்கி வேகமாக அவர்கள் இயல்பு நிலைக்குத் திரும்பும் நோக்கில் அமெரிக்க மருத்துவர்கள் 18 ஆம் நூற்றாண்டு முழுவதும் இதைப் பயன்படுத்தினர். பாதரசத்தை மருந்தாகப் பயன்படுத்தியவர்களில் பெஞ்சமின் ரசு குறிப்பிடத்தகுந்தவர் ஆவார். 1793 ஆம் ஆண்டு பிலடெப்பியாவில் மஞ்சள் காய்ச்சல் பாதித்தவர்களுக்கு சிகிச்சையளிக்க இவர் கலோமலைப் பயன்படுத்தினார். நோயாளிகளின் வயிற்றை சுத்தப்படுத்தும் மருந்து அல்லது பேதி மருந்தாக கலோமல் வழங்கப்பட்டது. பெரும்பாலும் நோயாளிகளின் முடி மற்றும் பற்கள் விழுவதை கவனத்தில் கொண்டு மருந்து நிர்வாகம் மேற்கொள்ளப்பட்டது [7].
பிலடெல்பியாவை மஞ்சள் காய்ச்சல் தாக்கிய சிறிது காலத்திற்குள் அந்த நோய் யமைக்காவில் பரவியது. இரத்தப்போக்கு அல்லது கலோமல் இரண்டில் எது மஞ்சள் காய்ச்சலுக்கான சிறந்த சிகிச்சை என்று பத்திரிகைகளில் பெரும் விவாதப் போர் நிகழ்ந்தது. இரத்தப்போக்கை விட கலோமல் மிகவும் பயனுள்ளதாக இருந்ததாக கருதுகோள் சான்றுகள் கூறுகின்றன [8]. லூயிசு மற்றும் கிளார்க் ஆகியோர் கலோமலை அவர்கள் காலத்தின் சிறந்த மருந்தாக, டிஞ்சர் எனப்படும் குழம்பு மற்றும் களிம்பாகப் பயன்படுத்தினர். நவீன ஆராய்ச்சியாளர்களும் இதே போல பாதரசத்தை பயன்படுத்துகின்றனர்[9].
பண்புகள்
[தொகு]12 ஆவது குழுத்தனிமங்களில் பாதரசம் தனித்தன்மை வாய்ந்தது ஆகும். M-M பிணைப்பை உடனடியாக உருவாக்கும் திறனுக்காக இவ்வாறு அது கருதப்படுகிறது. Hg2Cl2 என்பது ஒரு நேர்கோட்டு மூலக்கூறு ஆகும். I4/m 2/m 2/m என்ற இடக்குழுக்களுடன் நாற்கோணகப் படிகத்திட்டத்தில் கலோமல் கனிமம் படிகமாகிறது. படிகக் கட்டமைப்பின் ஓர் அலகு செல் கீழே காட்டப்பட்டுள்ளது:
 |
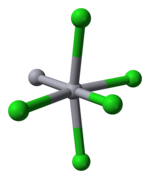 |
Hg–Hg பிணைப்பின் நீளம் 253 பைக்கோ மீட்டர் (உலோகத்தில் Hg–Hg பிணைப்பு 300 பைக்கோ மீட்டர்) மற்றும் நேர்கோட்டு Hg2Cl2 அலகில் Hg–Cl பிணைப்பின் நீளம் 243 பைக்கோ மீட்டர் ஆகும்.[10] ஒட்டுமொத்த ஒருங்கிணைவில் இடம்பெற்றுள்ள ஒவ்வொரு பாதரச அணுவும் எண் கோணங்களாகும். கூடுதலாக இவற்றுக்கு அருகாமையில் உள்ள இரண்டு பாதரச அணுக்களின் பல்நேரயனிகளுடன் 321 பைக்கோ மீட்டர் தொலைவில் நான்கு குளோரின் அணுக்கள் காணப்படுகின்றன.
தயாரிப்பு மற்றும் வினைகள்
[தொகு]தனிம நிலை பாதரசமும் பாதரச(II) குளோரைடும் வினைபுரிவதனால் பாதரச(I) குளோரைடு உருவாகிறது.
- Hg + HgCl2 → Hg2Cl2
குளோரைடு மூலங்களான சோடியம் குளோரைடு அல்லது ஐதரசன் குளோரைடு போன்றவற்றைப் பயன்படுத்தி நீரிய பாதரச(I) நைட்ரேட்டை கூறிடம்பெயரல் வினைக்கு உட்படுத்துவதாலும் இதைத் தயாரிக்கலாம்.
- 2HCl + Hg2(NO3)2 → Hg2Cl2 + 2HNO3
Hg2Cl2 சேர்மத்தை அமோனியா விகிதச்சமமற்றதாக மாற்றுகிறது.
- Hg2Cl2 + 2NH3 → Hg + Hg(NH2)Cl + NH4Cl
கலோமல் மின்முனை
[தொகு]பாதரச(I) குளோரைடு சேர்மம் இதன் தனித்துவமான ஆக்சிசனேற்ற ஒடுக்க பண்புகளின் காரணமாக மின் வேதியியலில் விரிவாகப் பயன்படுத்தப்படுகிறது. முற்காலத்தில் கலோமல் மின்முனையை தரவு மின்முனை என்று கருதுவர். கடந்த 50 ஆண்டுகளாக வெள்ளி/வெள்ளி குளோரைடு மின்வாய்கள் மேலோங்கிய பயன்பாட்டில் உள்ளன. பாதரசத்தின் அபாயகரமான நச்சுத்தன்மை காரணமாக பாதரச மின்வாய்கள் தடைசெய்யப்பட்டிருந்தாலும் பல வேதியியலர்கள் பாதரச மின்வாய்களின் துல்லியத்தை இன்னமும் நம்புகின்றனர். முறையாக கையாளப்பட்டால் இவை அபாயமற்றவை என்றும் அவர்கள் கூறுகிறார்கள்.
ஒளி வேதியியல்
[தொகு]பாதரச(I) குளோரைடு சிதைவடைந்து பாதரச(II) குளோரைடாக மாறுகிறது மற்றும் புற ஊதா ஒளியில் படநேர்ந்தால் தனிமநிலை பாதரசமாகிறது.
- Hg2Cl2 → HgCl2 + Hg
ஒளிக்கற்றையில் இடம்பெற்றுள்ள போட்டன்களின் எண்ணிக்கையைக் கணக்கிட பாதரசத்தின் உற்பத்தி கதிர் செறிவு அளவியில் பயன்படுத்தப்படுகிறது.
பாதரச(II) குளோரைடு மற்றும் அமோனியம் ஆக்சலேட்டு முன்னிலையில் ஒளி வினையை நிகழ்த்தினால் பாதரச(I) குளோரைடு, அமோனியம் குளோரைடு மற்றும் கார்பனீராக்சைடு முதலியன உற்பத்தியாகின்றன.
- 2HgCl2 + (NH4)2C2O4 + Light → Hg2Cl2(s) + 2[NH4+][Cl−] + 2CO2
1880 ஆம் ஆண்டில் யே. எம். ஈடர் முதன்முதலில் குறிப்பிட்ட இவ்வினையைக் கண்டறிந்தார் என்பதால் ஈடர் வினை என்ற பெயராலும் இவ்வினையை அடையாளப்படுத்துவர். டபிள்யூ.ஈ ரோசிவேயர் 1929 இல் இவ்வினையை மறு ஆய்வு செய்தார்.[11].
தொடர்புடைய பாதரச(I) சேர்மங்கள்
[தொகு]பாதரச(I) புரோமைடு Hg2Br2 சேர்மம் இளமஞ்சள் நிறத்திலும் பாதரச(I) அயோடைடு Hg2I2 நிறத்திலும் காணப்படுகின்றன. இரண்டுமே குறைந்த கரைதிறன் கொண்டவையாகும். வலிமையான அமிலங்கள் இல்லாதபோது பாதரச(I) புளோரைடு நிலைப்புத்தன்மையைக் குறைவாகக் கொண்டிருக்கும்.
முன்பாதுகாப்பு
[தொகு]பாதரச(I) குளோரைடு நச்சுத்தன்மையுடையது, இருப்பினும் நீரில் இதன் குறைவான கரைதிறன் காரணமாக பாதரச(II) குளோரைடைக் காட்டிலும் பொதுவாக இது ஆபத்துக் குறைவானது. 1700 ஆம் ஆண்டுகளின் பிற்பகுதியில் இருந்து 1860 ஆம் ஆண்டுகள் வரை அமெரிக்காவில் சிறுநீர்பிரிப்பு மற்றும் மலமிளக்கி மருந்துகளாகப் பயன்படுத்தப்பட்டது. 1954 ஆம் ஆண்டு வரை பிரிட்டனில் பல்துலக்கும் பொடிகளில் கலோமலும் ஒரு பொதுவான உட்பொருளாக இருந்தது. குழந்தைகளில் கை மற்றும் பாதங்களில் முனைவலி எனப்படும் இளஞ்சிவப்பு நோய் தோன்றுவதற்கு கலோமல் காரணமாக இருந்துள்ளது. அந்த நேரத்தில் இதன் இறப்பு விகிதம் 10 இல் 1 ஆகும் [12]. இதன் நச்சுத்தன்மை கண்டறியப்பட்டவுடன் கலோமலின் மருத்துவப் பயன்பாடுகள் கைவிடப்பட்டன.
குளியல் சோப்புகளிலும் தோல் மென்மையாக்கிகளிலும் கலோமலை பயன்படுத்த இயலும். அமெரிக்கா, கனடா, சப்பான் மற்றும் ஐரோப்பிய ஒன்றியம் முதலான நாடுகளில் தற்போது இப்பயன்பாடு சட்டப்படி குற்றமாகும் [13]. இத்தகைய அழகியல் பொருள்களை உற்பத்தி செய்யும் தொழிலாளர்களிடம் மேற்கொள்ளப்பட்ட ஓர் ஆய்வில், 2,3-டைமெர்காப்டோ-1-புரோப்பேன் சல்போனிக் அமிலத்தின் சோடியம் உப்பைக் கொடுத்து சோதித்த போது சிறுநீரில் பாதரசத்தின் செறிவு சாதாரண நிலைக்கு குறைவது கண்டறியப்பட்டது [14].
மேற்கோள்கள்
[தொகு]- ↑ "Mercury compounds [except (organo) alkyls] (as Hg)". Immediately Dangerous to Life and Health. National Institute for Occupational Safety and Health (NIOSH).
- ↑ 2.0 2.1 Zumdahl, Steven S. (2009). Chemical Principles 6th Ed. Houghton Mifflin Company. p. A22. பன்னாட்டுத் தரப்புத்தக எண் 978-0-618-94690-7.
- ↑ 3.0 3.1 3.2 3.3
 "Calomel". பிரித்தானிக்கா கலைக்களஞ்சியம் (11th). (1911). Cambridge University Press.
"Calomel". பிரித்தானிக்கா கலைக்களஞ்சியம் (11th). (1911). Cambridge University Press.
- ↑ வார்ப்புரு:Housecroft2nd
- ↑ Skoog, Douglas A.; Holler, F. James; Nieman, Timothy A. (1998). Principles of Instrumental Analysis (5th ed.). Saunders College Pub. pp. 253–271. பன்னாட்டுத் தரப்புத்தக எண் 978-0-03-002078-0.
- ↑ Buczacki, S., Pests, Diseases and Disorders of Garden Plants, Collins, 1998, pp 449-50. பன்னாட்டுத் தரப்புத்தக எண் 0-00-220063-5
- ↑ Koehler, Christopher S. W. (January 2001). "Heavy Metal Medicine". Today's Chemist at Work 10 (1): 61–65. பன்னாட்டுத் தர தொடர் எண்:1062-094X. http://pubs.acs.org/subscribe/journals/tcaw/10/i01/html/01chemch.html. பார்த்த நாள்: 2009-02-02.
- ↑ Johnston, Elizabeth Lichtenstein (1901). Recollections of a Georgia Loyalist...written in 1836. New York: Mansfield & Company. pp. 82-83.
- ↑ Inglis-Arkell, Esther. "Archaeologists Tracked Lewis and Clark by Following Their Trail of Laxatives" (in en-US). io9. https://io9.gizmodo.com/archaeologists-tracked-lewis-and-clark-by-following-the-1727887223?commerce_insets_disclosure=on.
- ↑ Wells A.F. (1984) Structural Inorganic Chemistry 5th edition Oxford Science Publications பன்னாட்டுத் தரப்புத்தக எண் 0-19-855370-6
- ↑ Roseveare, W. E. (1930). "The X-Ray Photochemical Reaction between Potassium Oxalate and Mercuric Chloride". J. Am. Chem. Soc. 52 (7): 2612–2619. doi:10.1021/ja01370a005.
- ↑ Sneader, Walter (2005). Drug Discovery: A History. John Wiley and Sons. pp. 45–46. பன்னாட்டுத் தரப்புத்தக எண் 978-0-471-89980-8. பார்க்கப்பட்ட நாள் 2009-02-02.
- ↑ "Commission Directive 86/199/EEC, OJ L 149, p. 38 of 3.6.1986".
- ↑ D. Gonzalez-Ramirez; M. Zuniga-Charles; A. Narro-Juarez; Y. Molina-Recio; K. M. Hurlbut; R. C. Dart; H. V. Aposhian (1 October 1998). "DMPS (2,3-Dimercaptopropane-1-sulfonate, Dimaval) Decreases the Body Burden of Mercury in Humans Exposed to Mercurous Chloride" (free full text). Journal of Pharmacology and Experimental Therapy 287 (1): 8–12. பப்மெட்:9765315. http://jpet.aspetjournals.org/cgi/content/abstract/287/1/8.

