அமோனியா
| |||
| பெயர்கள் | |||
|---|---|---|---|
| ஐயூபிஏசி பெயர்s
அசேன்
Azane | |||
| வேறு பெயர்கள் | |||
| இனங்காட்டிகள் | |||
| 7664-41-7 | |||
InChI
| |||
| யேமல் -3D படிமங்கள் | Image | ||
| பப்கெம் | 222 | ||
| வே.ந.வி.ப எண் | BO0875000 | ||
| |||
| பண்புகள் | |||
| NH3 | |||
| வாய்ப்பாட்டு எடை | 17.0306 g/mol | ||
| தோற்றம் | நிறமற்ற, கடும் நெடி வீசும் வளிமம் | ||
| அடர்த்தி | 0.6942 [2] | ||
| உருகுநிலை | -77.73 °C (195.42 K) | ||
| கொதிநிலை | -33.34 °C (239.81 K) | ||
| 89.9 g/100 ml at 0 °C | |||
| காடித்தன்மை எண் (pKa) | 9.25 | ||
| காரத்தன்மை எண் (pKb) | 4.75 | ||
| ஒளிவிலகல் சுட்டெண் (nD) | εr | ||
| கட்டமைப்பு | |||
| மூலக்கூறு வடிவம் | |||
| இருமுனைத் திருப்புமை (Dipole moment) | 1.42 D | ||
| தீங்குகள் | |||
| முதன்மையான தீநிகழ்தகவுகள் | தீநேர்வு தரவல்ல வளிமம், காரத்தன்மையான, அரிக்கவல்ல பொருள் | ||
| R-சொற்றொடர்கள் | R10, R23, R34, R50 (S1/2), S16, S36/37/39, S45, S61 | ||
| தீப்பற்றும் வெப்பநிலை | None[3] | ||
| தொடர்புடைய சேர்மங்கள் | |||
| ஏனைய எதிர் மின்னயனிகள் | ஹைட்ராக்ஸைடு (NH4OH) | ||
| ஏனைய நேர் மின்அயனிகள் | அமோனியம் (NH4+) | ||
தொடர்புடையவை |
குளோரைடு (NH4Cl) | ||
| தொடர்புடைய சேர்மங்கள் | ஹைட்ராசைன் ஹைட்ராசாயிக் காடி ஹைட்ரோசைலமைன் குளோரோமைன் | ||
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |||
நவச்சாரியம், நவச்சாரகம் அல்லது அமோனியா (Ammonia) என்பது ஒரு நைதரசன் அணுவுடன் மூன்று ஐதரசன் அணுக்கள் இணைந்திருக்கும் ஒரு சேர்மமாகும். இதன் மூலக்கூறு வாய்பாடு NH3. அறை வெப்ப அழுத்தநிலைகளில், அமோனியா ஒரு வளிமமாகும். நச்சுத்தன்மையும் அரிப்புத்தன்மையும் கொண்ட இவ்வளிமம் ஒருவகை கடும் நாற்றம் (நெடி) கொண்டது. அமோனியா காற்றைவிட இலேசானது.
அமோனியா 100 ஆண்டுகளுக்கும் மேலாக உலகில் உற்பத்தி செய்து பயன்படுத்தப்பட்டு வரும் ஒரு வேதிப்பொருள். உலகின் மொத்த உற்பத்தியில் எடையளவில் (டன்னளவில்) இரண்டாவதாக உள்ள வேதிப்பொருள்[4]. உற்பத்தி செய்யும் வேதிப்பொருட்களில் மொத்த மதிப்பில் (பணம்), முதல் இடம் வகிக்கின்றது[4]. 1980களின் துவக்கத்தில் ஆண்டொன்றுக்கு 100 மில்லியன் மெட்ரிக் டன்னுக்கும் அதிகமாக உறபத்தி செய்யப்பட்டது. அமோனியா பயிர்களுக்கு இடும் உர உற்பத்தியில் பயனாகும் ஒரு பொருள். பல்வேறு வகையான மருந்துப்பொருட்கள் உற்பத்தியிலும் அமோனியா பயன்படுகின்றது.
பெயர் வரலாறு
[தொகு]அமோனியா என்ற பெயர் இன்றைய லிபியா நாட்டில் அம்மானில் (Ammon) முன்பு இருந்த வியாழனுக்கான கோயிலில் (Temple of Jupiter Ammon), ஒட்டகத்தின் சாணத்தில் இருந்து பிரித்தெடுக்கப்பட்ட பொருளாக இருந்ததால், அம்மோனியம் என்னும் பெயர் பெற்றது[5] ஆனால், அமோனியாவில் இருந்து பெற்ற உப்புகளை ஹார்மோனிக்கஸ் சால் (சால் = உப்பு) Hammoniacus sal[6] என்று ரோமானிய எழுத்தாளர் பிளினி (கி.பி. 23-79) குறிப்பிட்டிருந்ததாகவும் கூறப்படுகின்றது. இதுதான் பிற்காலத்தில் அறியப்பட்ட சால்-அம்மொனியாக் (sal-ammoniac.)[6] என்பதா, இதிலிருந்து அமோனியா என்னும் பெயர் ஏற்பட்டதா என்பது உறுதிப்படுத்த முடியவில்லை.
அமோனியாவின் உட்கூறுகளை முதன் முதலாகக் 1777ல் கண்டுபிடித்தவர் கிளாடெ லூயி பெர்ட்டோலே (Claude Louis Berthollet)[5] என்பார். ஆனால் இவ் வளிமத்தை 1774 ஆம் ஆண்டு முதன் முதலாக தனியான ஒரு வளிமமாகக் கண்டுணர்ந்தவர் ஆங்கிலேய வேதியியலாளர் ஜோசப் பிரீஸ்ட்லி (Joseph Priestley). ஜோசப் பிரீஸ்ட்லி இதனைக் "காரக காற்று" (ஆல்க்கலைன் காற்று, alkaline air) என்று பெயர் சூட்டினார்.
குறிப்பிடத்தக்க பண்புகள்
[தொகு]தொழிலகங்களில் பயன்படும் அம்மோயாவை நீரற்ற அமோனியா என்று கூறுவர். ஏனெனில் அதில் நீர் சேராமல் இருக்கும். அமோனியா -33 °C வெப்பநிலையிலேயே கொதிக்கத் தொடங்குவதால், அதனை அதிக அழுத்தத்தில் கீழ் வெப்பநிலையில் வைத்திருப்பர். திண்ம நிலையில் இருந்து உருகும் வெப்பநிலை -77.7 °C. அமோனியா நீரில் நன்றாகக் கரையும். நீரில் எடையளவில் 45% கரையவல்லது. முழுக்கரைசைலாக உள்ளபொழுது இது அமோனியம் ஹைட்ராக்ஸைடு (NH4OH) என்று அழைக்கபடும். இது ஒரு காரப்பொருள் (ஆல்க்கலைன்). அமோனியா எரியும் பொழுது பச்சையும் மஞ்சளும் கலந்த நிறத் தீக்கொழுந்தாக எரிகின்றது.
அமோனியாவின் ஈரியல்பு
[தொகு]அமோனியா ஒரு வலுக்குறைந்த காரமாகும். அமோனியா ஏனைய காரங்களைப் போல அமிலங்களுடன் தாக்கமடைந்து உப்பைத் தோற்றுவிக்கும் இயல்புடையது. உதாரணமாக அமோனியா ஐதரோ குளோரிக் அமிலத்துடன் தாக்கமடைந்து அமோனியம் குளோரைட்டை உருவாக்கும். எனினும் முழுமையாக நீரற்ற சூழ்நிலையில் இத்தாக்கம் நடைபெறாது. அருகருகே அமோனியா மற்றும் ஐதரோ குளோரிக் அமில போத்தல்களை வைத்தால் இரண்டுக்கும் இடையே வெள்ளை நிற மூடுபனி போன்ற தோற்றத்தோடு அமோனியம் குளோரைட்டு உருவாகும்.

- NH3 + HCl → NH4Cl
அமோனியா அமிலங்களுடன் தாக்கமடைந்து உருவாக்கும் உப்புக்கள் அனைத்தும் அமோனியம் உப்புக்கள் என அழைக்கப்படுவதுடன் இவை அமோனியம் அயனைக் (NH4+) கொண்டிருக்கும்.
அமோனியா ஒரு மிகவும் வலுக்குறைந்த அமிலமாகவும் தொழிற்படக்கூடியது. சில உலோகங்களுடன் தாக்கமடைந்து அமைட்டுகளை உருவாக்கல் அமோனியாவின் அமில இயல்பை உறுதிப்படுத்துகின்றது. உதாரணமாக சோடியத்துடன் தாக்கமடைந்து சோடியம் அமைட்டை உருவாக்கும்.
- 2 Na + 2 NH3 → 2 NaNH2 + H2
இவ்வாறு காரமாகவும் அமிலமாகவும் தொழிற்பட்டு அமோனியா ஈரியல்பைக் காட்டும் வாயுவாகத் திகழ்கின்றது.
பிரிகையடைதல்
[தொகு]நீரைப்போல அமோனியாவும் கற்றயனாகவும், அனயனாகவும் பிரிகையடையும் இயல்புடையது.
- 2 NH
3 (aq) NH+
NH+
4 (aq) + NH−
2 (aq)
அமோனியா எரிதல்
[தொகு]அமோனியா ஒக்சிசனில் எரிந்து நைதரசனையும், நீரையும் தோற்றுவிக்கும். இது புறவெப்பத்தாக்கமாகும்.
- 4 NH3 + 3 O2 → 2 N2 + 6 H2O (g)
எனினும் தகுந்த ஊக்கிகள் காணப்பட்டால் இயக்கவியல் விளைவுகளாக நைதரசனின் ஒக்சைட்டுகள் தோன்றும். இத்தோற்றப்பாடே நைட்ரிக் அமில உற்பத்தியில் முக்கிய பங்கு வகிக்கின்றது.
- 4 NH3 + 5 O2 → 4 NO + 6 H2O
- 2 NO + O2 → 2 NO2
இவ்வாறு தோன்றும் நைத்ரிக் ஒக்சைட்டை நைத்ரிக் அமிலம் உற்பத்தி செய்வதற்காகப் பயன்படுத்துகின்றனர். எனினும் அமோனியா எரியும் போது சிறிதளவு வெப்பமே வெளிப்படுவதால் இத்தாக்கத்தை ஊக்கிகளின்றித் தொடர்தல் கடினமாகும்.
இயற்பியல் பண்புகள்
[தொகு]அமோனியா ஒரு நிறமற்ற வாயு ஆகும். காரச்சுவை இதை அடையாளப்படுத்துகிறது. காற்றை விட இது இலேசானது ஆகும். காற்றின் அடர்த்தியைக் காட்டிலும் அமோனியாவின் அடர்த்தி 0.589 முறை அதிகமாகும். மூலக்கூறுகளுக்கு இடையில் வலிமையான ஐதரசன் பிணைப்பு இருப்பதன் காரணமாக இதை எளிதில் திரவமாக்க முடியும். −33.3 °செல்சியசு வெப்பநிலையில் இது கொதிக்கிறது. −77.7 ° செல்சியசு வெப்பநிலையில் இது வெண் படிகங்களாக உறைகிறது. ஒரு வளிமண்டல அழுத்தம் அல்லது தாழ் வெப்ப நிலையில் −33.34 °செல்சியசு வெப்பநிலையில் அமோனியா கொதிக்கிறது. எனவே இதை அழுத்தத்தின் கீழ் சேமிக்க வேண்டும்.
தொகுப்பும் உற்பத்தியும்
[தொகு]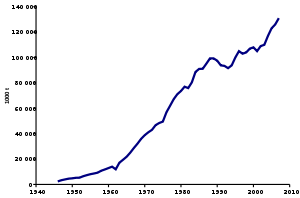
அமோனியா அதிக பயன்பாடுகளைக் கொண்டுள்ளது. எனவே மிக அதிகமாக உற்பத்தி செய்யப்படும் கனிம வேதியியல் சேர்மங்களில் இதுவும் ஒன்றாகும். உலகெங்கிலும் பல தொழிற்சாலைகள் அமோனியாவை உற்பத்தி செய்கின்றன. மனிதனால் உருவாக்கப்பட்ட அனைத்து சக்திகளிலும் 1% க்கும் மேலான நுகர்வும், உலக ஆற்றல் வரவுசெலவு திட்டத்தில் குறிப்பிடத்தக்க ஒதுக்கீடும் அம்மோனியா உற்பத்திக்காக என்பது குறிப்பிடத்தக்கது ஆகும்..2014 ஆம் ஆண்டு உலகாய அளவில் உற்பத்தி செய்யப்பட்ட அமோனியாவின் அளவு 176 மில்லியன் டன்கள் ஆகும். இதில் 32.6 சதவீதம் அமோனியா சீனாவில் உற்பத்தி செய்யப்பட்டுள்ளது. உருசியா 8.1 சதவீதம், இந்தியா 7.6% அமோனியாவையும் அமெரிக்கா 6.4% அமோனியாவையும் உற்பத்தி செய்துள்ளன. 88% அமோனியா உற்பத்தியானது விவசாய விதைகளுக்கு உரமாகவே பயன்படுத்தப்பட்டுள்ளது. 2012 ஆம் ஆண்டின் உலகாய அமோனியா உற்பத்தி இயற்கை வாயுவில் இருந்தே தயாரிக்கப்படுள்ளது. இது கிட்டத்தட்ட 72% ஆகும். முதலாம் உலகப் போர் துவங்குவதற்கு முன்னர், பேரளவு அமோனியா உலர் வடித்தல் மூலமே தயாரிக்கப்பட்டுள்ளது. இதற்காக நைட்ரசன் மிகுந்த காய்கறிகள், ஒட்டக சாணி உள்ளிட்ட விலங்குகளின் கழிவு பொருட்கள் இதற்காகப் பயன்படுத்தப்பட்டன. இவை நைட்ரசு அமிலத்தின் ஒடுக்கம் மூலமும் நைட்ரைட்டுகளுடன் ஐதரசன் சேர்க்கப்பட்டும் வடிக்கப்பட்டன. நைட்ரஜன் அமிலம் மற்றும் நைட்ரைட்டுகள் ஹைட்ரஜன் கொண்ட நைட்ரஜன் அமிலம் மற்றும் நைட்ரெயினைக் குறைப்பதன் மூலம் வடிகட்டப்பட்ட நைட்ரஜன் காய்கறி மற்றும் விலங்கு கழிவுப்பொருட்களின் உலர் வடித்தல், [93] அதிக அம்மோனியா பெறப்பட்டது; கூடுதலாக, இது நிலக்கரி வடிகட்டல் மூலமாக தயாரிக்கப்பட்டது, மேலும் ஆல்குலின் ஹைட்ராக்ஸைடுகளின் [94] ஆல்மோனியம் உப்புக்களின் சிதைவு காரணமாக இது சுழற்சியை போன்றது, உப்பு பொதுவாக பொதுவாக குளோரைடு (சால் அம்மோனியா) என்று பயன்படுத்தப்படுகிறது:
கூடுதலாக நிலக்கரியை வடித்தல் மூலமும், ஆல்கலின் ஐதராக்சைடுகளால் அமோனியா உப்புகளை சிதைவடையச் செய்தும் அமோனியா தயாரிக்கப்பட்டது. கால்சியம் ஆக்சைடு உப்பு பொதுவாக இதற்காகப் பயன்படுத்தப்படுகிறது. அம்மோனியா தொகுப்புக்கு தேவையான ஐதரசன் , நீர் வாயுவைப் பயன்படுத்தியும் பொருளாதார ரீதியாக உற்பத்தி செய்யப்படலாம். நிர்வாயு வினையைத் தொடர்ந்து நீர்வாயு மாற்ற வினை இதற்காக பயன்படுத்தப்படுகிறது. நீராவியை செஞ்சூடான் கல்கரின் வழியாகச் செலுத்தி ஐதரசன் மற்றும் கார்பன் டை ஆக்சைடு வாயுக்களின் கலவை பெறப்படுகிறது. பின்னர் கார்பன் டை ஆக்சைடு நீக்கப்படுகிறது. 2500 கிலோபாசுக்கல் வளி மண்டல அழுத்தத்தில் இக்க்லவையை நீரால் கழுவினால் கார்பன் டை ஆக்சைடு நீக்கப்படுகிறது. அல்லது நிலக்கரி அல்லது நிலக்கரி வாயுவை போன்ற பிற ஆதாரங்களைப் பயன்படுத்துவதன் மூலமும் கார்பன் டை ஆக்சைடைப் பிரிக்கலாம். . நவீன அம்மோனியா உற்பத்தி செய்யும் தொழிற்சாலைகள் ஐதரசன் உற்பத்தியைச் சார்ந்தே இருக்கின்றன. தொழிற்சாலைகளில் இருந்து கிடைக்கும் ஐதரசனே மேக்னடைட்டு வினையூக்கியைப் பயன்படுத்தி அல்லது அழுத்தத்திற்கு உட்படுத்தப்பட்ட இரும்பு வினையூக்கியைப் பயன்படுத்தி வளிமண்டல நைட்ரசனுடன் வினைபுரிகின்றன. 10000 கிலோபாசுக்கல் வளிமண்டல அழுத்தமும் 450 பாகை செல்சியசு வெப்பநிலையும் இங்கு பயன்படுகின்றன. நீரற்ற திரவ அமோனியா உருவாகிறது. இச்செயல் முறை ஏபர்-போசு செயல்முறை என்று அழைக்கப்படுகிறது.
- 3 H2 + N2 → 2 NH3(g)
அம்மோனியா தொகுப்புக்காகத் தேவைப்படும் ஐதரசனை பிற ஆதார மூலங்களான நிலக்கரி அல்லது கல்கரி போன்றவற்றை வணிகமுறை வளிமயமாக்கல் அல்லது நீரை நீராற்பகுக்கும் செலவின முறை மூலமும் தயாரிக்கலாம். ஐரோப்பாவின் அம்மோனியா உற்பத்தி பெரும்பாலும் மின்னாற்பகுப்பு வழியாக வெமொர்க்கில் தயாரிக்கப்பட்டது. புதுப்பிக்கத் தக்க ஆற்றல் மூலங்களைப் பயன்படுத்தியும் மின் உற்பத்தியை சரிசெய்து கொள்ளலாம்.
பயன்பாடுகள்
[தொகு]இரசாயன உரம்
[தொகு]உலகில் உற்பத்தி செய்யப்படும் 83% நவச்சாரியம் உரமாகவே பயன்படுத்தப்படுகின்றது. இது யூரியா அல்லது அமோனியாவின் உப்புக்களாக மாற்றப்பட்டு பயன்படுத்தப்படுகின்றது. உலகளவில் ஒவ்வொரு வருடமும் 110 மில்லியன் தொன் அமோனியா உரமாகப் பயன்படுகின்றது.
நைதரசன் சேர்மங்களுக்கு முன்னோடியாகப் பயன்படல்
[தொகு]அனைத்து வகையான நைதரசன் சேர்மங்களுக்கும் நேரடியாகவோ மறைமுகமாகவோ அமோனியாவிலிருந்தே உற்பத்தி செய்யப்படுகின்றன. அமோனியாவிலிருந்து பெறப்படும் மிக முக்கிய சேர்மம் நைத்ரிக் அமிலமாகும். பிளாட்டினம் ஊக்கிக்கு மேல் 700–850 °C வெப்பநிலையில் கிட்டத்தட்ட 9 மடங்கு வளிமண்டல அமுக்கத்தில் அமோனியாவை ஒக்சியேற்றுவதன் மூலம் நைத்ரிக் அமிலம் பெறப்படுகின்றது. இத்தாக்கத்தின் இடை விளைவாக நைத்ரிக் ஒக்சைட்டு உருவாகி அது பின்னர் நைத்ரிக் அமிலமாக மாற்றப்படுகின்றது.
- NH3 + 2 O2 → HNO3 + H2O
இவ்வாறு உருவாக்கப்படும் நைத்ரிக் அமிலத்திலிருந்து இரசாயன உரங்கள், வெடிமருந்துகள் உட்பட பல்வேறு வகையான நைதரசன் சேர்மங்களை உற்பத்தி செய்துகொள்ள முடியும்.
சுத்தப்படுத்தி
[தொகு]கண்ணாடி, வெண்களி, உருக்காலான பொருட்களை சுத்தப்படுத்தவும் வெதுப்பிகளை சுத்தப்படுத்தவும் 5-10% செறிவுடைய நீரில் கரைக்கப்பட்ட அமோனியா பயன்படுத்தப்படுகின்றது.
நொதித்தல்
[தொகு]அற்கஹோல் உற்பத்தியில் நொதித்தலின் போது pH அளவைக் கட்டுப்படுத்தவும் மதுவத்துக்கு நைதரசன் வழங்கியாகவும் 16% - 25% அமோனியா கரைசல் பயன்படுத்தப்படுகின்றது.
அமோனியாவின் தொழிற்சாலை உற்பத்தி
[தொகு]
இதன் பல்வேறு வகையான பயன்பாடு காரணமாக (முக்கியமாக விவசாயத்தில் உர உற்பத்தியால்) அமோனியா உலகில் அதிகளவு உற்பத்தி செய்யப்படும் அசேதனச் சேர்மங்களில் ஒன்றாகத் திகழ்கின்றது. மனிதன் பயன்படுத்தும் செயற்கை ஆற்றலில் 1% அமோனியா உற்பத்திக்குச் செலவாதல் இதன் உற்பத்தியின் முக்கியத்துவத்தைக் காட்டுகின்றது. 2012ஆம் ஆண்டில் 198 மில்லியன் தொன்கள் உற்பத்தி செய்யப்பட்டதுடன் 2019ஆம் ஆண்டளவில் இன்னும் 35 மில்லியன் தொன்களால் இது அதிகரிக்கலாம் என எதிர்பார்க்கப்படுகின்றது. சீனாவில் 28.6% மும், இந்தியாவில் 8.6% மும் உற்பத்தி செய்யப்படுவதுடன் இவ்வுற்பத்தியில் 80% இரசாயன உரத்துக்காகப் பயன்படுத்தப்படுகின்றது.
தற்காலத்தில் ஹேபர் பொஸ்ச் முறை என்ற முறையே அமோனியா உற்பத்திக்குப் பயன்படுத்தப்படுகின்றது. மக்னறைட் அல்லது இரும்பு ஊக்கியின் மேல் அல்லது 10,000 kPa அமுக்கத்தில் 450 °C வெப்பநிலையில் ஐதரசன் வாயுவையும் நைதரசன் வாயுவையும் தாக்கமடையச் செய்வதால் அமோனியா உற்பத்தி நடைபெறுகின்றது.
- 3 H2 + N2 → 2 NH3
மேற்கோள்கள்
[தொகு]- ↑ Ammonia data at NIST Webbook, last accessed May 7 2007.
- ↑ NIST Chemistry WebBook (website page of the National Institute of Standards and Technology) URL last accessed May 15 2007
- ↑ MSDS Sheet from W.D. Service Co.
- ↑ 4.0 4.1 Van Nostrand's Scientific Encyclopedia, 9th Ed., (Ed.)Glenn D. Considine, Wiley-Intersceince, 2002.
- ↑ 5.0 5.1 Van Nostrand's Sceintific Encyclopedia, 9th Ed., (Ed.)Glenn D. Considine, Wiley-Intersceince, 2002.
- ↑ 6.0 6.1 Webmineral website URL last accessed August 27 2006



