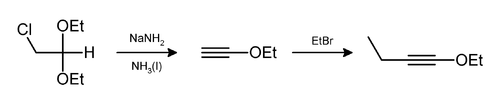சோடியம் அமைடு

| |
| |
| பெயர்கள் | |
|---|---|
| ஐயூபிஏசி பெயர்
சோடியம் அமைடு, சோடியம் அசனைடு[1]
| |
| வேறு பெயர்கள்
சோடாமைடு
| |
| இனங்காட்டிகள் | |
| 7782-92-5 | |
| ChemSpider | 22940 |
| EC number | 231-971-0 |
InChI
| |
| யேமல் -3D படிமங்கள் | Image |
| பப்கெம் | 24533 |
SMILES
| |
| UN number | 1390 |
| பண்புகள் | |
| NaNH2 | |
| வாய்ப்பாட்டு எடை | 39.01 கி மோல்−1 |
| தோற்றம் | நிறமற்ற படிகங்கள் |
| மணம் | அம்மோனியாவைப் போன்ற மணம் |
| அடர்த்தி | 1.39 கி செமீ−3 |
| உருகுநிலை | 210 °C (410 °F; 483 K) |
| கொதிநிலை | 400 °C (752 °F; 673 K) |
| வினைபுரிகிறது. | |
| கரைதிறன் | 0.004 கி/100 மிலி (திரவ அம்மோனியா), எத்தனால்இல் வினைபுரிகிறது. |
| காடித்தன்மை எண் (pKa) | 38 (இணை அமிலம்) [2] |
| கட்டமைப்பு | |
| படிக அமைப்பு | செங்கோண வட்டம் |
| வெப்பவேதியியல் | |
| Std enthalpy of formation ΔfH |
-118.8 கிலோ யூல்/மோல் |
| நியம மோலார் எந்திரோப்பி S |
76.9 யூல்/மோல் கெல்வின் |
| வெப்பக் கொண்மை, C | 66.15 யூல்/மோல் கெல்வின் |
| தீங்குகள் | |
| தீப்பற்றும் வெப்பநிலை | 4.44 °C (39.99 °F; 277.59 K) |
Autoignition
temperature |
450 °C (842 °F; 723 K) |
| தொடர்புடைய சேர்மங்கள் | |
| ஏனைய எதிர் மின்னயனிகள் | சோடியம் பிஸ்(டிரைமெதில்சிலைல்)அமைடு |
| ஏனைய நேர் மின்அயனிகள் | பொட்டாசியம் அமைடு |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
| | |
| Infobox references | |
சோடியம் அமைடு (Sodium amide) சோடா அமைடு எனப்படக் கூடிய NaNH2 என்ற மூலக்கூற்று வாய்ப்பாட்டை உடைய கனிமச் சேர்மம் ஆகும். இது நீருடன் மிக வேகமாக வினைபுரியக் கூடியது. வெண்மை நிறமுடையது. வணிகரீதியாகக் கிடைக்கக்கூடிய மாதிரிகள் அவற்றின் தயாரிப்பின் போது காணப்படும் உலோக இரும்பின் காரணமாக சிறிது சாம்பல் நிறமுடன் காணப்படலாம். இத்தகைய மாசுகள் வழக்கமாக வினைக்காரணியின் பயன்பாட்டைக் குறைப்பதில்லை.[சான்று தேவை] NaNH2 ஆனது உருகிய நிலையில் மின்சாரத்தைக் கடத்துகிறது. இதன் கடத்துதிறனானது ஒரே மாதிரியான நிலைகளில் சோடியம் ஐதராக்சைடுடன் ஒத்ததாக காணப்படுகிறது. NaNH2 ஆனது கரிமத் தொகுப்பு முறைகளில் பரவலாகப் பயன்படும் ஒரு வேதிப்பொருளாக உள்ளது.
தயாரிப்பு மற்றும் அமைப்பு[தொகு]
சோடியத்துடன் அம்மோனியா வாயுவின் வினையின் காரணமாக சோடியம் அமைடானது தயாரிக்கப்படலாம்.[3] ஆனால், வழக்கமாக திரவ அம்மோனியாவுடன் சோடியத்தை இரும்பு (III) நைட்ரேட்டை ஒரு வினைவேகமாற்றியாகப் பயன்படுத்தி தயாரிக்கப்படுகிறது. இந்த வினையானது அம்மோனியாவின் கொதிநிலையில் மிக வேகமாக நடைபெறுகிறது c. −33 °C. இந்த வினையில், [Na(NH3)6]+e− என்ற எலக்ட்ரைடு வினையிடைப் பொருளாக உருவாகிறது. [4]
- 2 Na + 2 NH3 → 2 NaNH2 + H2
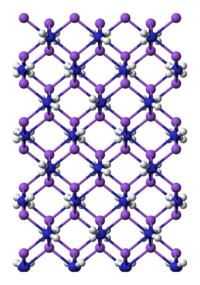
NaNH2 ஆனது உப்பைப் போன்ற ஒரு பொருளாகும். இது ஒரு முடிவிலாப் பலபடிடைப் போல படிகமாகறிது.[5] சோடியத்தைப் பொறுத்து இதன் வடிவியல் அமைப்பானது நான்முகியின் அமைப்பைப் பெறுகிறது.[6] அம்மோனியாவில், NaNH2 மின்கடத்துத்திறனைப் பெற்ற, கரைசல் முழுவதிலும் ஒரே சீரான, இசைவான Na(NH3)6+ மற்றும் NH2− அயனிகளைக் கொண்ட கரைசல்களை உருவாக்குகின்றன.
பயன்கள்[தொகு]
சோடியம் அமைடானது முக்கியமாக கரிம வேதியியலில் அம்மோனியாக் கரைசல்களில் கூட, மிகவும் வலிமையான காரமாகப் பயன்படுகின்றன. [சான்று தேவை]. சோடாமைடினைப் பயன்படுத்துவதில் உள்ள சிறப்பம்சங்களில் ஒன்று இச்சேர்மம் மிக அரிதாகவே கருக்கவர் காரணியாக செயல்படுகிறது. இண்டிகோ சாயம் தயாரிப்பில் N-பினைல்கிளைசீனின் வளையமாக்களில் பயன்படும் மீத்திறன் காரக்கலவையில் ஒரு முக்கியப் பகுதிப்பொருளாகப் பயன்படுகிறது. இந்த வினையானது அம்மோனியாவை உற்பத்தி செய்து அதனை ஒருவிதமாக மறுசுழற்சி செய்யப்பயன்படுகிறது.[7]

ஐதரோஆலசன் நீக்க வினை[தொகு]
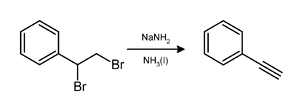
சோடியம் அமைடு அருகருகாய் அமைந்துள்ள டைபுரோமோ அல்கேனிலிருந்து இரண்டு சமான அளவுள்ள ஐதரசன் புரோமைடினை இழக்கச்செய்து அல்கைனைத் தரும் வினையைத் துாண்டுகிறது. இந்த வினை பினைல்அசிட்டிலீன் தயாரிப்பில் நிகழ்வது போன்ற வினையாக உள்ளது. [8] வழக்கமாக, இரண்டு சமான அளவுள்ள சோடியம் அமைடானது தேவையான அல்கைனைத் தருகிறது. விளைபொருளில் காணப்படும் முனையங்களில் உள்ள CH ஆனது சமான அளவுள்ள காரத்தை புரோட்டானேற்றம் செய்யும் காரணத்தால் மூன்று சமான அளவுள்ள சோடியம் அமைடுகள் முனையங்களில் முப்பிணைப்பைக் கொண்ட அல்கைன்களை உருவாக்குவதற்குத் தேவைப்படுகிறது.
ஐதரசன் குளோரைடு மற்றும் எத்தனால் ஆகியவை ஈடுபட்டு 1-ஈத்தாக்சி-1-பியூட்டைன் தயாரிக்கப் பயன்படும் வினையிலும் இதே போன்ற நீக்க வினைகள் நடத்தப்படலாம்.[9][10]
வளையமாக்கல் வினைகள்[தொகு]
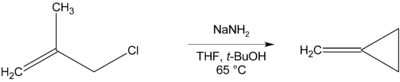
மெதில்வளையபுரோப்பேன் தயாரிப்பில் காணப்படுவது போல, நீக்கப்படுவதற்கான β-ஐதரசனைக் கொண்டிராத சேர்மங்களில் வளைய சேர்மங்கள் உருவாக்கப்படலாம்.[11]
வளையபுரோப்பேன்கள்,[12] அசிரிடின்கள்[13] மற்றும் வளையபியூட்டேன்கள்[14] ஆகியவை இதே முறையில் தயாரிக்கப்படலாம்.
கார்பன் மற்றும் நைட்ரசன் அமிலங்களில் புரோட்டான் நீக்கம்[தொகு]
முனைய அல்கைன்களை உள்ளடக்கிய கார்பன் அமிலங்கள் திரவ அம்மோனியாவில் உள்ள சோடியம் அமைடுகளால் புரோட்டான் நீக்கம் செய்யப்படுகின்றன. [15] மெதில் கீட்டோன்கள்,[16] வளையஎக்சனோன்,[17] பினைல்அசிட்டிக் அமிலம் மற்றும் அதன் வழிப்பொருட்கள்[18] மற்றும் டைபினைல்மீத்தேன்[19] அசிட்டைல்அசிட்டோன் இரண்டு புரோட்டான்களை இழந்து ஒரு இரட்டைஎதிரயனியைத் தருகிறது.[20] சோடியம் அமைடானது இண்டோல் [21] மற்றும் பிப்பெரிடின் ஆகியவற்றையும் கூட புரோட்டான் நீக்கம் செய்கிறது.[22]
பாதுகாப்பு[தொகு]
சோடியம் அமைடு நீருடன் அதிதீவிரமாக வினைபுரிந்து அம்மோனியா மற்றும் சோடியம் ஐதராக்சைடு ஆகியவற்றைத் தருவதுடன் காற்றில் எரிந்து சோடியத்தின் ஆக்சைடுகளையும், நைட்ரசனின் ஆக்சைடுகளையும் தருகின்றது.
- NaNH2 + H2O → NH3 + NaOH
- 4 NaNH2 + 7 O2 → 2 Na2O + 4 NO2 + 4 H2O
குறைவான ஈரப்பதம் மற்றும் காற்றின் முன்னிலையில், அதாவது மோசமாக மூடப்பட்ட கொள்கலன்கறில், பெராக்சைடுகளைக் கொண்ட வெடிபொருட்கலவைகள் உருவாகக்கூடும். இவ்வாறான நிகழ்வு திண்மத்தை மஞ்சள் நிறமாகவோ, பழுப்பு நிறமாகவோ மாற்றக்கூடும். இதன் காரணமாகவே, சோடியம் அமைடானது, மந்த வாயுக்களின் சூழலில், நன்றாக, இறுக மூடப்பட்ட கொள்கலன்களில் பாதுகாக்கப்பட வேண்டியுள்ளது. மஞ்சள் அல்லது பழுப்பு நிறமுள்ள சோடியம் அமைடு மாதிரிகள் வெடிக்கும் அபாயம் நிறைந்தவையாகும்.[23]
மேலும் காண்க[தொகு]
மேற்கோள்கள்[தொகு]
- ↑ http://goldbook.iupac.org/A00266.html
- ↑ Buncel, E.; Menon, B. (1977). "Carbanion mechanisms: VII. Metallation of hydrocarbon acids by potassium amide and potassium methylamide in tetrahydrofuran and the relative hydride acidities". Journal of Organometallic Chemistry 141 (1): 1–7. doi:10.1016/S0022-328X(00)90661-2.
- ↑ Bergstrom, F. W. (1955). "Sodium amide". Organic Syntheses. http://www.orgsyn.org/demo.aspx?prep=cv3p0778.; Collective Volume, vol. 3, p. 778
- ↑ Greenlee, K. W.; Henne, A. L.; Fernelius, W. C. (1946). "Sodium Amide". Inorganic Syntheses 2: 128–135. doi:10.1002/9780470132333.ch38.
- ↑ Zalkin, A.; Templeton, D. H. (1956). "The Crystal Structure Of Sodium Amide". Journal of Physical Chemistry 60 (6): 821–823. doi:10.1021/j150540a042.
- ↑ Wells, A. F. (1984). Structural Inorganic Chemistry. Oxford: Clarendon Press. பன்னாட்டுத் தரப்புத்தக எண்:0-19-855370-6. https://archive.org/details/structuralinorga0000well_m8i1.
- ↑ L. Lange, W. Treibel "Sodium Amide" in Ullmann's Encyclopedia of Industrial Chemistry 2005, Wiley-VCH, Weinheim. எஆசு:10.1002/14356007.a24_267
- ↑ Campbell, K. N.; Campbell, B. K. (1950). "Phenylacetylene". Organic Syntheses 30: 72. http://www.orgsyn.org/demo.aspx?prep=cv4p0763.; Collective Volume, vol. 4, p. 763
- ↑ Jones, E. R. H.; Eglinton, G.; Whiting, M. C.; Shaw, B. L. (1954). "Ethoxyacetylene". Organic Syntheses 34: 46. http://www.orgsyn.org/demo.aspx?prep=cv4p0404.; Collective Volume, vol. 4, p. 404
Bou, A.; Pericàs, M. A.; Riera, A.; Serratosa, F. (1987). "Dialkoxyacetylenes: di-tert-butoxyethyne, a valuable synthetic intermediate". Organic Syntheses 65: 58. http://www.orgsyn.org/demo.aspx?prep=cv8p0161.; Collective Volume, vol. 8, p. 161
Magriotis, P. A.; Brown, J. T. (1995). "Phenylthioacetylene". Organic Syntheses 72: 252. http://www.orgsyn.org/demo.aspx?prep=cv9p0656.; Collective Volume, vol. 9, p. 656
Ashworth, P. J.; Mansfield, G. H.; Whiting, M. C. (1955). "2-Butyn-1-ol". Organic Syntheses 35: 20. http://www.orgsyn.org/demo.aspx?prep=cv4p0128.; Collective Volume, vol. 4, p. 128 - ↑ Newman, M. S.; Stalick, W. M. (1977). "1-Ethoxy-1-butyne". Organic Syntheses 57: 65. http://www.orgsyn.org/demo.aspx?prep=cv6p0564.; Collective Volume, vol. 6, p. 564
- ↑ Salaun, J. R.; Champion, J.; Conia, J. M. (1977). "Cyclobutanone from methylenecyclopropane via oxaspiropentane". Organic Syntheses 57: 36. http://www.orgsyn.org/demo.aspx?prep=cv6p0320.; Collective Volume, vol. 6, p. 320
- ↑ Nakamura, M.; Wang, X. Q.; Isaka, M.; Yamago, S.; Nakamura, E. (2003). "Synthesis and (3+2)-cycloaddition of a 2,2-dialkoxy-1-methylenecyclopropane: 6,6-dimethyl-1-methylene-4,8-dioxaspiro(2.5)octane and cis-5-(5,5-dimethyl-1,3-dioxan-2-ylidene)hexahydro-1(2H)-pentalen-2-one". Organic Syntheses 80: 144. http://www.orgsyn.org/demo.aspx?prep=v80p0144.
- ↑ Bottini, A. T.; Olsen, R. E. (1964). "N-Ethylallenimine". Organic Syntheses 44: 53. http://www.orgsyn.org/demo.aspx?prep=cv5p0541.; Collective Volume, vol. 5, p. 541
- ↑ Skorcz, J. A.; Kaminski, F. E. (1968). "1-Cyanobenzocyclobutene". Organic Syntheses 48: 55. http://www.orgsyn.org/demo.aspx?prep=cv5p0263.; Collective Volume, vol. 5, p. 263
- ↑ Saunders, J. H. (1949). "1-Ethynylcyclohexanol". Organic Syntheses 29: 47. http://www.orgsyn.org/demo.aspx?prep=cv3p0416.; Collective Volume, vol. 3, p. 416
Peterson, P. E.; Dunham, M. (1977). "(Z)-4-Chloro-4-hexenyl trifluoroacetate". Organic Syntheses 57: 26. http://www.orgsyn.org/demo.aspx?prep=cv6p0273.; Collective Volume, vol. 6, p. 273
Kauer, J. C.; Brown, M. (1962). "Tetrolic acid". Organic Syntheses 42: 97. http://www.orgsyn.org/demo.aspx?prep=cv5p1043.; Collective Volume, vol. 5, p. 1043 - ↑ Coffman, D. D. (1940). "Dimethylethynylcarbinol". Organic Syntheses 20: 40. http://www.orgsyn.org/demo.aspx?prep=cv3p0320.; Collective Volume, vol. 3, p. 320Hauser, C. R.; Adams, J. T.; Levine, R. (1948). "Diisovalerylmethane". Organic Syntheses 28: 44. http://www.orgsyn.org/demo.aspx?prep=cv3p0291.; Collective Volume, vol. 3, p. 291
- ↑ Vanderwerf, C. A.; Lemmerman, L. V. (1948). "2-Allylcyclohexanone". Organic Syntheses 28: 8. http://www.orgsyn.org/demo.aspx?prep=cv3p0044.; Collective Volume, vol. 3, p. 44
- ↑ Hauser, C. R.; Dunnavant, W. R. (1960). "α,β-Diphenylpropionic acid". Organic Syntheses 40: 38. http://www.orgsyn.org/demo.aspx?prep=cv5p0526.; Collective Volume, vol. 5, p. 526
Kaiser, E. M.; Kenyon, W. G.; Hauser, C. R. (1967). "Ethyl 2,4-diphenylbutanoate". Organic Syntheses 47: 72. http://www.orgsyn.org/demo.aspx?prep=cv5p0559.; Collective Volume, vol. 5, p. 559
Wawzonek, S.; Smolin, E. M. (1951). "α,β-Diphenylcinnamonitrile". Organic Syntheses 31: 52. http://www.orgsyn.org/demo.aspx?prep=cv4p0387.; Collective Volume, vol. 4, p. 387 - ↑ Murphy, W. S.; Hamrick, P. J.; Hauser, C. R. (1968). "1,1-Diphenylpentane". Organic Syntheses 48: 80. http://www.orgsyn.org/demo.aspx?prep=cv5p0523.; Collective Volume, vol. 5, p. 523
- ↑ Hampton, K. G.; Harris, T. M.; Hauser, C. R. (1971). "Phenylation of diphenyliodonium chloride: 1-phenyl-2,4-pentanedione". Organic Syntheses 51: 128. http://www.orgsyn.org/demo.aspx?prep=cv6p0928.; Collective Volume, vol. 6, p. 928
Hampton, K. G.; Harris, T. M.; Hauser, C. R. (1967). "2,4-Nonanedione". Organic Syntheses 47: 92. http://www.orgsyn.org/demo.aspx?prep=cv5p0848.; Collective Volume, vol. 5, p. 848 - ↑ Potts, K. T.; Saxton, J. E. (1960). "1-Methylindole". Organic Syntheses 40: 68. http://www.orgsyn.org/demo.aspx?prep=cv5p0769.; Collective Volume, vol. 5, p. 769
- ↑ Bunnett, J. F.; Brotherton, T. K.; Williamson, S. M. (1960). "N-β-Naphthylpiperidine". Organic Syntheses 40: 74. http://www.orgsyn.org/demo.aspx?prep=cv5p0816.; Collective Volume, vol. 5, p. 816
- ↑ "Sodium Amide". Princeton, NJ: Princeton University. 2011-03-16. Archived from the original on 2011-11-04. பார்க்கப்பட்ட நாள் 2011-07-20.