ஆக்சைடு

ஆக்சைடு (oxide) என்பது குறைந்தது ஒர் ஆக்சிசன் அணுவும் மற்றொரு வேதித் தனிமமும் சேர்ந்துள்ள ஒரு சேர்மம் ஆகும்.[1] ஒக்சைடு அல்லது ஒக்சைட்டு என்ற பெயர்களாலும் ஆக்சைடு அழைக்கப்படுகிறது. இதனுடைய மூலக்கூற்று வாய்ப்பாட்டில் ஆக்சைடு என்பது ஆக்சிசனின் O2– இரட்டை எதிர்மின் அயனியாகக் கருதப்படுகிறது. குறிப்பாக உலோக ஆக்சைடுகள் ஆக்சிசனின் எதிர்மின் அயனியை −2. என்ற ஆக்சிசனேற்ற நிலையைக் கொண்டுள்ளன. புவியின் மேலோடு பெரும்பாலும் திண்ம ஆக்சைடுகளால் ஆகியிருக்கிறது. தனிமங்கள் காற்றில் உள்ள ஆக்சிசன் அல்லது நீரில் உள்ள ஆக்சிசனால் ஆக்சிசனேற்றப்படுவதே இதற்கு காரணமாகும். ஐதரோ கார்பன்கள் ஆக்சிசனில் எரிவதால் இரண்டு முக்கியமான ஆக்சைடுகள் தோன்றுகின்றன. அவை கார்பனோராக்சைடு மற்றும் கார்பனீராக்சைடு என்பனவாகும். தனிமங்கள் தூய நிலையில் இருந்தாலும் பெரும்பாலும் அவற்றின் மீது ஆக்சைடு படலங்கள் தோன்றுகின்றன. உதாரணமாக அலுமினியத்தின் மீது அலுமினியம் ஆக்சைடு Al2O3 படலம் உருவாகிறது. இதை வினைமுடக்க அடுக்கு என்கிறார்கள். இது அலுமினியத்தை அரிப்பிலிருந்து தடுக்கிறது[2]. தனித்த நிலையில் சில தனிமங்கள் பல ஆக்சைடுகளை உருவாக்குகின்றன. ஒவ்வொன்றும் வெவ்வேறு அளவுகளில் ஆக்சிசனையும் தனிமத்தையும் கொண்டிருக்கின்றன. சில ஆக்சைடுகளில் இவை கார்பனோராக்சைடு மற்றும் கார்பனீராக்சைடைக் குறிப்பிடுவது போல ஆக்சிசன்களின் எண்ணிக்கையைக் குறிப்பிட்டு அழைப்பது வழக்கமாக இருக்கிறது. மற்றும் சில நிகழ்வுகளில் இரும்பு(II) ஆக்சைடு இரும்பு(III) ஆக்சைடு என்று குறிப்பிடுவது போல தனிமத்தின் ஆக்சிசனேற்ற எண்ணைக் குறிப்பிட்டு அழைக்கவும் செய்கிறார்கள். நைட்ரசன் போன்ற சில தனிமங்கள் பல வகையான ஆக்சைடுகளை உருவாக்குகின்றன.
உருவாக்கம்[தொகு]
எலக்ட்ரான் ஏற்புத்தன்மை காரணமாக ஆக்சிசன், அனைத்து தனிமங்களுடனும் சேர்ந்து அவற்றுடன் தொடர்புடைய ஆக்சைடுகளைத் தருகின்றன. உயர்ந்த தனிமங்களான தங்கம் அல்லது பிளாட்டினம் போன்றவை விலைமதிப்பு மிக்கவையாகும். ஏனெனில் அவை நேரடியாக ஆக்சிசனுடன் வினைபுரிவதை எதிர்க்கின்றன. தங்கம் (III) ஆக்சைடு போன்ற ஆக்சைடுகள் வேறு வகையான பாதைகளில் தயாரிக்கப்படுகின்றன.
தனிமங்கள் நீராற்பகுக்கப்படுதல் ஆக்சிசனேற்றம் அடைதல் என்ற இரு வேறு வழிகளால் அரிப்புக்கு உள்ளாகின்றன. தண்ணீர் மற்றும் ஆக்சிசன் சேர்ந்து உருவாகும் அரிப்பு இன்னும் அதிகமானதாகும். கிட்டத்தட்ட அனைத்து தனிமங்களும் வளி மண்டலத்தில் இருக்கும் ஆக்சிசன் அல்லது ஆக்சிசன் நிறைந்த சூழலில் எரிகின்றன. நீர் மற்றும் காற்று கலந்த சூழலில் பொதுவாக காற்றில் சோடியம் போன்ற உலோகங்கள் தீவிரமாக எரிந்து ஐதராக்சைடுகளை உருவாக்குகின்றன. இதன் காரணமாகவே கார உலோகங்களும் கார மண் உலோகங்களும் அவற்றின் உலோக வடிவில் கிடைப்பதில்லை. சீசியம் ஆக்சிசனுடன் தீவிரமாக வினைபுரிகிறது. இதனால் வெற்றிடக் குழாய்களில் வாயு அகற்றியாக இது பயன்படுத்தப்படுகிறது. சோடியம் மற்றும் பொட்டாசியம் கரைசல்கள் ஆக்சிசன் நீக்கியாக சில கரிமக் கரைப்பான்களில் பயன்படுத்தப்படுகிறது. பெரும்பாலான தனிமங்களின் மேற்பரப்பு ஆக்சைடு மற்றும் ஐதராக்சைடு படலங்கலால் ஆனதாகும். அலுமினியம் தனிமத்தின் அலுமினியம் ஆக்சைடு படலம் உருவாகி அதன் வினையை மட்டுப்படுத்தி அரிப்பிலிருந்து பாதுகாக்கிறது. உலோக பகுதிகள் மீது மேலும் ஆக்சைடு படலத்தை உருவாக்கி உலோகங்களை அரிப்பிலிருந்து பாதுகாக்கிறார்கள். மக்னீசியம் மற்றும் அலுமினியம் உலோகங்கள் திட்ட வெப்பநிலை அழுத்தத்தில் ஆக்சிசனுடன் மெதுவாக வினைபுரிகின்றன. நன்றாக தூளாக்கப்பட்ட பெரும்பாலான தனிமங்களின் தூள்கள் பயங்கரமாக வெடிக்கும் தன்மையைக் கொண்டுள்ளன. திண்ம எரிபொருள் ஏவுர்திகளில் இவற்றை பயன்படுத்துகிறார்கள்.

இரும்பு உலர் ஆக்சிசனுடன் வினைபுரிந்து இரும்பு (II) ஆக்சைடாக உருவாகிறது. ஆனால் நீரேற்ற பெரிக் ஆக்சைடுகள் (Fe2O3−x(OH)2x) உருவாக ஆக்சிசனும் நீரும் அவசியமாகிறது. 3.5 பில்லியன் ஆண்டுகளுக்கு முன்னர் கடலில் வீழ்படிவாக்கப்பட்ட இரும்பிலிருந்து ஒளிச்சேர்க்கை பாக்டீரியா மூலம் ஏமடைட்டு என்ற கனிமமாக மாற்றப்பட்டு வெளிப்படுவதாகக் கருதப்படுகிறது.
கட்டமைப்பு[தொகு]
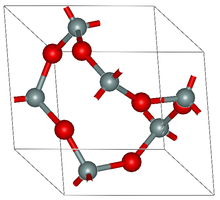
தனித்த மூலக்கூறுகளிலிருந்து பல்லுருவ மற்றும் படிக அமைப்புகள் வரை ஆக்சைடுகள் பல்வேறு வகையான கட்டமைப்புகள் கொண்டுள்ளன. திட்ட வெப்ப அழுத்த நிலையில் ஆக்சைடுகள் திடப்பொருட்களிலிருந்து வாயுக்கள் வரை இருக்கின்றன.
உலோக ஆக்சைடுகள்[தொகு]
பெரும்பாலான உலோகங்களின் ஆக்சைடுகள் பலபகுதி கட்டமைப்பை ஏற்றுக்கொள்கின்றன. ஆக்சைடுகள் பொதுவாக மூன்று உலோக அணுக்களுடன் இணைந்திருக்கின்றன. (எ.கா, உரூட்டைல் கனிமம்) அல்லது ஆறு உலோக அணுக்களுடன் (கார்போரண்டம் அல்லது பாறை உப்பு கட்டமைப்பு) இணைந்திருக்கின்றன. M-O பிணைப்புகள் பொதுவாக வலுவானவையாக இருப்பதால் இந்த சேர்மங்கள் குறுக்கிணைப்பு பலபடிகளாகக் கருதப்படுகின்றன. திண்மங்கள் அமிலங்கள், காரங்களால் பாதிக்கப்பட்டாலும் கரைப்பான்களில் கரையாத தன்மையைப் பெறுகின்றன. வாய்ப்பாடுகள் மிக எளிமையானவையாகும். பல ஆக்சைடுகள் விகிதவியல் அளவுகளில் இருப்பதில்லை.
ஒடுக்க வினைகள்[தொகு]
உலோகங்கள் அதன் ஆக்சைடுகளில் இருந்து ஒரு ஒடுக்கும் முகவரை சேர்ப்பதன் மூலமாக ஒடுக்க வினை நிகழ்ந்து எளிமையாகப் பிரித்தெடுக்கப்படுகின்றன. பெரும்பாலும் கார்பன் கல்கரி வடிவில் ஒடுக்கும் முகவராகச் செயல்படுகிறது. இரும்புத் தாதுவை ஒடுக்கி இரும்பு தயாரித்தல் மிகவும் எளிய எடுத்துக் காட்டாகும். பல படிநிலைகள் இருந்தாலும் தொகுக்கப்பட்ட சமன்பாடு இங்கு தரப்படுகிறது.
- 2 Fe2O3 + 3 C → 4 Fe + 3 CO2
உலோக ஆக்சைடுகள் கரிமச் சேர்மங்களால் ஒடுக்கப்படுகின்றன. இச்செயல்முறை பல வேதியியல் மாற்ற செயல்பாடுகளுக்கு அடிப்படையாக அமைகிறது.
வெப்ப சிதைவு[தொகு]
வினைத்திறன் குறைவாக உள்ள தனிமங்களின் ஆக்சைடுகள் வெப்பப் படுத்துவதால் ஒடுக்கமடைகின்றன. உதாரணமாக வெள்ளி ஆக்சைடு 200 பாகை செல்சியசு வெப்பநிலைக்கு சூடுபடுத்துவதால் ஒடுக்கமடைகிறது.[3].
- 2 Ag2O → 4 Ag + O2
இடப்பெயர்ச்சி ஒடுக்கம்[தொகு]
அதிக வினைத்திறன் கொண்ட உலோகத்தின் ஆக்சைடுகள் வினைத்திறன் குறைந்த உலோகத்தின் ஆக்சைடுகளை இடப்பெயர்ச்சி செய்து ஒடுக்கமடைகின்றன. எடுத்துக்காட்டாக துத்தநாகம் வினைத்திறன் மிக்கது ஆகும், இது அதைவிட வினைத்திறன் குறைந்த தாமிரத்தின் ஆக்சைடை இடப்பெயர்ச்சி செய்கிறது,
- Zn + CuO → ZnO + Cu
நீரேற்றல் தாக்கம்[தொகு]
இலத்திரன் நாட்டம் குறைவான தனிமங்களின் ஒக்சைட்டுகளை நீரில் கரைக்கும் போது நீரேற்றல் தாக்கம் நடைபெறும். உதாரணமாக சோடியம் ஒக்சைட்டு (கார இயல்புள்ளது) நீரில் கரைக்கப்படும் போது சோடியம் ஐதரொக்சைட்டு உருவாகும்.
- O2− + H2O → 2 OH−
ஒக்சைட்டுகளுக்கு சில உதாரணங்கள்[தொகு]
| பெயர் | மூலக்கூற்று வாய்ப்பாடு | விபரம் |
|---|---|---|
| நீர் (ஐதரசன் ஒக்சைட்டு) | H 2O |
மிக முக்கிய கரைப்பான், உயிரினங்களின் அவசியத் தேவை |
| நைட்ரஸ் ஒக்சைட்டு | N 2O |
சிரிப்பூட்டும் வளிமம், உணர்வகற்றி, நைதரசன் நிலைப்படுத்தலால் பெறப்படும் உணர்வகற்றிகள், ஏவூர்திகளில், பைங்குடில் வளிமம் போன்றவற்றில் ஆக்சிசனேற்றியாக. NO 2, (NO), N 2O 3, N 2O 4 போன்ற நைதரசன் ஆக்சைடுகளும் (உள்ளன. (குறிப்பாக வளி மாசடையும் இடங்களில்). அமில மழையில் நைட்ரிக் காடியைத் தோற்றுவித்து உடலுக்குக் கேடு விளைவிக்கும். |
| சிலிக்கனீரொக்சைட்டு | SiO 2 |
மணல், குவார்ட்சு ஆகியவற்றில் உள்ளது |
| இரும்பு(II,III)ஒக்சைட்டு | Fe 3O 4 |
இரும்பு(III)ஒக்சைட் (Fe 2O 3) உடன் இரும்புத் தாது, துரு போன்ற பொருட்களிலுள்ளது. |
| அலுமினியம் ஒக்சைட்டு | Al 2O 3 |
அலுமினியத் தாதான அலுமினா மற்றும் குருந்தம், மாணிக்கம் ஆகியவற்றில் உள்ளது |
| நாக ஒக்சைட்டு | ZnO | இறப்பரை வல்கனைசுப்படுத்தப் பயன்படுகின்றது, கொங்கிறீட்டு, ஒப்பனைப் பொருட்கள் ஆகியவற்றில் சேர்க்கப்படுகின்றது, தோல் பாதுகாப்புப் பொருட்களில் பயன்படுகின்றது. வெள்ளை நிறத் தூள் |
| காபனீரொக்சைட்டு | CO 2 |
புவியின் வளிமண்டலத்தை ஆக்கும் வாயுக்களில் ஒன்று, மிகவும் முக்கியமான பச்சை வீட்டு வாயு, ஒளித்தொகுப்பில் எளிய சீனிகளை உருவாக்கப் பயன்படும், சுவாசித்தல் மற்றும் நொதித்தலின் போது பிரதான விளைவாகப் பெறப்படும், சேதனப் பொருட்கள் எரியும் போது விளைவாகக் கிடைக்கும். CO அல்லது காபனோரொக்சைட்டு மற்றைய காபன் ஒக்சைட்டாகும். |
| கால்சியம் ஒக்சைட்டு | CaO | நீறாத சுண்ணாம்பு என அழைக்கப்படும் |
மேற்கோள்கள்[தொகு]
- ↑ Foundations of College Chemistry, 12th Edition
- ↑ Greenwood, N. N.; & Earnshaw, A. (1997). Chemistry of the Elements (2nd Edn.), Oxford:Butterworth-Heinemann. பன்னாட்டுத் தரப்புத்தக எண் 0-7506-3365-4.
- ↑ http://chemister.ru/Database/properties-en.php?dbid=1&id=4098
