புளுட்டோனியம்(IV) ஆக்சைடு
| |
| பெயர்கள் | |
|---|---|
| ஐயூபிஏசி பெயர்
புளுட்டோனியம்(IV) ஆக்சைடு
| |
| முறையான ஐயூபிஏசி பெயர்
புளுட்டோனியம்(4+) ஆக்சைடு | |
| வேறு பெயர்கள்
புளுட்டோனியம் டையாக்சைடு
| |
| இனங்காட்டிகள் | |
| 12059-95-9 | |
| ChemSpider | 10617028 |
InChI
| |
| யேமல் -3D படிமங்கள் | Image |
SMILES
| |
| பண்புகள் | |
| O2Pu | |
| வாய்ப்பாட்டு எடை | 276.00 g·mol−1 |
| தோற்றம் | அடர் மஞ்சள் படிகங்கள் |
| அடர்த்தி | 11.5 கி செ.மீ−3 |
| உருகுநிலை | 2,744 °C (4,971 °F; 3,017 K) |
| கொதிநிலை | 2,800 °C (5,070 °F; 3,070 K) |
| கட்டமைப்பு | |
| படிக அமைப்பு | புளோரைட்டு (கனசதுரம்), cF12 |
| புறவெளித் தொகுதி | Fm3m, No. 225 |
| ஒருங்கிணைவு வடிவியல் |
நான்முகி (O2−); கனசதுரம் (PuIV) |
| தீங்குகள் | |
| முதன்மையான தீநிகழ்தகவுகள் | கதிரியக்கம் |
| தீப்பற்றும் வெப்பநிலை | தீப்பற்றாது |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
| | |
| Infobox references | |
புளுட்டோனியம்(IV) ஆக்சைடு (Plutonium(IV) oxide) என்பது PuO2. என்ற மூலக்கூற்று வாய்ப்பாட்டால் விவரிக்கப்படும் ஒரு கனிம வேதியியல் சேர்மமாகும். உயர் உருகுநிலை கொண்ட இத்திண்மம் புளுட்டோனியத்தின் முதன்மையான சேர்மமாகும். துகள்களின் அளவு, வெப்பநிலை, உற்பத்தி முறை ஆகியனவற்றைப் பொறுத்து இதன் நிறம் மஞ்சள் நிறம் அல்லது ஆலீவ் பச்சை நிறம் என்று மாறுபடும்.
கட்டமைப்பு[தொகு]
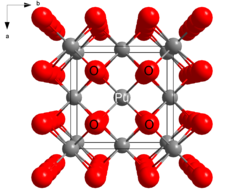
புளுட்டோனியம்(IV) ஆக்சைடு சேர்மம் புளோரைட்டு நோக்குருவில் Pu4+ அயனி மையங்கள் முக மைய்ய கனசதுர கட்டமைப்பிலும் ஆக்சைடு அயனிகள் நான்முகியின் துளைகளிலும் ஆக்கிரமித்து படிகமாகிறது. அணுக்கரு எரிபொருளாக PuO2 சேர்மத்தை பயன்படுத்த முடியும். எண்முக துளைகளில் உள்ள காலியிடங்கள் அணுக்கரு பிளவு விளைபொருள்களை அனுமதிக்கிறது.
பண்புகள்[தொகு]
புளுட்டோனியம்(IV) ஆக்சைடு நிலைப்புத் தன்மையுடன் காணப்படும் ஒரு பீங்கான் வகை பொருளாகும். தண்ணீரில் குறைந்த அளவே கரைகிறது. 2744 பாகை செல்சியசு என்ற உயர் உருகுநிலையை கொண்டுள்ளது.
விரைவு சீரொளி உருகும் ஆய்வு ஆதாரங்களின் அடிப்படையில் புளுட்டோனியம்(IV) ஆக்சைடின் உருகுநிலை 2011 ஆம் ஆண்டு மேலும் சில நூறு பாகைகள் வரை உயர்த்தப்பட்டது. மேற்கொண்ட ஆய்வுகள் மாசுபாடுகள் ஏதும் இல்லாத கொள்கலன்கள் ஆய்வுக்கு எடுத்துக் கொள்ளப்படுகின்றன. புளுட்டோனியத்தின் கதிரியக்க ஆல்பா சிதைவுப் பண்பு காரணமாக, PuO2 சேர்மத்தை தொடும்போது சூடாக இருக்கும். அனைத்து புளுட்டோனியம் சேர்மங்களையும் போலவே இதுவும் அணு பரவல் அல்லாத ஒப்பந்தத்தின் கீழ் கட்டுப்பாட்டுக்கு உட்பட்டதாகும்.
தயாரிப்பு[தொகு]
ஆக்சிசன் சூழலில் புளுட்டோனியம் தன்னிச்சையாகவே ஆக்சிசனேற்றம் அடைந்து புளுட்டோனியம்(IV) ஆக்சைடாக மாறுகிறது. புளுட்டோனியம்(IV) ஆக்சலேட்டை (Pu(C2O4)2•6H2O) 300 பாகை செல்சியசு வெப்பநிலையில் சுட்டு புளுட்டோனியம்(IV) ஆக்சைடு தயாரிப்பது பிரதானமான தயாரிப்பு முறையாகும். HNO3/HF அமிலத்தில் கரைந்த புளுட்டோனியத்தை அணுக்கரு எரிபொருளாக பயன்படுத்திய பின்னர் மேற்கொள்ளப்படும் மறுசெயல்முறையில் புளுட்டோனியம் ஆக்சலேட்டு கிடைக்கிறது[1]. உருகிய-உப்பு வளர்ப்பு அணு உலைகளில் கிடைக்கும் யுரேனியம் நீக்கப்பட்ட எரிபொருள் உப்புடன் சோடியம் கார்பனேட்டைச் சேர்த்தும் புளுட்டோனியம்(IV) ஆக்சைடை மீட்டெடுக்க முடியும்.
பயன்கள்[தொகு]

புளுட்டோனியம் டையாக்சைடுடன் யுரேனியம் டையாக்சைடை சேர்த்து கலப்பு ஆக்சைடு எரிபொருளாக அணுக்கரு உலைகளில் பயன்படுத்துகிறார்கள். நாசாவினால் விண்ணுக்கு ஏவப்பட்டிருக்கும் தானியங்கி விண்கலமான நியூ ஆரிசான்சு புளூட்டோ ஆய்வு குறுங்கோள், செவ்வாய் கிரகத்தின் அறிவியல் ஆய்வுக்கூடத் திட்டத்தின் ஒரு பகுதியான கியூரியோசிட்டி தரையளவி விண்கலம் போன்ற பல தொலைநோக்கு விண்கலங்களுக்கு புளுட்டோனியம்-238 ஐசோடோப்பை எரிபொருளாகப் பயன்படுத்தியுள்ளார்கள். ஐசோடோப்பு ஆல்பா கதிர்களை உமிழ்ந்து கதிரியக்க சிதைவு அடைவதால் வெப்பம் உற்பத்தி செய்யப்படுகிறது. விண்வெளி சுற்றுப்பாதையிலிருந்து பூமியின் வளிமண்டலத்தில் தற்செயலாக மீண்டும் நுழைவது ஒரு விண்கலத்தின் உடைப்பு மற்றும் / அல்லது எரிவதற்கு வழிவகுக்கும் என்ற கவலைகள் உள்ளன. இதன் விளைவாக கிரக மேற்பரப்பின் ஒரு பெரிய பகுதிக்கு மேல் அல்லது மேல் வளிமண்டலத்திற்குள் புளுட்டோனியம் சிதறடிக்கப்படும். இருப்பினும், PuO2 கதிரியக்க ஐசோடோ வெப்பமின் மின்னாக்கிகளைக் கொண்டு சென்ற குறைந்தது இரண்டு விண்கலங்கள் தற்செயலாக பூமியின் வளிமண்டலத்தை அடைந்து எரிந்துவிட்டன. மே 1968 இல் நிம்பசு பி -1 மற்றும் ஏப்ரல் 1970 இல் அப்பல்லோ 13 சந்திர தொகுதி விண்கலம் ஆகியவை அவ்விரண்டு விண்கலங்களாகும்[2][3]. இரு விண்கலங்களிலிலும் இருந்த கதிரியக்க ஐசோடோப்பு வெப்பமின் மின்னாக்கிகள் மறுநுழைவிலிருந்து தப்பித்தன. இவற்றின் தாக்கம் அப்படியே உள்ளது. ஆனால் சுற்றுச்சூழல் மாசுபாடு எதுவும் குறிப்பிடப்படவில்லை. டிரான்சிட் 5-பிஎன் -3 விண்கலம் 1964 இல் ஏவப்பட்ட போது சந்தித்த தோல்வியைத் தொடர்ந்து 1960 ஆம் ஆண்டுகளின் நடுப்பகுதியில் கதிரியக்க ஐசோடோப்பு வெப்பமின் மின்னாக்கிகள் மறுவாழ்வு மற்றும் தாக்கத்தின் போது அப்படியே இருக்குமாறு வடிவமைக்கப்பட்டுள்ளன. ஆரம்ப தலைமுறை புளுட்டோனியம்-உலோக கதிரியக்க ஐசோடோப்பு வெப்பமின் மின்னாக்கிகள் புவியின் விண்வெளியில் மறுநுழைவு செய்து சிதைந்து கதிரியக்கப் பொருள்களை மடகாசுகருக்கு வடக்கே வளிமண்டலத்தில் சிதறடித்தது, பின்னர் அனைத்து அமெரிக்க கதிரியக்க ஐசோடோப்பு வெப்பமின் மின்னாக்கிகளையும் மறுவடிவமைப்பு செய்யவும் தூண்டியது. பின்னர் இத்திட்டம் பயன்பாட்டில் அல்லது வளர்ச்சியில் இருந்தது[4]. இயற்பியலாளர் பீட்டர் சிம்மர்மேன், டெட் டெய்லரின் ஆலோசனையைப் பின்பற்றி, குறைந்த உற்பத்தி (1-கிலோ டன்) அணு ஆயுதத்தை புளுட்டோனியம் ஆக்சைடில் இருந்து ஒப்பீட்டளவில் எளிதாக உருவாக்க முடியும்[5] என்பது நிருபிக்கப்பட்டது. ஒரு புளுட்டோனியம்-ஆக்சைடு குண்டு புளுட்டோனியம் உலோகத்திலிருந்து தயாரிக்கப்படும் குண்டைக்காட்டிலும் கிட்டத்தட்ட மூன்று மடங்கு பெரியதாகவும் அதிக அடர்த்தியை கொண்டதாகவும் இருக்கும். ஆக்சைடு தூள் வடிவில் இருந்தால் அளவு இன்னும் மிகப்பெரியதாக இருக்கும்[6].
முன்பாதுகாப்பு[தொகு]
உடலில் உள்ள புளுட்டோனியம் ஆக்சைட்டின் நடத்தை அது உட்கொள்ளபட்ட விதத்திற்கேற்ப மாறுபடும். இது கரையாத பொருள் என்பதால் , உட்கொள்ளப்பட்டதில் மிகப் பெரிய சதவீதம் உடல் கழிவுகளாக உடலில் இருந்து மிக விரைவாக அகற்றப்படும்[7]. துகள் வடிவ 10 மைக்ரோ மீட்டருக்கும் குறைவான (0.01 மிமீ) துகள் உள்ளிழுக்கப்பட்டால் புளூட்டோனியம் ஆக்சைடு அதன் ஆல்பா-உமிழ்வு காரணமாக நச்சுத்தன்மையை உண்டாக்கும்[8].
மேற்கோள்கள்[தொகு]
- ↑ Jeffrey A. Katalenich Michael R. Hartman Robert C. O’Brien Steven D. Howe (Feb 2013). "Fabrication of Cerium Oxide and Uranium Oxide Microspheres for Space Nuclear Power Applications". Proceedings of Nuclear and Emerging Technologies for Space 2013: 2. https://inldigitallibrary.inl.gov/sti/5680982.pdf. பார்த்த நாள்: 2019-11-04.
- ↑ A. Angelo Jr. and D. Buden (1985). Space Nuclear Power. Krieger Publishing Company. பன்னாட்டுத் தரப்புத்தக எண்:0-89464-000-3.
- ↑ "General Safety Considerations" (PDF). Fusion Technology Institute, University of Wisconsin–Madison. Spring 2000. Archived from the original (PDF lecture notes) on 2018-09-15. பார்க்கப்பட்ட நாள் 2019-11-04.
- ↑ "Transit". Encyclopedia Astronautica. பார்க்கப்பட்ட நாள் 2013-05-07.
- ↑ Michael Singer; David Weir; Barbara Newman Canfield (Nov 26, 1979). "Nuclear Nightmare: America's Worst Fear Come True". New York Magazine.
- ↑ Sublette, Carey. "4.1 Elements of Fission Weapon Design". The Nuclear Weapon Archive. 4.1.7.1.2.1 Plutonium Oxide. பார்க்கப்பட்ட நாள் 20 October 2017.
The critical mass of reactor grade plutonium is about 13.9 kg (unreflected), or 6.1 kg (10 cm nat. U) at a density of 19.4. A powder compact with a density of 8 would thus have a critical mass that is (19.4/8)^2 time higher: 82 kg (unreflected) and 36 kg (reflected), not counting the weight of the oxygen (which adds another 14%). If compressed to crystal density these values drop to 40 kg and 17.5 kg.
- ↑ United States Nuclear Regulatory Commission, Fact sheet on plutonium (accessed Nov 29 2013)
- ↑ "Toxicological Profile For Plutonium" (PDF). U.S. Department of Health and Human Services. 2007-09-27. பார்க்கப்பட்ட நாள் 2009-04-23.
