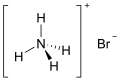
அமோனியம் புரோமைடு
| |

| |
| பெயர்கள் | |
|---|---|
| ஐயூபிஏசி பெயர்
அமோனியம் புரோமைடு
| |
| இனங்காட்டிகள் | |
| 12124-97-9 | |
| ChEBI | CHEBI:85364 |
| ChemSpider | 23804 |
| யேமல் -3D படிமங்கள் | Image |
| வே.ந.வி.ப எண் | BO9155000 |
| |
| UNII | R0JB3224WS |
| பண்புகள் | |
| NH4Br | |
| வாய்ப்பாட்டு எடை | 97.94 கி/மோல் |
| தோற்றம் | வெண்மைநிறத் தூள், நீருறிஞ்சி |
| அடர்த்தி | 2.429 கி/செ.மீ3 |
| உருகுநிலை | 235 °C (455 °F; 508 K) |
| கொதிநிலை | 452 °C (846 °F; 725 K) |
| 60.6 g/100 mL (0 °C) 78.3 g/100 mL (25 °C) 145 g/100 mL (100 °C) | |
| ஒளிவிலகல் சுட்டெண் (nD) | 1.712 |
| கட்டமைப்பு | |
| படிக அமைப்பு | சம அளவு |
| தீங்குகள் | |
| GHS pictograms |  [1] [1]
|
| H319[1] | |
| P305+351+338 | |
| தொடர்புடைய சேர்மங்கள் | |
| ஏனைய எதிர் மின்னயனிகள் | அமோனியம் புளோரைடு அமோனியம் குளோரைடு அமோனியம அயோடைடு |
| ஏனைய நேர் மின்அயனிகள் | சோடியம் புரோமைடு பொட்டாசியம் புரோமைடு |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
அமோனியம் புரோமைடு (Ammonium bromide) என்பது NH4Br என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட ஐதரோ புரோமிக் அமிலத்தினுடைய அமோனியம் உப்பாகும். உவர்ப்புச் சுவையுடன் காணப்படும் இச்சேர்மம் நிறமற்ற பட்டகமாகப் படிகமாகிறது. சூடுபடுத்தும்போது பதங்கமாகும் தன்மையைப் பெற்றிருக்கும் இச்சேர்மம் தண்ணீரில் எளிதாகக் கரைகிறது. காற்றுடன் தொடர்பு கொள்ள நேர்ந்தால் படிப்படியாக மஞ்சள் நிறமாக மாறுகிறது. ஏனெனில் புரோமைடு அயனியில் சிறிதளவு புரோமினாக ஆக்சிசனேற்றம் அடைகிறது.
தயாரிப்பு
[தொகு]ஐதரசன் புரோமைடை நேரடியாக அமோனியாவுடன் சேர்த்து வினைபுரியச் செய்தால் அமோனியம் புரோமைடு உருவாகிறது.
- NH3 + HBr → NH4Br
இரும்பு(II) புரோமைடு அல்லது இரும்பு(III) புரோமைடுடன் அமோனியாவை வினைபடச் செய்வதன் மூலமாகவும் இதைத் தயாரிக்க முடியும். அதாவது இரும்புத் துருவல்கள் மீது நீர்த்த புரோமின் கரைசலைச் செலுத்தி அமோனியம் புரோமைடு தயாரிக்க முடியும்.
- 2 NH3 + FeBr2 + 2 H2O → 2 NH4Br + Fe(OH)2
வினைகள்
[தொகு]அமோனியம் புரோமைடு ஒரு வீரியம் குறைந்த அமிலமாகும். தண்ணீரில் இதனுடைய காடித்தன்மை எண் ~5 என்ற அளவாகும். அமோனியம் அயனி நீரில் சிறிதளவு நீராற்பகுப்பு அடைவதால் இவ்வுப்பை அமில உப்பு என்றும் அழைப்பர். தண்ணீரில் இடப்பட்ட அமோனியம் புரோமைடு ஒரு வலிமையான மின்பகுளியாகும்.
- NH4Br(s) → NH4+(aq) + Br−(aq)
உயர்மட்ட வெப்பநிலைக்கு சூடாக்கும்போது இச்சேர்மம் அமோனியாவாகவும் ஐதரசன் புரோமைடாகவும் சிதைவடைகிறது.
- NH4Br → NH3 + HBr
பயன்கள்
[தொகு]அமோனியம் புரோமைடு படமெடுக்கும் புகைப்படத் தொழிலில் பயன்படுகிறது, காகிதங்கள், தட்டுகள் மற்றும் தீத்தடுப்பானாகவும் பயன்படுகிறது. பதிவச்சு மற்றும் செதுக்கும் செயல்முறைகள், அரிமானத் தடுப்பு, மற்றும் மருந்துகள் தயாரித்தல் போன்றவற்றில் பயன்படுகிறது[2]
மேற்கோள்கள்
[தொகு]- ↑ 1.0 1.1 Sigma-Aldrich Co., Ammonium bromide. Retrieved on 2013-07-20.
- ↑ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, பன்னாட்டுத் தரப்புத்தக எண் 0-07-049439-8
