மாலிப்டினம்(V) குளோரைடு

| |
| |
| பெயர்கள் | |
|---|---|
| ஐயூபிஏசி பெயர்s
மாலிப்டினம்(V) குளோரைடு
மாலிப்டினம் பென்டாகுளோரைடு | |
| இனங்காட்டிகள் | |
| 10241-05-1 | |
| EC number | 233-575-3 |
| பப்கெம் | 61497 |
| வே.ந.வி.ப எண் | QA4690000 |
| UNII | BB0UFP2VO5 |
| பண்புகள் | |
| Cl10Mo2 | |
| வாய்ப்பாட்டு எடை | 273.21 கி/மோல் (MoCl5) |
| தோற்றம் | அடர் பச்சை திண்மம் நீருரிஞ்சும் இணைகாந்தம் |
| அடர்த்தி | 2.928 கி/செ.மீ3 |
| உருகுநிலை | 194 °C (381 °F; 467 K) |
| கொதிநிலை | 268 °C (514 °F; 541 K) |
| நீராற்பகுப்பு அடைகிறது. | |
| கரைதிறன் | உலர்ஈதர், உலர் ஆல்ககால், கரிமக் கரைப்பான்கள் போன்றவற்றில் கரையும் |
| கட்டமைப்பு | |
| படிக அமைப்பு | monoclinic |
| ஒருங்கிணைவு வடிவியல் |
edge-shared bioctahedron |
| தீங்குகள் | |
| முதன்மையான தீநிகழ்தகவுகள் | ஆக்சிசனேற்றி, நீராற்பகுப்பு அடைந்து HCl விடுவிக்கப்படுகிறது. |
| தீப்பற்றும் வெப்பநிலை | எளிதில் தீப்பற்றாது |
| தொடர்புடைய சேர்மங்கள் | |
| ஏனைய எதிர் மின்னயனிகள் | மாலிப்டினம்(V) புளோரைடு மாலிப்டினம்(V)(IV) புரோமைடு மாலிப்டினம்(III) அயோடைடு |
| ஏனைய நேர் மின்அயனிகள் | குரோமியம்(IV) குளோரைடு தங்குதன்(V) குளோரைடு |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
| | |
| Infobox references | |
மாலிப்டினம்(V) குளோரைடு (Molybdenum(V) chloride) (MoCl5)2 என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட கனிம வேதியியல் சேர்மமாகும். அடர் கருப்பு நிறச் சேர்மமான இச்சேர்மம் பிற மாலிப்டினம் சேர்மங்களை தயாரிக்க ஆராயப்பட்டு வருகிறது. ஈரத்தால் பாதிக்கப்படும் இச்சேர்மம் குளோரினேற்றம் பெற்ற கரைப்பான்களில் கரைகிறது. மாலிப்டினம் பென்டாகுளோரைடு என்று வழக்கமாக அழைக்கப்படும் இச்சேரம் உண்மையில் இருபடி Mo2Cl10 என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட ஒரு இருபடியாகும்[1]
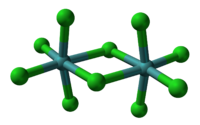
கட்டமைப்பு[தொகு]
ஒவ்வொரு மாலிப்டினமும் உட்புற எண்முக சீரொழுங்கும், மாலிப்டின மையங்களுக்கு[2] இடையில் இரண்டு குளோரைடு பாலங்களையும் கொண்டுள்ளன. இதே கட்டமைப்பு தங்குதன், நையோபியம், டாண்ட்டலம் பென்டாகுளோரைடுகளில் காணப்படுகிறது[3]. வாயு முகநிலையிலும் கரைசல்களில் பகுதியாகவும் இந்த இருபடிகள் சிறிதளவு சிதைவடைந்து ஒருபடி பென்டா ஆலைடைக் கொடுக்கின்றன[4] . இவை இணைகாந்தப் பண்பு கொண்டு, மாலிப்டின மையங்கள் ஒவ்வொன்றும் இணைபிரிந்த எலக்டரானைப் பெற்றுள்ளன. முறையான +5 ஆக்சிசனேற்ற நிலையில் உலோக மையத்தின் மீது இணைதிறன் எலக்ட்ரானை விடுவிக்கின்றன.
தயாரிப்பும் வேதி வினைகளும்[தொகு]
Mo தனிமத்தை குளோரினேற்றம் செய்தும், MoO3 சேர்மத்தை குளோரினேற்றம் செய்தும் மாலிப்டினம்(V) குளோரைடைத் தயாரிக்கலாம். இம்முறையில் நிலைப்புத்தன்மையற்ற மாலிப்டினம் எக்சாகுளோரைடு உற்பத்தியாவதில்லை[5]
MoCl5 ஒரு வலுவான ஆக்சிசனேற்றியாகும். அசிட்டோநைட்ரைலால் ஒடுக்கப்பட்டு ஆரஞ்சுநிற அணைவுச் MoCl4(MeCN)2, சேர்மத்தைக் கொடுக்கிறது. பின்னர் இது டெட்ரா ஐதரோ பியூரானுடன் வினைபுரிந்து MoCl4(THF)2 என்ற பிற மாலிப்டினமுள்ள அணைவுச் சேர்மங்கள் தயாரிப்பில் உதவும் முன்னோடிச் சேர்மத்தைக் கொடுக்கிறது. MoCl5 சேர்மம் HBr ஆல் ஒடுக்கப்பட்டு MoBr4 உருவாகிறது[6].
-50 பாகை செல்சியசு வெப்பநிலையில் எத்தில் புரோமைடு முன்னிலையில் புரோமினேற்றம் நிகழ்ந்து இடைநிலையாக MoBr5 உருவாகிறது. 20 ° செல்சியசு வெப்பநிலையில் Br2 உருவாக்கப்பட்டு மாலிப்டினத்தின் வழக்கமான +5 ஆக்சிசனேற்ற நிலை +4 ஆக்சிசனேற்ற நிலையாக மாறுகிறது. வினையில் நிகழும் ஒட்டுமொத்த மாற்றமும் இச்சமன்பாட்டில் தரப்பட்டுள்ளது.
2 MoCl5 + 10 HBr → 2 MoBr4 + 10 HCl + Br2
MoBr4 , டெட்ரா ஐதரோபியூரானுடன் வினைபுரிந்து Mo(III) இனத்தைச் சார்ந்த மெர்-MoBr3(THF)3 கிடைக்கிறது. எளிதில் ஆக்சிசனமேற்றமடையாத ஈந்தணைவி களுக்கு எதிராக MoCl5 ஒரு நல்ல இலூயிக் அமிலமாக விளங்குகிறது[7]
குளோரைடுடன் வினைபுரிந்து [MoCl6]− என்ற ஒரு கூட்டு விளைபொருளாக உருவாகிறது. குளோரினேற்றம், ஆக்சிசன்நீக்கம், ஆக்சிசனேற்ற பிணைப்பு வினைகள் போன்ற கரிமத்தொகுப்பு வினைகளில் அரிதாக மாலிப்டினம்(V) குளோரைடு பயன்படுத்தப்படுகிறது[8]
முன்பாதுகாப்பு[தொகு]
மாலிப்டினம்(V) குளோரைடு ஒரு தீவிரமான ஆக்சிசனேற்ரி என்பதால் விரைவாக நீராற்பகுப்பு அடைந்து ஐதரசன் குளோரைடு வாயுவை விடுவிக்கிறது.
மேற்கோள்கள்[தொகு]
- ↑ Holleman, A. F.; Wiberg, E. (2001). Inorganic Chemistry. San Diego, CA: Academic Press. பன்னாட்டுத் தரப்புத்தக எண்:0-12-352651-5.
- ↑ Beck, J.; Wolf, F. (1997). "Three New Polymorphic Forms of Molybdenum Pentachloride". Acta Crystallogr. B53: 895–903. doi:10.1107/S0108768197008331.
- ↑ Wells, A. E. (1984). Structural Inorganic Chemistry (5th ). Oxford: Clarendon Press. https://archive.org/details/structuralinorga0000well_m8i1.
- ↑ Brunvoll, J.; Ischenko, A. A.; Spiridonov, V. P.; Strand, T. G. (1984). "Composition and Molecular Structure of Gaseous Molybdenum Pentachloride by Electron Diffraction". Acta Chem. Scand. A38: 115–120. doi:10.3891/acta.chem.scand.38a-0115.
- ↑ Tamadon, Farhad; Seppelt, Konrad (2013). "The Elusive Halides VCl5, MoCl6, and ReCl6". Angew. Chem. Int. Ed. 52: 767–769. doi:10.1002/anie.201207552.
- ↑ Dilworth, J. R.; Richards, R. L. (1990). "The Synthesis of Molybdenum and Tungsten Dinitrogen Compounds". Inorg. Synth. 28: 33–45. பன்னாட்டுத் தரப்புத்தக எண்:0-471-52619-3.
- ↑ Calderazzo, F.; Maichle-Mössmer, C.; Pampaloni, G.; Strähle, J. (1993). "Low-temperature Syntheses of Vanadium(III) and Molybdenum(IV) Bromides by Halide Exchange". Dalton Trans. 1993: 655–658. doi:10.1039/DT9930000655.
- ↑ "Molybdenum(V) Chloride". Encyclopedia of Reagents for Organic Synthesis. (2004). New York, NY: J. Wiley & Sons.
