யுரேனியம்(III) குளோரைடு
| |
| பெயர்கள் | |
|---|---|
| ஐயூபிஏசி பெயர்
யுரேனியம்(III) குளோரைடு
| |
| வேறு பெயர்கள்
யுரேனியம் குளோரைடு
யுரேனியம் முக்குளோரைடு ஐப்போரானசு குளோரைடு | |
| இனங்காட்டிகள் | |
| 10025-93-1 | |
| ChemSpider | 146484 |
| யேமல் -3D படிமங்கள் | Image |
| பப்கெம் | 167444 |
SMILES
| |
| பண்புகள் | |
| Cl3U | |
| வாய்ப்பாட்டு எடை | 344.38 g·mol−1 |
| தோற்றம் | பச்சைநிற படிகத் திண்மம் |
| அடர்த்தி | 5.500 கி/செ.மீ3, நீர்மம் |
| உருகுநிலை | 837 °C (1,539 °F; 1,110 K) |
| கொதிநிலை | 1,657 °C (3,015 °F; 1,930 K) |
| கரையும் | |
| தீங்குகள் | |
| தீப்பற்றும் வெப்பநிலை | எளிதில் தீப்பற்றாது |
Autoignition
temperature |
எளிதில் தீப்பற்றாது |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
| | |
| Infobox references | |
யுரேனியம்(III) குளோரைடு (Uranium(III) chloride) என்பது UCl3 என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட ஒரு கனிம வேதியியல் சேர்மம் ஆகும். யுரேனியம் மற்றும் குளோரின் சேர்ந்து இச்சேர்மம் உருவாகிறது. பயன்படுத்தப்பட்ட அணுக்கரு எரிபொருளை மறுசுழற்சி மூலமாக மீண்டும் உபயோகப்படுத்த தயாரிக்கும் செயல்முறையில் யுரேனியம்(III) குளோரைடு பெரும்பாலும் பயன்படுகிறது. யுரேனியம்(IV) குளோரைடில் இருந்து பல்வேறு முறைகளில் யுரேனியம்(III) குளோரைடைத் தயாரிக்க முடியும். எனினும் யுரேனியம்(IV) குளோரைடைவிட, யுரேனியம்(III) குளோரைடு நிலைப்புத்தன்மை குறைந்தது ஆகும்.
தயாரிப்பு[தொகு]
யுரேனியம் (III) குளோரைடைத் தொகுப்பு முறையில் தயாரிக்க இரண்டு வழிகள் உள்ளன. பின்வரும் செயல்முறைகள் யுரேனியம் (III) குளோரைடு உற்பத்தி செய்வது குறித்து விவரிக்கின்றன.
1.யுரேனியம் நாற்குளோரைடுடன் தனிம யுரேனியத்தைச் NaCl-KCl கலவையுடன் சேர்த்து, 670–710 ° செ வெப்பநிலைக்கு சூடுபடுத்தினால் யுரேனியம்(III) குளோரைடு உருவாகிறது.
(2) யுரேனியம் நாற்குளோரைடை ஐதரசன் வாயுவுடன் சேர்த்து சூடாக்கியும் யுரேனியம்(III) குளோரைடு தயாரிக்கலாம்.
பண்புகள்[தொகு]
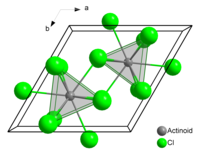
திடநிலை யுரேனியம் (III) குளோரைடு, ஒவ்வொரு யுரேனியம் அணுவும், ஒரு மூவுச்சி முக்கோணப் பட்டகக் கட்டமைப்பில் உள்ளது போல தோராயமாக அதே தூரத்தில் ஒன்பது குளோரின் அணுக்களை அருகாமை அண்டை அனுக்களாகப் பெற்றுள்ளன.
அறை வெப்பநிலையில் யுரேனியம்(III) குளோரைடு பச்சைநிற படிகத் திண்மமாகக் காணப்படுகிறது. 837° செல்சியசு வெப்பநிலையை உருகுநிலையாகவும் 1657° செல்சியசு வெப்பநிலையை கொதி நிலையாகவும் பெற்றுள்ள யுரேனியம்(III) குளோரைடு 5500 கி.கி/மீ3 அல்லது 5500 கி/செ.மீ3 அடர்த்தியுடனும் காணப்படுகிறது.[3]
எடை அடிப்படையில் யுரேனியம்(III) குளோரைடின் பகுதிப்பொருட்களின் எடை சதவீதம்:
குளோரின்: 30.84%
யுரேனியம்: 69.16%
இச்சேர்மத்தின் முறையான ஆக்சிசனேற்ற நிலைகள்:
குளோரின் : −1
யுரேனியம்: +3
அதிகமான நீருறிஞ்சும் திறன் கொண்ட யுரேனியம்(III) குளோரைடு நன்றாக தண்ணீரில் கரைகிறது. மற்றும் ஐதரோகுளோரிக் அமிலத்தில் நிலைப்புத் தன்மையுடன் காணப்படுகிறது.[4]
பயன்கள்[தொகு]
வினைச் செயலிகள்[தொகு]
நான்கைதரோ பியுரான் மற்றும் சோடியம் மெத்தில்சைக்ளோ பெண்டாடையீன் ஆகியனவற்றுடன் சேர்த்து யுரேனியம் மெட்டலோசீன் அணைவுச் சேற்மங்கள் தயாரிக்கப் பயன்படுகிறது.[5]
வினையூக்கிகள்[தொகு]
இலித்தியம் அலுமினியம் ஐதரைடு மற்றும் ஒலிஃபீன்கள் இடையிலான வினையின் போது யுரேனியம்(III) குளோரைடு வினையூக்கியாகப் பயன்பட்டு ஆல்க்கைல் அலுமினேட்டுச் சேர்மங்கள் தயாரிக்கப் பயன்படுகிறது.[6]
உருகிய வடிவம்[தொகு]
வெப்ப வேதியிய செயல்முறைகளில் யுரேனியம் (III) குளோரைடு, அணுசக்தி எரிபொருள்களின் மறுசீராக்கல் செயல்முறைக்கு முக்கியமா வேதிப்பொருளாக உதவுகிறது.[7] மின்தூய்மையாக்கல் செயல்முறைகளில் UCl3 வடிவத்தில் உள்ள யுரேனியம், எரிக்கப்பட்ட அணுக்கரு எரிபொருளை மறுசுழற்சிக்கு தயாரிக்கும் வடிவமாகக் கருதப்படுகிறது.[7][8]
நீரேற்றுகள்[தொகு]
யுரேனியம்(III) குளோரைடு மூன்று வகையான நீரேற்று வடிவங்களில் காணப்படுகிறது.
- UCl3.2H2O.2CH3CN
- UCl3.6H2O
- UCl3.7H2O
மெத்தில் சயனைடில் உள்ள யுரேனியம்(IV) குளோரைடுடன் தேவையான அள் அவுக்குத் தண்ணீர் மற்றும் புரொப்பியானிக் அமிலம் சேர்த்து ஒவ்வொரு நீரேற்றையும் தயாரித்துக் கொள்ள முடியும்.[9]
பாதுகாப்பு[தொகு]
UCl3 இன் நீண்ட கால நச்சு விளைவுகள் குறித்த தரவுகள் இல்லையென்றாலும் அதிகமான அளவு பயன்படுத்துவதை இயன்ற அளவுக்கு தவிர்க்க வேண்டும்.
மற்ற கரையும் யுரேனியம் சேர்மங்களைப் போலவே UCl3 சேர்மமும் இரத்தத்தால் ஈர்க்கப்பட்டு சிறுநீரகம் நச்சடைவதற்கு வழிகோலுகிறது.[10]
மேற்கோள்கள்[தொகு]
- ↑ Serrano, K.; Taxil, P.; Dugne, O.; Bouvet, S.; Puech, E. J. Nucl. Mater. 2000, 282, 137–145.
- ↑ Remsen, Ira. Inorganic Chemistry. New York: Henry Holt and Company, 1890.
- ↑ Wells A.F. (1984) Structural Inorganic Chemistry 5th edition Oxford Science Publications பன்னாட்டுத் தரப்புத்தக எண் 0-19-855370-6
- ↑ Comey, Arthur M.; Hahn, Dorothy A. A Dictionary of Chemical Solubilities: Inorganic. New York: The MacMillan Company, 1921.
- ↑ Brenna, J.G.; Anderson, R.A.; Zalkin, A. Inorg. Chem. 1986, 25, 1756–1760.
- ↑ Le Marechal, J.F.; Ephritikhine, M.; Folcher, G. J. Organomet. Chem. 1986, 309, C1–C3.
- ↑ 7.0 7.1 Okamoto, Y.; Madden, P.; Minato, K. J. Nucl. Mater. 2005, 344, 109–114.
- ↑ Okamoto, Y.; Kobayashi, F.; Ogawa, T. J. Alloys Compd. 1998, 271, 355–358.
- ↑ Mech, A.; Karbowick, M.; Lis, T. Polyhedron. 2006, 25, 2083–2092.
- ↑ Bertell, Rosalie. "Gulf War Veterans and Depleted Uranium." May 1999. Available: http://ccnr.org/du_hague.html
புற இணைப்புகள்[தொகு]
- Uranium(III) chloride information at Webelements
- Uranium(III) chloride பரணிடப்பட்டது 2013-02-16 at Archive.today International Bio-Analytical Industries, Inc.
