மின்னாற்பகுப்பு

வேதியியல் மற்றும் உற்பத்தியில், மின்னாற்பகுப்பு (Electrolysis) என்பது மின்சாரத்தைப் பயன்படுத்தி தன்னிச்சையற்ற வேதியியல் மாற்றத்தை ஏற்படுத்துவதாகும். மின்னாற்பகுப்பு என்பது மின்னாற்பகுப்பு கலத்தைப் பயன்படுத்தி தாதுக்கள் போன்ற இயற்கையாகக் கிடைக்கும் மூலங்களிலிருந்து தனிமங்களைப் பிரிப்பதற்கான ஒரு முறையாக வணிக ரீதியாக முக்கியமானது.
வரலாறு[தொகு]
- 1800 ஆம் ஆண்டு – வில்லியம் நிக்கோல்சன் மற்றும் சோஃகன் ரிட்டர் இருவரும் நீரை ஐதரசன் மற்றும் ஆக்சிசன் என இரண்டு ஆக்கக்கூறுகளாகப் பிரித்தனர்.[1]
- 1807 ஆம் ஆண்டு – பொட்டாசியம், சோடியம், பேரியம், கால்சியம் மற்றும் மக்னீசியம் ஆகியவை சர் அம்ஃபிரி டேவி என்பவரால் மின்னாற்பகுப்பைப் பயன்படுத்திக் கண்டறியப்பட்டன.
- 1886 ஆம் ஆண்டு – என்றி மோய்சன் என்பவர் மின்னாற்பகுப்பைப் பயன்படுத்தி ஃப்ளூரினைக் கண்டறிந்தார்.[2]
- 1886 ஆம் ஆண்டு – ஃகால் ஃகெரௌல்ட்டின் செய்முறை அலுமினியத்தை உருவாக்குவதற்கான வழியை உருவாக்கியது.[3]
- 1890 ஆம் ஆண்டு – காஸ்ட்னெர்-கெல்லரின் செய்முறை சோடியம் ஐதராக்சைடை உருவாக்குவதற்கான வழியை உருவாக்கியது.
கண்ணோட்டம்[தொகு]
மின்னாற்பகுப்பு என்பது உருகிய அல்லது கரைக்கப்பெற்ற கரைப்பான் (ஒரு மின்பகுளி) வழியாக நேரடி மின்னோட்டத்தைச் செலுத்துவதன் மூலமாக, மின்முனைகளில் வேதிவினைகளை உருவாக்கி பொருட்களைச் சிதைக்கும் நிகழ்வு ஆகும்.
மின்னாற்பகுப்பை ஏற்படுத்துவதற்குத் தேவைப்படும் முக்கிய பகுதிப்பொருள்கள் பின்வருமாறு:
- இயங்கும் மின்துகள்களைக் கொண்ட திரவம் - மின்பகுளி
- வெளிப்புற ஆதாரமாக நேரடி மின்சாரம்
- மின்வாய்கள் எனப்படும் இரண்டு திடமான உலோகக் கம்பிகள் அல்லது தட்டுகள்
மின்னாற்பகுப்பு செய்முறையில் அந்தப் பகுதிப்பொருள்கள் பின்வரும் வேலைகளை மேற்கொள்கின்றன:
- திரவத்தில் (மின்பகுளி) இயங்கும் மின்துகள்கள் மின்சாரக் கடத்திகளாகச் செயல்படுகின்றன. ஒருவேளை திடமான உப்பைப் போன்று மின் துகள்கள் இயங்காவிட்டால், மின்னாற்பகுப்பை முழுமையாகப் பெற இயலாது.
- வெளியிலிருந்து அளிக்கப்படும் நேரடி மின்சாரமானது நீர்மம் அல்லது கரைசலில் மின்துகள்களை உருவாக்குவதற்குத் தேவையான ஆற்றலை அளிக்கிறது. வெளிப்புறச் சுற்றில் மின்சாரமானது மின்னணுவின் மூலம் கொண்டுசெல்லப்படுகிறது.
- மின்வாய்கள் இயற்பியல் சம்பந்தமான பிணைப்பை பின்வருவனவற்றிற்கு இடையில் ஏற்படுத்துகின்றன
- மின்னாற்பகுப்பை அடைவதற்கான ஆற்றலைத் தரும் மின்சுற்று
- பிரிக்க இயலும் மின்துகளிலான பகுதிப்பொருளைக் கொண்ட மின்பகுளி.
மின்வாய்கள் மின்சாரத்தை நிச்சயம் கடத்தும். மாழை (உலோகம்), காரீயம் மற்றும் குறைக்கடத்திபகுதிப்பொருள் ஆகியவற்றின் மின்வாய்கள் பெருமளவு பயன்படுத்தப்படுகின்றன. பொருத்தமான மின்வாயைத் தேர்ந்தெடுப்பது பின்வருவனவற்றைப் பொருத்தது:
- மின்வாய் மற்றும் மின்பகுளி ஆகியவற்றிற்கு இடையேயான வேதியியல் மாற்றம்
- மின்வாயைத் தயாரிப்பதற்கு ஆகும் செலவு
நடைமுறையில் மின்னாற்பகுப்பை அடைவதற்குப் பின்வரும் துணைப் பகுதிப்பொருள்கள் பயன்படுகின்றன:
- எதிர்விளைவுத் தூண்டிகள் மற்றும் விளைபொருள்கள் ஆகியவற்றை அளிப்பதற்கும், வைத்துக்கொள்வதற்கும் மற்றும் நீக்குவதற்குமான கொள்கலன்
- மின்சுற்று
மின்னாற்பகுப்பின் செய்முறை[தொகு]
மின்னாற்பகுப்பின் மிக முக்கியச் செய்முறையானது வெளிப்புறச் சுற்றிலிருந்து எலக்ட்ரான்களை நீக்குவது அல்லது சேர்ப்பதன் மூலம் அணுக்கள் மற்றும் மின்துகள்களை பரிமாற்றம் செய்வதாகும். மின்பகுளி மூலம் பெறப்படும் மின்னாற்பகுப்பின் இன்றியமையாத விளைபொருள்கள் நடைமுறையில் சில வேறுபட்ட நிலையைக் கொண்டுள்ளன என்பதுடன், அந்த விளைபொருள்கள் சில இயற்பியல் செய்முறைகளால் நீக்கம் செய்யப்படுகின்றன. உதாரணமாக, உவர் நீர் மின்னாற்பகுப்பில் உற்பத்தி செய்யப்படும் ஐதரசன் மற்றும் குளோரின் ஆகிய இரண்டு விளைபொருள்களும் வளிம வடிவத்திலானவை. மின்பகுளி மூலம் பெறப்படும் இத்தகைய வளிம விளைபொருள்களின் நீர்க்குமிழிகள் சேகரித்து வைக்கப்படுகின்றன.
இயங்கும் மின்துகள்களைக் (மின்பகுளி) கொண்ட நீர்மம் பின்வருவனவற்றால் உற்பத்தி செய்யப்படுகிறது
- இயங்கும் மின்துகள்களை உருவாக்குவதற்கு கரைப்பானுடன் (காடியைப் (அமிலத்தைப்) போன்ற) கூடிய மின்துகள் ஆக்கக்கூறுகளின் கரைப்பானேற்றம் அல்லது எதிர்விளைவு
- வெப்பத்தினால் மின்துகள்களாலான ஆக்கக்கூறை உருகவைப்பது (உருக்கும் முறை)
மின்பகுளியில் மூழ்கியுள்ள இரண்டு மின்வாய்களுக்குக் குறுக்கே மின் ஆற்றலானது செலுத்தப்படுகிறது.
மின்துகள்களை ஈர்க்கும் ஒவ்வொரு மின்வாயும் எதிர்மறையான மின்னேற்றத்தைக் கொண்டது. நேர்மறையான-மின்னேற்றம் பெற்ற மின்துகள்கள் (எதிர்மின்துகள்கள்) அணுக்களை-வழங்கும் (எதிர்மறையான) எதிர்மின்வாயை நோக்கி நகருகின்றன, அதேபோன்று எதிர்மறையான-மின்னேற்றம் பெற்ற மின்துகள்கள் (நேர்மின்துகள்கள்) நேர்மறையான நேர்மின்வாயை நோக்கி நகருகின்றன.
மின்வாய்களில், அணுக்கள் மற்றும் மின்துகள்களால் எதிர்மின்னிகள் உட்கிரகிக்கப்படுகின்றன அல்லது வெளியிடப்படுகின்றன. மின்னேற்றம் செய்யப்பெற்ற மின்துகள்களை எதிர்மின்னியில் அனுப்புவதற்கு அந்த அணுக்கள் எதிர்மின்னிகளைப் பெறுவதும் அல்லது இழப்பதுமாக இருக்கிறது. மின்பகுளியிலிருந்து மின்னேற்றம் பெறாத அணுக்களைப் பிரிப்பதற்கு அந்த மின்துகள்கள் எதிரமின்னிகளைப் பெறுவதும் அல்லது இழப்பதுமாக இருக்கின்றன. மின்துகள்களிலிருந்து மின்னேற்றம் பெறாத அணுக்களை உருவாக்குவது மின்னிறக்கம் எனப்படும்.
மின்துகள்களை மின்வாய்களாக மாற்றுவதற்கு ஆற்றல் தேவைப்படுகிறது என்பதுடன், மின்துகள்களின் நிலையில் மாற்றத்தை ஏற்படுத்துவதற்கு வெளிப்புற மின்னாற்றல் ஆதாரத்தின் மூலமாக வழங்கப்படுகிறது.
மின்வாய்களில் ஆக்சிசனேற்றம் மற்றும் ஆக்சிசனிறக்கம்[தொகு]
மின்துகள்களின் ஆக்சிசனேற்றம் அடைந்த அல்லது நடுநிலையான மூலக்கூறுகள் நேர்மின்வாயில் பெறப்படுகின்றன, அதே போன்று குறைக்கப்பெற்ற மின்துகள்கள் அல்லது நடுநிலையான மூலக்கூறுகள் எதிர்மின்வாயில் பெறப்படுகின்றன. உதாரணமாக, நேர்மின்வாயில் பெர்ரசு மின்துகள்களை பெர்ரிக் மின்துகள்களாக ஆக்சிசனேற்றம் செய்வது என்பது சாத்தியமானதாகும்.
- Fe2+
aq → Fe3+
aq + e–
எதிர்மின்வாயில் பெர்ரிசயனைடு மின்துகள்களை பெர்ரோசயனைடு மின்துகள்களாகக் குறைப்பது என்பது சாத்தியமானதாகும்:
- Fe(CN)3-
6 + e– → Fe(CN)4-
6
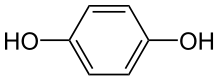
மேலும் நடுநிலையான மூலக்கூறுகள் மின்வாயில் எதிர்விளைவை உண்டாக்கலாம். உதாரணமாக: எதிர்மின்வாயில் பி-பென்சோகுயின் ஐதரோகுயினோனாகக் குறைக்கப்படுகிறது:
கடைசி எடுத்துக்காட்டில், H+ மின்துகள்களும் (ஐதரசன் மின்துகள்கள்) வினையில் பங்கெடுத்துக்கொள்கின்றன என்பதுடன், கரைசல்கள் அல்லது கரைப்பான்களில் (நீர், மெத்தனால் மற்றும் பல) மின்துகள்கள் காடியால் (அமிலத்தினால்) உருவாக்கப்படுகின்றன. மின்னாற்பகுப்பின் எதிர்விளைவுகளில் பங்குபெறும் H+ மின்துகள்கள் அனைத்தும் அமிலக் கரைசல்களில் நடுநிலையாகச் செயல்படுகின்றன. காரப்பொருள் கரைசல்களில் எதிர்விளைவுகளில் பங்குபெறும் OH- (ஹைட்ராக்ஸைடு மின்துகள்கள்) நடுநிலையானதாகும்.
ஆக்ஸிஜனேற்றம் செய்யப்பெற்ற அல்லது குறைக்கப்பெற்ற பகுதிப்பொருள்கள் கரைப்பானாக (வழக்கமாக நீர் பயன்படுகிறது) அல்லது மின்வாய்களாகப் பயன்படுகின்றன. இது வாயுக்களை உள்ளடக்கிய மின்னாற்பகுப்பைக் கொண்டுள்ளது.
மின்னாற்பகுப்பிற்கான பாரடேயின் விதிகள்[தொகு]
மின்னாற்பகுப்பின் முதல் விதி[தொகு]
மின்னாற்பகுப்பின் போது மின்வாயில் வெளிப்படும் பொருளின் நிறையானது (அல்லது பொருண்மை, m) மின்பகு நீர்மத்தின் வழியே பாயும் மின்னூட்டத்திற்கு (Q) நேர்த்தகவில் அமையும்.[4]
மின்னாற்பகுப்பின் இரண்டாம் விதி[தொகு]
ஒரே அளவு மின்னூட்டம் மின்பகு நீர்மங்களின் வழியே பாயும் போது அதனால் மின்வாய்களில் வெளிப்படும் பொருள்களின் நிறை (அல்லது பொருண்மை, m) அத்தனிமங்களின் வேதிய இணைமாற்றுக்கு (E) நேர்த்தகவில் அமையும்.
- m α E
தொழில்துறைப் பயன்பாடுகள்[தொகு]

- அலுமினியம், லித்தியம், சோடியம், பொட்டாசியம், மக்னீசியம் ஆகியவற்றைத் தயாரிப்பதற்கு மின்னாற்பகுப்பு பயன்படுகிறது.
- மின்னாற்பகுப்பைச் செயல்படுத்துவதற்குத் தேவைப்படும் மின்சாரத்தின் அளவை மதிப்பீடு செய்வதன் மூலம் மின்னாற்பகுப்பின் போது நிலைமாறிய கருப்பொருளின் அளவை கண்டறிவதற்கு மின்வேதியியல் தொழில்நுட்பத் திறன் பயன்படுகிறது.
- குளோரின் மற்றும் சோடியம் ஐதராக்சைடு ஆகியவற்றைத் தயாரிப்பதற்கு மின்னாற்பகுப்பு பயன்படுகிறது.
- சோடியம் குளோரேட் மற்றும் பொட்டாசியம் குளோரேட் ஆகியவற்றைத் தயாரிப்பதற்கு மின்னாற்பகுப்பு பயன்படுகிறது.
- டிரைஃப்ளூரோஅசிடிக் அமிலம் போன்ற ஃப்புளூரினேற்றம் செய்யப்பெற்ற கரிம ஆக்கக்கூறுகளைத் தயாரிப்பதற்கு மின்னாற்பகுப்பு பயன்படுகிறது.
- நேர்மின்வாயைப் போன்ற குறைந்த சுத்தத்திலான மெருகிடப்பட்ட காப்பரிலிருந்து எதிர்மின்வாயைப் போன்ற மின்பகுளிக் காப்பர் தயாரிக்க மின்னாற்பகுப்பு பயன்படுகிறது.
மின்னாற்பகுப்பு மற்ற பல பயன்பாடுகளைக் கொண்டுள்ளது:
- மின்முறை மாழையியல் என்பது மின்னாற்பகுப்பைப் பயன்படுத்தித் தூய வடிவத்திலான மாழைகளைப் பெறுவதற்கு உலோக ஆக்கக்கூறுகளிலிருந்து உலோகங்களைக் குறைக்கும் செய்முறையாகும். உதாரணமாக, சோடியம் ஐதராக்சைடில் அதன் உருகும் நிலையானது மின்னாற்பகுப்பினால் பிரிக்கப்பெற்று சோடியம் மற்றும் ஆக்ஸிஜனாக மாற்றப்படுகிறது என்பதுடன், இரண்டுமே முக்கியமான வேதியியல் பயன்பாடுகளைக் கொண்டுள்ளன. (அதே நேரத்தில் நீரானது உற்பத்தி செய்யப்படுகிறது.)
- நேர்மின்னாக்கம் என்பது உலோகங்களின் மேற்பரப்பை அரித்தலில் இருந்து தடுக்கும் மின்பகுளிச் செய்முறையாகும். உதாரணமாக, இந்தச் செய்முறையின் மூலம் கப்பல்கள் ஆக்சிசனால் நீரில் அரிக்கப்படுவதிலிருந்து பாதுகாக்கப்படுகிறது. மேலும் இந்தச் செய்முறையானது கப்பலின் மேற்பரப்பை அழகுபடுத்துவதற்குப் பயன்படுகிறது.
- மின்னாற்பகுப்பிற்கு எதிரான செய்முறையில் மின்கலம் பயன்படுத்தப்படுகிறது. லித்தியம் மின்பகுளியாகச் செயல்படுவதுடன், மின்ஆற்றலையும் அளிக்கிறது என ஹம்ப்ரி டேவி என்பவர் கண்டறிந்தார்.[சான்று தேவை]
- விண்வெளிக் கப்பல் மற்றும் அணுவாற்றலிலான நீர்மூழ்கிக் கப்பலில் ஆக்ஸிஜனை உற்பத்தி செய்வதற்கு மின்னாற்பகுப்பு பயன்படுகிறது.
- மின்முலாம் பூசுதல் என்பது உலோகங்களின் படலத்தில் அவற்றை வலுவூட்டுவதற்குப் பயன்படுகிறது. வாகன உடற்பகுதிகள் மற்றும் நிக்கல் நாணயங்களில் பயன்படுவதைப் போல, நடைமுறை மற்றும் ஒப்பனைத் திட்டங்களுக்காக பல்வேறு தொழிற்சாலைகளில் மின்முலாம் பூசுதலில் மின்னாற்பகுப்பு பயன்படுகிறது.
- எரிபொருளுக்காக, மலிவான ஆதாரத்திலான மின்னாற்றலைப் பயன்படுத்தி ஹைட்ரஜன் உற்பத்தி செய்யப்படுகிறது.
- இயந்திரக் கருவிகள் அல்லது கத்திகளைப் போன்று, உலோகத்தின் மேற்பரப்பில் நிலையான அடையாளம் அல்லது சின்னத்துடன் கூடிய மின்பகுளியாலான சித்திரங்களை உருவாக்குவதற்கு மின்னாற்பகுப்பு பயன்படுகிறது.
மின்னாற்பகுப்பு பழைய செயற்கைப் பொருள்களைத் தூய்மையாக்குதல் மற்றும் பாதுகாத்தலில் பயன்படுகிறது. மின்னாற்பகுப்பு உலோகம் அல்லாத துகள்களை உலோகத்திலிருந்து பிரித்தெடுக்கிறது என்பதுடன், பழைய நாணயங்கள் மற்றும் பெரிய பொருள்களைத் தூய்மையாக்குவதற்காகப் பயன்படுகிறது.
செய்முறை ஆய்வாளர்கள்[தொகு]
மின்னாற்பகுப்பின் அறிவியல் முன்னோடிகள் பின்வருமாறு:
- அந்துவான் இலவாசியே
- இராபர்ட் புன்சன்
- அம்பிரி டேவி
- மைக்கேல் ஃபாரடே
- பால் ஃகெரௌல்ட்
- சுவாந்தே அறீனியசு
- அடால்ப் வில்லெம் எர்மேன் கோல்ப்
- வில்லியம் நிக்கோல்சன்
- யோசப் லூயி கே-லூசாக்
- அலெக்சாண்டர் வான் அம்போல்ட்
- யோகன் வில்லெம் ஃகிட்டார்ஃப்
மின்கலங்களின் முன்னோடிகள்:
- அலெசான்றோ வோல்ட்டா
- கேஸ்டன் பிளான்டே
மேற்கோள்கள்[தொகு]
- ↑ Fabbri, Emiliana; Schmidt, Thomas J. (5 October 2018). "Oxygen Evolution Reaction—The Enigma in Water Electrolysis" (in en). ACS Catalysis 8 (10): 9765–9774. doi:10.1021/acscatal.8b02712.
- ↑ Wisniak, Jaime (2018-08-26). "Henri Moissan: The discoverer of fluorine". Educación Química 13 (4): 267. doi:10.22201/fq.18708404e.2002.4.66285. பன்னாட்டுத் தர தொடர் எண்:1870-8404. http://revistas.unam.mx/index.php/req/article/view/66285.
- ↑ "Paul Héroult and Charles M. Hall". Science History Institute (in ஆங்கிலம்). 1 June 2016.
- ↑ "The History of Electrochemistry: From Volta to Edison". ECS (in அமெரிக்க ஆங்கிலம்). பார்க்கப்பட்ட நாள் 2019-10-11.