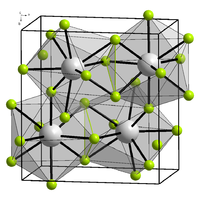
லியுதேத்தியம்(III) புளோரைடு
| |
| பெயர்கள் | |
|---|---|
| வேறு பெயர்கள்
லியுதேத்தியம் முப்புளோரைடு
| |
| இனங்காட்டிகள் | |
| 13760-81-1 | |
| ChemSpider | 75534 |
| EC number | 237-355-8 |
InChI
| |
| யேமல் -3D படிமங்கள் | Image |
| பப்கெம் | 83712 |
SMILES
| |
| பண்புகள் | |
| LuF3 | |
| வாய்ப்பாட்டு எடை | 231.97கி/மோல்[1] |
| தோற்றம் | வெண்மையான தூள்[2] |
| அடர்த்தி | 8.29 கி/செ.மீ3[3] |
| உருகுநிலை | 1,184[4] °C (2,163 °F; 1,457 K) |
| கொதிநிலை | 2200°செல்சியசு[5] |
| அறியப்படவில்லை[6] | |
| தீங்குகள் | |
| GHS pictograms |  
|
| GHS signal word | அபாயம் |
| H301, H311, H315, H319, H331, H335 | |
| P261, P264, P270, P271, P280, P301+310, P302+352, P304+340, P305+351+338, P311, P312, P321, P322, P330 | |
| தொடர்புடைய சேர்மங்கள் | |
| ஏனைய எதிர் மின்னயனிகள் | லியுதேத்தியம்(III) குளோரைடு இலூட்டீசியம்(III) புரோமைடு |
| ஏனைய நேர் மின்அயனிகள் | இசுக்காண்டியம்(III) புளோரைடு இட்ரியம்(III) புளோரைடு |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
| Infobox references | |
லியுதேத்தியம்(III) புளோரைடு (Lutetium(III) fluoride) என்பது LuF3.என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட ஒரு கனிம வேதியியல் சேர்மமாகும். லியுதேத்தியம் முப்புளோரைடு என்ற பெயராலும் இது அழைக்கப்படுகிறது.
தயாரிப்பு[தொகு]
லியுதேத்தியம் ஆக்சைடும் ஐதரசன் புளோரைடும் சேர்ந்து வினைபுரிவதால் அல்லது லியுதேத்தியம் குளோரைடு ஐதரோபுளோரிக் அமிலத்துடன் சேர்ந்து வினைபுரிவதால் லியுதேத்தியம்(III) புளோரைடு உருவாகிறது.:[7]
- Lu2O3 + 6 HF → 2 LuF3 + 3 H2O
- LuCl3 + 3 HF → LuF3 + 3 HCl
லியுதேத்தியம் சல்பைடும் ஐதரோபுளோரிக் அமிலத்துடன் சேர்ந்து வினைபுரிவதாலும் லியுதேத்தியம்(III) புளோரைடு உருவாகிறது:[8]
- 3 Lu2S3+ 20 HF + (2 + 2x) H2O → 2 (H3O)Lu3F10·xH2O↓ + 9 H2S↑ (x = 0.9)
- (H3O)Lu3F10 → 3 LuF3 + HF↑ + H2O↑
லியுதேத்தியம் ஆக்சைடு நைட்ரசன் முப்புளோரைடுடன் 240 பாகை செல்சியசு வெப்பநிலையில் வினைபுரிந்து லியுதேத்தியம் ஆக்சி புளோரைடு உருவாகிறது. 460 பாகை செல்சியசு வெப்பநிலைக்கு தொடர்ந்து சூடாக்கினால் லியுதேத்தியம் புளோரைடு கிடைக்கிறது:[9]
மேற்கோள்கள்[தொகு]
- ↑ "Lutetium Fluoride".
- ↑ "Lutetium Fluoride".
- ↑ "Lutetium Fluoride".
- ↑ K.M Lyapunov, A.V Baginskii, S.V Stankus (June 2004). "Experimental study of the enthalpy of lutetium trifluoride in solid and liquid states" (in en). Journal of Alloys and Compounds 372 (1–2): 7–9. doi:10.1016/j.jallcom.2003.09.139.
- ↑ "Lutetium Fluoride".
- ↑ "Lutetium Fluoride".
- ↑ Georg Brauer (ed.), In collaboration with Marianne Baudler u. a .: Handbook of Preparative Inorganic Chemistry. 3rd, revised edition. Volume I, Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6 , p. 254.
- ↑ O.V. Andrrev, I.A. Razumkova, A.N. Boiko (March 2018). "Synthesis and thermal stability of rare earth compounds REF 3 , REF 3 · n H 2 O and (H 3 O)RE 3 F 10 · n H 2 O (RE = Tb − Lu, Y), obtained from sulphide precursors" (in en). Journal of Fluorine Chemistry 207: 77–83. doi:10.1016/j.jfluchem.2017.12.001.
- ↑ Randall D. Scheele, Bruce K. McNamara, Andrew M. Casella, Anne E. Kozelisky, Doinita Neiner (February 2013). "Thermal NF3 fluorination/oxidation of cobalt, yttrium, zirconium, and selected lanthanide oxides" (in en). Journal of Fluorine Chemistry 146: 86–97. doi:10.1016/j.jfluchem.2012.12.013.
