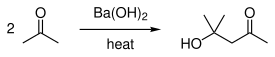
பேரியம் ஐதராக்சைடு

| |

| |
| இனங்காட்டிகள் | |
|---|---|
| 17194-00-2 22326-55-2 (ஒற்றை நீரேற்று) 12230-71-6 (எந்நீரேற்று) | |
| ChEBI | CHEBI:32592 |
| ChemSpider | 26408 |
Gmelin Reference
|
846955 |
| யேமல் -3D படிமங்கள் | Image |
| பப்கெம் | 28387 |
| வே.ந.வி.ப எண் | CQ9200000 |
SMILES
| |
| பண்புகள் | |
| Ba(OH)2 | |
| வாய்ப்பாட்டு எடை | 171.34 கிராம்/மோல் (நீரிலி) 189.355 கிராம்/மோல் (ஒற்றை நீரேற்று) 315.46 கிராம்/மோல் (எந்நீரேற்று) |
| தோற்றம் | வெண் திண்மம் |
| அடர்த்தி | 3.743 கிராம்/செ.மீ3 (ஒற்றை நீரேற்று) 2.18 கிராம்/செ.மீ3 (எந்நீரேற்று, 16 °செல்சியசில்) |
| உருகுநிலை | 78 °C (172 °F; 351 K) (எந்நீரேற்று) 300 °செல்சியசில் (ஒற்றை நீரேற்று) 407 °செல்சியசில் (நீரிலி) |
| கொதிநிலை | 780 °C (1,440 °F; 1,050 K) |
| BaO இன் நிறை (Ba(OH)2இல்லை): 1.67 கிராம்/100 மி.லி (0 °செல்சியசில்) 3.89 கிராம்/100 மி.லி (20 °செல்சியசில்) 4.68 கிராம்/100 மி.லி (25 °செல்சியசில்) 5.59 கிராம்/100 மி.லி (30 °செல்சியசில்) 8.22 கிராம்/100 மி.லி (40 °செல்சியசில்) 11.7 கிராம்/100 மி.லி (50 °செல்சியசில்) 20.94 கிராம்/100 மி.லி (60 °செல்சியசில்) 101.4 கிராம்/100 மி.லி (100 °செல்சியசில்) | |
| பிற கரைப்பான்கள்-இல் கரைதிறன் | குறைவு |
| காரத்தன்மை எண் (pKb) | 0.15 (first OH–), 0.64 (second OH–)[1] |
| -53.2•10−6 செ.மீ3/மோல் | |
| ஒளிவிலகல் சுட்டெண் (nD) | 1.50 (எந்நீரேற்று) |
| கட்டமைப்பு | |
| படிக அமைப்பு | எண்முகம் |
| வெப்பவேதியியல் | |
| Std enthalpy of formation ΔfH |
−944.7 கிலோயூல்/மோல் |
| தீங்குகள் | |
| ஈயூ வகைப்பாடு | தீங்கானது (Xn) |
| R-சொற்றொடர்கள் | R20/22 |
| S-சொற்றொடர்கள் | (S2), S28 |
| தீப்பற்றும் வெப்பநிலை | தீப்பற்றாது |
| தொடர்புடைய சேர்மங்கள் | |
| ஏனைய எதிர் மின்னயனிகள் | பேரியம் ஆக்சைடு பேரியம் பெராக்சைடு |
| ஏனைய நேர் மின்அயனிகள் | கால்சியம் ஐதராக்சைடு இசுட்ரோன்சியம் ஐதராக்சைடு |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
| | |
| Infobox references | |
பேரியம் ஐதராக்சைடு (Barium hydroxide) என்பது Ba(OH)2 என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட கனிம வேதியியல் சேர்மமாகும். Ba(OH)2(H2O)x என்ற பொதுவாய்ப்பாடு பேரியம் ஐதராக்சைடு நீரேற்றுகளைக் குறிக்கப் பயன்படுத்தப்படுகிறது. (x =1) என்ற மதிப்பைக் கொண்ட ஒற்றை நீரேற்று பேரைட்டா அல்லது பேரைட்டா-நீர் என்ற பெயரால் அழைக்கப்படுகிறது. பேரியத்தின் முதன்மையான சேர்மங்களில் இதுவும் ஒன்றாகும். வெண்மையான நிறத்திலுள்ள ஒற்றைநீரேற்று பேரியம் ஐதராக்சைடு மணிகள் வர்த்தக ரீதியான பயன்பாட்டில் உள்ளது.
தயாரிப்பும் கட்டமைப்பும்[தொகு]
பேரியம் ஆக்சைடை (BaO) தண்ணீரில் கரைப்பதால் பேரியம் ஐதராக்சைடு உருவாகிறது.
BaO + 9 H2O → Ba(OH)2•8H2O
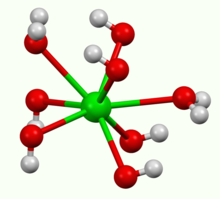
எண்நீரேற்றாக பேரியம் ஐதராக்சைடு படிகமாகிறது. இப்படிகங்களை வெற்றிடத்தில் 100 °செல்சியசு வெப்பநிலைக்கு சூடுபடுத்தினால் அவற்றை ஒற்றைநீரேற்று வடிவமாக மாற்ற இயலும். இவ்வொற்றை நீரேற்று பேரியம் ஆக்சைடாகவும் தண்ணீராகவும் மாறுகிறது[2]. ஒற்றை நீரேற்று வடிவ ஐதராக்சைடு அடுக்கமைப்பு முறையில் படத்தில் காட்டியுள்ளபடி படிகவடிவத்தை ஏற்கிறது.
Ba2+ மையங்கள் பட்டக எதிர் சதுர வடிவியலை ஏற்கின்றன. ஒவ்வொரு Ba2+ மையமும் இரண்டு தண்ணீர் ஈந்தணைவிகளுடனும் ஆறு ஐதராக்சைடு ஈந்தணைவிகளுடனும் பிணைக்கப்பட்டுள்ளன. இவை முறையே இரட்டையாகவும் மும்மடங்காகவும் அடுத்துள்ள Ba2+ மையமுடன் பாலமைக்கின்றன. எண்நீரேற்றைப் பொறுத்தவரை தனி Ba2+ மையங்கள் மீண்டும் எட்டு ஒருங்கிணைவுகள் அடைகின்றன ஆனால் ஈந்தனைவிகளுடன் பகிர்ந்துகொள்வதில்லை[3] In the octahydrate, the individual Ba2+ centers are again eight coordinate but do not share ligands.[4]
.
பயன்கள்[தொகு]
தொழிற்சாலைகளில் பேரியம் ஐதராக்சைடு மற்ற பேரியம் சேர்மங்கள் தயாரிப்பதற்குத் தேவையான முன்னோடிச் சேர்மமாகப் பயன்படுத்தப்படுகிறது. ஒற்றை நீரேற்று ஒரு நீர்நீக்கியாக பல்வேறு பொருள்களிலிருந்து சல்பேட்டை நீக்கப் பயன்படுகிறது. பேரியம் சல்பேட்டின் குறைந்த கரைதிறனை இச்செயல்பாடு வெளிப்படுத்துகிறது. இத்தொழிற்சாலை செயல்முறை ஆய்வகப் பயன்பாட்டிலும் பயன்படுத்தப்படுகிறது.
ஆய்வகப் பயன்கள்[தொகு]
பலவீனமான அமிலங்களை குறிப்பாக கரிம அமிலங்களை தரம்பார்க்க உதவும் பகுப்பாய்வு வேதியியலில் பேரியம் ஐதராக்சைடு பயன்படுத்தப்படுகிறது. சோடியம் ஐதராக்சைடு, பொட்டாசியம் ஐதராக்சைடுகளில் கார்பனேட்டு கரைந்திருப்பதைப் போல அல்லாமல் நீர்த்த பேரியம் ஐதராக்சைடு கரைசலை உத்தரவாதமாக கார்பனேட்டு இல்லாத கரைசல் எனக் கூறமுடியும். ஏனெனில் பேரியம் கார்பனேட்டு நீரில் கரையாது. இதனால் பினாப்தலீன், தைமால்ப்தலீன் போன்ற நிறங்காட்டிகளைப் பயன்படுத்தி தரம்பார்க்கும்போது கார்பனேட்டு அயனிகள் இருப்பதால் தரம்பார்த்தல் பிழைகள் தவிர்க்கப்படுகின்றன [5].. பேரியம் ஐதராக்சைடு அவ்வப்போது கரிமத் தொகுப்பு வினைகளில் வலிமையான காரமாகப் பயன்படுத்தப்படுவதுண்டு. எசுத்தர்கள்[6] மற்றும் நைட்ரைல்களின்[7][8][9] நீராற்பகுப்பு வினை, ஆல்டால் குறுக்க வினையில் ஒரு காரமாகப் பயன்படுவது போன்றவை உதாரணங்களாகும்.
டைமெத்தில் எண்டெக்கேண்டையோயேட்டில் உள்ள இரண்டு சமான எசுத்தர் குழுக்களில் ஒன்றை நீராற்பகுக்கவும் பேரியம் ஐதராக்சைடு பயன்படுத்தப்படுகிறது [10]. இதேபோல அமினோ அமிலங்களை கார்பாக்சில் நீக்கம் செய்து பேரியம் கார்பனேட்டை விடுவிக்கும் செயல்முறை வினைகளிலும் பேரியம் ஐதராக்சைடு பயன்படுத்தப்படுகிறது [11].
மேலும், சைக்ளோபெண்டனோன் [12], டையசிட்டோன் ஆல்ககால் [13], டி-குளுக்கோனிக் γ-லாக்டோன் [14] போன்றவற்றை தயாரிப்பதிலும் பேரியம் ஐதராக்சைடு பயன்படுத்தப்படுகிறது.
வினைகள்[தொகு]
800 °செல்சியசு வெப்பநிலைக்கு சூடாக்கும்போது பேரியம் ஐதராக்சைடு பேரியம் ஆக்சைடாகச் சிதைவடைகிறது. கார்பன் டை ஆக்சைடுடன் வினைபுரிகையில் பேரியம் கார்பனேட்டைக் கொடுக்கிறது. நீர்த்த கரைசலில் உயர் காரமாகச் செயல்பட்டு அமிலங்களுடன் நடுநிலையாக்கல் வினைகளில் ஈடுபடுகிறது. இதனால் முறையே கந்தக அமிலத்துடன் வினைபுரிந்து பேரியம் சல்பேட்டும், பாசுபாரிக் அமிலத்துடன் வினைபுரிந்து பேரியம் பாசுப்பேட்டும் உருவாகின்றன.ஐதரசன் சல்பைடுடன் பேரியம் ஐதராக்சைடு வினைபுரியும்போது பேரியம் சல்பைடு தோன்றுகிறது. கரையாத அல்லது குறைவாகக் கரையக்கூடிய பேரியம் உப்புகளின் வீழ்படிவுகள் இரட்டை இடப்பெயர்ச்சி வினைகளின் விளைவாகத் தோன்றுகின்றன. மற்ற உலோக உப்புகளின் கரைசல்கள் பேரியம் ஐதராக்சைடின் நீரிய கரைசலுடன் கலக்கும்போது இத்தகைய இரட்டை இடப்பெயர்ச்சி வினைகள் நிகழ்கின்றன[15]
அமோனியம் உப்புகளுடன் பேரியம் ஐதராக்சைடு ஈடுபடும் வினைகள் வலிமையான வெப்பங்கொள் வினைகளாகும். எந்நீரேற்று பேரியம் ஐதராக்சைடு அமோனியம் குளோரைடுடன்[16][17] or[18] ஈடுபடும் வினை அல்லது அமோனியம் தயோசயனேட்டுடன்[18][19] ஈடுபடும் வினை மாணவர்களுக்கு வகுப்பறையில் செய்து காட்டப் பயன்படும் செயல்விளக்க வினையாகப் பயன்படுகிறது. இவ்வினையயின் மூலம் தண்ணீரை உறையவைக்கத் தேவையான வெப்பம் இவ்வினையில் தோன்றுவதை விளக்க முடிகிறது.
பாதுகாப்பு[தொகு]
வலிமையான காரங்களைப் பயன்படுத்துகையில் கடைபிடிக்கவேண்டிய அனைத்து நடவடிக்கைகளும் இதற்கும் பொருந்தும். மேலும் நீரில் கரையும் மற்ற பேரியம் உப்புகளுக்கான முன்னெச்சரிக்கைகள் இதற்கும் தேவையாகும்.
இதையும் காண்க[தொகு]
மேற்கோள்கள்[தொகு]
- ↑ "Sortierte Liste: pKb-Werte, nach Ordnungszahl sortiert. - Das Periodensystem online" (in ஜெர்மன்).
- ↑ (1960). Gmelins Handbuch der anorganischen Chemie (8. Aufl.), Weinheim: Verlag Chemie, p. 289.
- ↑ Kuske, P.; Engelen, B.; Henning, J.; Lutz, H.D.; Fuess, H.; Gregson, D. "Neutron diffraction study of Sr(OH)2(H2O) and beta-Ba(OH)2*(H2O)" Zeitschrift für Kristallographie (1979-2010) 1988, vol. 183, p319-p325.
- ↑ Manohar, H.; Ramaseshan, S. "The crystal structure of barium hydroxide octahydrate Ba (OH)2(H2O)8" Zeitschrift für Kristallographie, Kristallgeometrie, Kristallphysik, Kristallchemie 1964. vol. 119, p357-p374
- ↑ வார்ப்புரு:VogelQuantitative
- ↑ Meyer, K.; Bloch, H. S. (1945). "Naphthoresorcinol". Org. Synth. 25: 73; Coll. Vol. 3: 637.
- ↑ Brown, G. B. (1946). "Methylsuccinic acid". Org. Synth. 26: 54; Coll. Vol. 3: 615.
- ↑ Ford, Jared H. (1947). "β-Alanine". Org. Synth. 27: 1; Coll. Vol. 3: 34.
- ↑ Anslow, W. K.; King, H.; Orten, J. M.; Hill, R. M. (1925). "Glycine". Org. Synth. 4: 31; Coll. Vol. 1: 298.
- ↑ Durham, L. J.; McLeod, D. J.; Cason, J. (1958). "Methyl hydrogen hendecanedioate". Org. Synth. 38:55; Coll. Vol. 4:635.
- ↑ [1]
- ↑ Thorpe, J. F.; Kon, G. A. R. (1925). "Cyclopentanone". Org. Synth. 5: 37; Coll. Vol. 1: 192.
- ↑ Conant, J. B.; Tuttle, Niel. (1921). "Diacetone alcohol". Org. Synth. 1: 45; Coll. Vol. 1: 199.
- ↑ Karabinos, J. V. (1956). "γ-lactone". Org. Synth. 36: 38; Coll. Vol. 4: 506.
- ↑ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 0-07-049439-8
- ↑ "Endothermic Reactions of Hydrated Barium Hydroxide and Ammonium Chloride". UC San Diego. பார்க்கப்பட்ட நாள் 2 April 2014.
- ↑ Endothermic Solid-Solid Reactions
- ↑ 18.0 18.1 Camp, Eric. "Endothermic Reaction". Univertist of Washington. Archived from the original on 10 சனவரி 2020. பார்க்கப்பட்ட நாள் 2 April 2014.
- ↑ "Endothermic solid-solid reactions" (PDF). Classic Chemistry Demonstrations. The Royal Society of Chemistry. Archived from the original (PDF) on 7 April 2014. பார்க்கப்பட்ட நாள் 2 April 2014.