பெரிலியம் நைட்ரைடு
| |
| இனங்காட்டிகள் | |
|---|---|
| 1304-54-7 | |
| பண்புகள் | |
| Be3N2 | |
| வாய்ப்பாட்டு எடை | 55.06 கி/மோல் |
| தோற்றம் | மஞ்சள் அல்லது வெண்மை துகள் |
| அடர்த்தி | 2.71 கி/செ.மீ3 |
| உருகுநிலை | 2,200 °C (3,990 °F; 2,470 K) |
| கொதிநிலை | 2,240 °C (4,060 °F; 2,510 K) (சிதைவடையும்) |
| சிதைவடையும் | |
| [[அமிலங்கள், காரங்கள்]]-இல் கரைதிறன் | நீராற்பகுப்பு அடையும் |
| கட்டமைப்பு | |
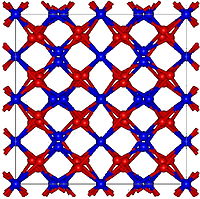
| படிக அமைப்பு | கனசதுரம், cI80, இடக்குழு = Ia-3, No. 106 (α வடிவம்) |
| தீங்குகள் | |
| அமெரிக்க சுகாதார ஏற்பு வரம்புகள்: | |
அனுமதிக்கத்தக்க வரம்பு
|
நேரக் கணக்கீட்டு சராசரி 0.002 மி.கி/மீ3 C 0.005 மி.கி/மீ3 (30 நிமிடங்கள்), அதிகபட்ச உயர்வுடன் 0.025 மி.கி/மி3 (Be ஆக)[1] |
பரிந்துரைக்கப்பட்ட வரம்பு
|
Ca C 0.0005 மி.கி/மி3 (Be ஆக)[1] |
உடனடி அபாயம்
|
Ca [4 மி.கி/மீ3 (Be ஆக)][1] |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
பெரிலியம் நைட்ரைடு (Beryllium nitride) என்பது Be3N2,என்ற மூலக்கூறு வாய்ப்பாடு கொண்ட பெரிலியம் தனிமத்தின் நைட்ரைடு உப்பு ஆகும். பகுதிப்பொருள்களாக உள்ள பெரிலியம் மற்றும் நைட்ரசன் தனிமங்களில் இருந்து உயர் வெப்பநிலையில் (1100 முதல் 1500 0 செ)[2] பெரிலியம் நைட்ரைடு தயாரிக்க முடியும். பெரிலியம் அசைடு போலில்லாமல் பெரிலியம் நைட்ரைடு வெற்றிடத்திலேயே சிதைவடைந்து பெரிலியம் மற்றும் நைட்ரசனைக் கொடுக்கிறது.[2] மேலும் இது விரைவாக நீராற்பகுப்பு அடைந்து பெரிலியம் ஐதராக்சைடு மற்றும் அமோனியாவைக்[2] கொடுக்கிறது. கனசதுர α-Be3N2 வடிவுடன் சிதைவுற்ற புளோரைட்டு எதிர் அமைப்பு மற்றும் அறுகோண β-Be3N2[2] ஆகிய பல்லுருத் தோற்றங்களில் பெரிலியம் நைட்ரைடு காணப்படுகிறது. 1800 முதல் 1900 0 செல்சியசு வெப்பநிலையில், அமோனியா வாயுப் பாய்ச்சலில் சிலிக்கான் நைட்ரைடுடன் (Si3N4 ) வினைபுரிந்து BeSiN2 சேர்மத்தைத் தருகிறது.[2]
தயாரிப்பு
[தொகு]700 முதல் 1400 0 செல்சியசு வெப்பநிலையில் பெரிலியம் உலோகத் தூளை ஆக்சிசனற்ற சூழலில் உலர் நைட்ரசனுடன் வினைபுரியச் செய்வதன் மூலம் பெரிலியம் நைட்ரைடைத் தயாரிக்கலாம்.
பயன்கள்
[தொகு]வெப்பந்தாங்கும் பீங்கான் தயாரிப்பில்[3], அணுக்கரு உலைகளில், மற்றும் கதிரியக்கக் கார்பன் – 14 உற்பத்தியில் பெரிலியம் நைட்ரைடு பெரிதும் பயன்படுகிறது.
வினைகள்
[தொகு]கனிம அமிலங்களுடன் பெரிலியம் நைட்ரைடு வினை புரிந்து அமோனியாவையும் அமிலத்துடன் தொடர்புடைய உப்புகளையும் உருவாக்குகிறது.
- Be3N2 + 6 HCl → 3 BeCl2 + 2 NH3
காரக் கரைசல்களுடன் வினைபுரியும் போது ஒரு பெரிலேட்டை உருவாக்கி அமோனியாவை வெளியேற்றுகிறது.
- Be3N2 + 6 NaOH → 3 Na2BeO2 + 2 NH3
அமிலங்கள் மற்றும் காரங்களுடன் வினைபுரியும் போது தீவிரத்துடனும் வேகத்துடனும் நடைபெறும் வினைகள் தண்ணீருடன் வினைபுரியும் போது மெதுவாக நிகழ்கிறது.
- Be3N2 + 6 H2O → 3 Be(OH)2 + 2 NH3
ஆக்சிசனேற்றிகளுடன் வினைபுரியும் போது வேதிவினையானது அதிதீவிரமாக நடைபெறுகிறது. 0 செல்சியசு வெப்பநிலையில் பெரிலியம் நைட்ரைடு காற்றில் ஆக்சிசனேற்றம் அடைகிறது.
மேற்கோள்கள்
[தொகு]- ↑ 1.0 1.1 1.2 "NIOSH Pocket Guide to Chemical Hazards #0054". National Institute for Occupational Safety and Health (NIOSH).
- ↑ 2.0 2.1 2.2 2.3 2.4 Egon Wiberg, Arnold Frederick Holleman (2001) Inorganic Chemistry, Elsevier பன்னாட்டுத் தரப்புத்தக எண் 0-12-352651-5
- ↑ Hugh O. Pierson, 1996, Handbook of Refractory Carbides and Nitrides: Properties, Characteristics, Processing, and Applications, William Andrew Inc.,பன்னாட்டுத் தரப்புத்தக எண் 0-8155-1392-5
