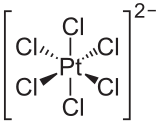பிளாட்டினம்: திருத்தங்களுக்கு இடையிலான வேறுபாடு
சி தானியங்கி உதவியுடன் செய்த குழப்பச்சீரமைப்பு: வெள்ளி - link(s) தொடுப்புகள் வெள்ளி (தனிமம்) உக்கு மாற்றப்பட்டன |
No edit summary |
||
| வரிசை 69: | வரிசை 69: | ||
{{Elementbox_footer | color1=#ffc0c0 | color2=black }} |
{{Elementbox_footer | color1=#ffc0c0 | color2=black }} |
||
'''பிளாட்டினம்''' (இலங்கை வழக்கு, '''பிளாத்தினம்''') ([[ஆங்கிலம்]]: Platinum) என்பது '''Pt''' என்னும் வேதியியல் குறியீடு கொண்ட ஒரு வேதியியல் [[தனிமம்]]. [[அணுவெண்]] 78 கொண்ட |
'''பிளாட்டினம்''' (இலங்கை வழக்கு, '''பிளாத்தினம்''') ([[ஆங்கிலம்]]: Platinum) என்பது '''Pt''' என்னும் வேதியியல் குறியீடு கொண்ட ஒரு வேதியியல் [[தனிமம்]]. [[அணுவெண்]] 78 கொண்ட இத்தனிமம் தனிம அட்டவணையில் 10 ஆவது நெடுங்குழுவில் உள்ளது. இதன் [[அணுக்கரு]]வில் 117 [[நொதுமி]]கள் உள்ளன. இது தட்டி கொட்டி நெளியக் கூடிய, வளையக்க்கூடிய, பளபளப்பேறும் வெண் சாம்பல் நிறமுடைய [[மாழை]] (உலோகம்) ஆனால் எடை மிகுந்த ஒரு மாழை. இது பிறழ்வரிசை மாழை இனத்தைச் சேர்ந்த தனிமம். [[தங்கம்]] போலவே விலை உயர்ந்த நகை அணிகள் செய்யப் பயன்படுகின்றது.பிளாட்டினம் தங்கத்தை விட நூறுமடங்கு மதிப்பு மிக்க மாழை ஆகும். மின் கருவிகளில் உறுதியான மின்னிணைப்புதரும் மின் முனைகளாகவும், [[தானுந்து]]களில் இருந்து வெளியேறும் கழிவு [[வளிமம்|வளிமங்களில்]] உள்ள, சுற்றுச் சூழலுக்குத் தூய்மைக்கேடு விளைவிக்கும் கார்பன் மோனாக்ஸைடு (CO), நைதரசன் ஆக்சைடு போன்ற வளிமங்களை நச்சுத்தனமை குறைந்த வளிமங்களாக மாற்றவும் பிளாட்டினம் பயன்படுகின்றது. அனைத்துலக பங்குச்சந்தையில் வாங்கி-விற்கும் பொருளாகப் பயன்படுகையில் பிளாட்டினத்தின் [[ISO பணக் குறியீடு|ISO குறியீடு]] XPT என்பதாகும். |
||
== குறிப்பிடத்தக்க பண்புகள் == |
== குறிப்பிடத்தக்க பண்புகள் == |
||
10:10, 30 திசம்பர் 2020 இல் நிலவும் திருத்தம்
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| பொது | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| பெயர், குறி எழுத்து, தனிம எண் |
பிளாட்டினம், Pt, 78 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| வேதியியல் பொருள் வரிசை |
தாண்டல் உலோகங்கள்s | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| நெடுங்குழு, கிடை வரிசை, வலயம் |
10, 6, d | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| தோற்றம் | சாம்பல் வெள்ளை 
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| அணு நிறை (அணுத்திணிவு) |
195.084(9) g/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| எதிர்மின்னி அமைப்பு |
[Xe] 4f14 5d9 6s1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| சுற்றுப் பாதையிலுள்ள எதிர்மின்னிகள் (எலக்ட்ரான்கள்) |
2, 8, 18, 32, 17, 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| இயல்பியல் பண்புகள் | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| இயல் நிலை | திண்மம் | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| அடர்த்தி (அறை வெ.நி அருகில்) |
21.45 கி/செ.மி³ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| உருகுநிலையில் நீர்மத்தின் அடர்த்தி |
19.77 g/cm³ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| உருகு வெப்பநிலை |
2041.4 K (1768.3 °C, 3214.9 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| கொதி நிலை | 4098 K (3825 °C, 6917 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| நிலை மாறும் மறை வெப்பம் |
22.17 கி.ஜூ/மோல் (kJ/mol) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| வளிமமாகும் வெப்ப ஆற்றல் |
469 கி.ஜூ/மோல் | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| வெப்பக் கொண்மை |
(25 °C) 25.86 ஜூ/(மோல்·K) J/(mol·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| அணுப் பண்புகள் | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| படிக அமைப்பு | cubic face centered | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ஆக்சைடு நிலைகள் |
1, 2, 3, 4, 5, 6 (மென் கார ஆக்ஸைடு) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| எதிர்மின்னியீர்ப்பு | 2.28 (பௌலிங் அளவீடு) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| அயனாக்க ஆற்றல் | 1st: 870 கிஜூ/மோல் | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2nd: 1791 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| அணு ஆரம் | 135 பிமீ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| அணுவின் ஆரம் (கணித்) |
177 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| கூட்டிணைப்பு ஆரம் | 128 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| வான் டெர் வால் ஆரம் |
175 பி.மீ (pm) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| வேறு பல பண்புகள் | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| காந்த வகை | paramagnetic | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| மின் தடைமை | (20 °C) 105 nΩ·m | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| வெப்பக் கடத்துமை |
(300 K) 71.6 வாட்/(மீ·கெ) W/(m·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| வெப்ப நீட்சி | (25 °C) 8.8 மைக்.மீ/(மி.மீ·கெ) µm/(m·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ஒலியின் விரைவு (மென் கம்பி) |
(அறை வெ.நி) 2800 மீ/நொ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| யங்கின் மட்டு | 168 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Shear modulus | 61 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| அமுங்குமை | 230 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| பாய்சான் விகிதம் | 0.38 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| மோவின்(Moh's) உறுதி எண் | 4–4.5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| விக்கர் உறுதிஎண் Vickers hardness |
549 MPa (மெகாபாஸ்) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| பிரிநெல் உறுதிஎண் Brinell hardness]] |
392 MPa (மெகாபாஸ்) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS பதிவெண் | 7440-06-4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| குறிபிடத்தக்க ஓரிடத்தான்கள் | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| மேற்கோள்கள் | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
பிளாட்டினம் (இலங்கை வழக்கு, பிளாத்தினம்) (ஆங்கிலம்: Platinum) என்பது Pt என்னும் வேதியியல் குறியீடு கொண்ட ஒரு வேதியியல் தனிமம். அணுவெண் 78 கொண்ட இத்தனிமம் தனிம அட்டவணையில் 10 ஆவது நெடுங்குழுவில் உள்ளது. இதன் அணுக்கருவில் 117 நொதுமிகள் உள்ளன. இது தட்டி கொட்டி நெளியக் கூடிய, வளையக்க்கூடிய, பளபளப்பேறும் வெண் சாம்பல் நிறமுடைய மாழை (உலோகம்) ஆனால் எடை மிகுந்த ஒரு மாழை. இது பிறழ்வரிசை மாழை இனத்தைச் சேர்ந்த தனிமம். தங்கம் போலவே விலை உயர்ந்த நகை அணிகள் செய்யப் பயன்படுகின்றது.பிளாட்டினம் தங்கத்தை விட நூறுமடங்கு மதிப்பு மிக்க மாழை ஆகும். மின் கருவிகளில் உறுதியான மின்னிணைப்புதரும் மின் முனைகளாகவும், தானுந்துகளில் இருந்து வெளியேறும் கழிவு வளிமங்களில் உள்ள, சுற்றுச் சூழலுக்குத் தூய்மைக்கேடு விளைவிக்கும் கார்பன் மோனாக்ஸைடு (CO), நைதரசன் ஆக்சைடு போன்ற வளிமங்களை நச்சுத்தனமை குறைந்த வளிமங்களாக மாற்றவும் பிளாட்டினம் பயன்படுகின்றது. அனைத்துலக பங்குச்சந்தையில் வாங்கி-விற்கும் பொருளாகப் பயன்படுகையில் பிளாட்டினத்தின் ISO குறியீடு XPT என்பதாகும்.
குறிப்பிடத்தக்க பண்புகள்
பிளாட்டினம் ஓர் உறுதியான மாழை ஆகும்.காற்றிலும், வெப்பமான சூழலிலும் இது மாசடையாமல் ஜொலிக்கும் தன்மை உடையது.தங்கத்தை கரைக்கும் பாதரசம்(Mercury), நைட்ரிக் அமிலம், அமிலங்களின் அரசனான கந்தக அமிலம் ஆகியவற்றால் கூட பிளாட்டினத்தை அரிக்க முடியாது.எனவே பிளாட்டினம் வேதி-வினைகளை ஊக்குவிக்கும் பொருளாக பயன்படுகிறது.
தூய பொருளாக இருக்கும் பொழுது இம் மாழை வெண் சாம்பல் நிறமுடையது. இம்மாழை எளிதில் அரிக்கப் படாத ஒரு பொருள். பிளாட்டினக்குழு என்று கூறப்படும் பிளாட்டினம், ரூத்தேனியம், ரோடியம், பலேடியம், ஆசுமியன், இரிடியம் ஆகிய ஆறு மாழைகளும் (இவை ஆறு பிளாட்டினக் குடும்ப மாழைகள் என்று கூறப்படுகின்றது), மிகச்சிறந்த வேதி வினையூக்கிகளாகப் பயன்படுகின்றன. பிளாட்டினம் தானுந்துகளில் கழிவுக் குழாய் வழியாக வெளியேறும் நச்சு வளிமங்களை மாற்றும் வினையூக்கியாகப் பயன்படுகின்றது. உள் எரி பொறிகளின் உந்தறையில் அழுத்தமுறும் எரிவளியை எரியூட்டுவதற்குப் பயன்படும் மின் தீப்பொறி உண்டாக்கும் மின்குச்சிகளிலும் (spark plug) பயன்படுகின்றது.
பிளாட்டினத்தின் பொதுவான ஆக்ஸிஜன் நிலைகள் +2 , +4 ஆகும். ஆனால் +1 மற்றும் +3 நிலைகள் அதிகம் காணப்படாத நிலைகள.
சேர்மங்கள்
எக்சாகுளோரோபிளாட்டினிக் அமிலம் அல்லது அறுகுளோரோபிளாட்டினிக் அமிலம் பிளாட்டினத்தின் மிக முக்கியமான சேர்மமாகும். பல பிளாட்டினம் சேர்மங்கள் தயாரிப்பதற்கு இது ஒரு முன்னோடி சேர்மமாக உள்ளது. நிழற் படக்கலையில், துத்தநாக அரிப்பைத் தடுப்பதில், அழியா மை தயாரிப்பு, கண்ணாடிகளுக்கு முலாம் பூச, பீங்கான்களுக்கு நிறமிட, ஒரு வினையூக்கியாக என்று பிளாட்டினம் பல்வேறு பயன்களைக் கொண்டுள்ளது[1]. எக்சாகுளோரோபிளாட்டினேட்டை அமோனியம் குளோரைடு போன்ற ஓர் அமோனியம் உப்புடன் சேர்த்து சூடாக்கும் போது அமோனியம் எக்சாகுளோரோபிளாட்டினேட்டு உருவாகிறது[2]. இது ஒப்பீட்டளவில் எந்த அமோனியம் கரைசல்களிலும் கரையாது. ஐதரசன் முன்னிலையில் இந்த அமோனியம் உப்பை சூடுபடுத்தினால் இந்த உப்பு ஒடுக்கமடைந்து தனிமநிலை பிளாட்டினம் உருவாகிறது. பொட்டாசியம் எக்சாகுளோரோபிளாட்டினேட்டு இதே போல கரையாது. எடையளவியலில் பொட்டாசியம் அயனிகளை உறுதிப்படுத்த எக்சாகுளோரோபிளாட்டிக் அமிலம் பயன்படுத்தப்படுகிறது[3]. எக்சாகுளோரோபிளாட்டினிக் அமிலத்தை வெப்பப்படுத்தினால் அது பிளாட்டினம்(IV) குளோரைடு மற்றும் பிளாட்டினம்(II) குளோரைடுகள் வழியாக தனிமநிலை பிளாட்டினமாக சிதைவடைகிறது. இருப்பினும் இவ்வினை படிநிலைகளாக நிகழ்வதில்லை.
- (H3O)2PtCl6•nH2O
 PtCl4 + 2 HCl + (n + 2) H2O
PtCl4 + 2 HCl + (n + 2) H2O - PtCl4
 PtCl2 + Cl2
PtCl2 + Cl2 - PtCl2
 Pt + Cl2
Pt + Cl2
இம்மூன்று வினைகளும் மீள் வினைகளாகும். ம். பிளாட்டினம் (II) மற்றும் பிளாட்டினம் (IV) புரோமைடுகள் நன்கு அறியப்படுகின்றன. பிளாட்டினம் எக்சாபுளோரைடு ஒரு வலிமையான ஆக்சிசனேற்றியாகும். இது ஆக்சிசனையும் ஆக்சிசனேற்றம் செய்யக் கூடிய வலிமை மிக்கது ஆகும்.
ஆடம்சு வினையூக்கி என்று அழைக்கப்படும் பிளாட்டினம்(IV) ஆக்சைடு ( PtO2) கருப்பு நிறத்தில் தூளாக உள்ளது. இது பொட்டாசியம் ஐதராக்சைடு கரைசலிலும் அடர்த்தியான அமிலங்களிலும் கரைகிறது. பிளாட்டினம் டை ஆக்சைடு, பிளாட்டினம் ஆக்சைடு இரண்டும் வெப்பப்படுத்தும் போது சிதைவடைகின்றன. பிளாட்டினம்(II, IV) ஆக்சைடு உருவாகிறது.
- 2 Pt2+ + Pt4+ + 4 O2− → Pt3O4
இதர சேர்மங்கள்
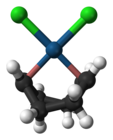
பல்லேடியம் அசிட்டேட்டு சேர்மம் போலில்லாமல் பிளாட்டினம்(II) அசிட்டேட்டு வணிக ரீதியாக கிடைப்பதில்லை. ஒரு காரம் தேவைப்பட்டால், சோடியம் அசிடேட்டுடன் இதனுடைய ஆலைடுகள் இணைத்து பயன்படுத்தப்படுகின்றன. பிளாட்டினம்(II) அசிட்டைலசிட்டோனேட்டும் இதே முறையில் பயன்படுத்தப்படுகிறது [4]. பல பேரியம் பிளாட்டினைடுகள் தொகுப்புமுறையில் தயாரிக்கப்பட்டன, இதில் பிளாட்டினம் -1 முதல் -2 வரையிலான எதிர்மறை ஆக்சிசனேற்ற நிலைகளில் உள்ளது. BaPt, Ba3Pt2, மற்றும் Ba2Pt உள்ளிட்டவை இதில் அடங்கும். Cs2Pt, என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட சீசியம் பிளாடினைடு அடர் சிவப்பு நிறத்தில் ஒளி ஊடுறுவும் படிகமாகக் காணப்படுகிறது. இச்சேர்மத்தில் Pt2− எதிர்மின் அயனிகள் காணப்படுகின்றன. மின்வேதியியல் முறைபடி ஒடுக்கப்பட்ட மேற்பரப்புகளிலும் பிளாட்டினம் எதிர்மறை ஆக்சிசனேற்ற நிலையைக் கொண்டுள்ளது. உலோக வகை தனிமங்கள் எதிர்மறை ஆக்சிசனேற்ற நிலையில் இருப்பது வழக்கத்திற்கு மாறானதாகும். எத்திலின் ஈந்தனைவியைக் கொண்டுள்ள செய்செசு உப்பு முதலாவதாக கண்டுபிடிக்கப்பட்ட கரிம உலோகச் சேர்மங்களில் ஒன்றாகும். டைகுளோரோ(சைக்ளோ ஆக்டா1,5-டையீன்)பிளாட்டினம்(II) வர்த்தக முறையில் கிடைக்கின்ற ஒலிபீன் அணைவுச் சேர்மமாகும். எளிதில் இடம்பெயரச்செய்கின்ற ஈந்தனைவிகளை இது (1,5-சைக்ளோ ஆக்டா டையீன்) பெற்றுள்ளது. இந்த அணைவுச் சேர்மமும் ஆலைடுகளும் பிளாட்டின வேதியியலின் கொடக்கப் புள்ளிகளாகக் கருதப்படுகின்றன.
சிசுபிளாட்டின் அல்லது சிசு-டையமீன்டைகுளோரோபிளாட்டினம் என்ற சேர்மம் சதுர தள பிளாட்டினம்(II) வைக் கொண்ட தொடர்வரிசையின் முதலாவது புற்றுநோய் மருந்து ஆகும். கார்போபிளாட்டின், ஆக்சாலிபிளாட்டின் என்பவை பிற புற்றுநோய் மருந்துகளாகும். இந்த சேர்மங்கள் டி.என்.ஏவை குறுக்குவழியில் இணைப்புக்கு உட்படுத்தும் திறன் கொண்டவை ஆகும். ஒத்த பாதைகளால் புற்றுநோய் உணர் முகவர்களை ஆல்கைலேற்றம் செய்யும் செல்களைக் கொல்கின்றன. குமட்டல் மற்றும் வாந்தியெடுப்பு, முடி இழப்பு, காது கேளாமை போன்றவை சிசுபிளாட்டின் மருந்தால் ஏற்படும் பக்க விளைவுகள் ஆகும்.
-
எக்சாகுளோரோபிளாட்டினேட்டு அயனி
-
செய்செசு உப்பின் எதிர்மின் அயனி
-
டைகுளோரோ(சைக்ளோஆக்டா-1,5-டையீன்)பிளாட்டினம்(II)
-
சிசுபிளாட்டின்
பயன்பாடுகள்
- வெப்பநிலையை அளக்கப் பயன்படும் மின்தடை வெப்பமானிகளில் பயன்படுகின்றது. வெப்பநிலை மாற்றத்தினால், பிளாட்டினத்தின் மின் தடை எதிர்பார்க்கும்படி மாறுவதால், மின் தடை மாற்றத்தை அளப்பதின் மூலம் வெப்பநிலையை அறியும் ஒரு கருவியாகப் பயன்படுகின்றது.
- நீட்சிப் பொருளாகிய சிலிக்கோன் எலாஸ்டமர் பொருள்களில் வினையூக்கியாகப் பயன்படுகின்றது.
- நகைகள்
- தானுந்துகளில் நச்சு வளிகளை மாற்றப் பயன்படும் வினையூக்கி
வரலாறு
இயற்கையில் கிடைக்கும் பிளாட்டினம்மும் பிளாட்டினம்-மிகுந்துள்ள கலவைப்பொருள்கள் பற்றியும் நெடுங்காலமாக மக்கள் அறிந்திருந்தார்கள். கொலம்பசின் காலத்திற்கு முன்னமே ஐக்கிய அமெரிக்க பழங்குடியினர், பிளாட்டினத்தைப் பற்றி அறிந்திருந்தனர். ஆனால் ஐரோப்பிய எழுத்துக்களில் 1557 இல்தான் பிளாட்டினத்தைப் பற்றிய செய்தியை இத்தாலியராகிய ஜூலியஸ் சீசர் ஸ்காலிகர் (Julius Caesar Scaliger) (1484–1558) என்பவர்தான் முதன்முதலாக பனாமா, மெக்சிக்கோ ஆகிய இடங்களில் கிடைப்பதைப் பற்றியும் அது எசுப்பானியருடைய தொழிற்கலை அறிவால் உருக்கமுடியாமல் இருந்ததாகக் குறிப்பிடுகின்றார். ("up until now impossible to melt by any of the Spanish arts").
ஜூலை 2010 ஆம் ஆண்டு தமிழ்நாட்டில் பிளாட்டினம் இருப்பதாக கண்டரியபட்டது[5].

உற்பத்தி
பிளாட்டினமானது நிக்கல் மற்றும் தாமிர சுரங்கங்களின் மீதமுள்ள பிளாட்டின சேர்மங்களில் இருந்து வணிக ரீதியாக பெறப்படுகிறது.செம்பை மின்னாற் சுத்திகரிப்பு செய்யும் போது இது நேர்முனை முனைகளில் படிகின்றது. நூய பிளாட்டினமானது மற்ற தாதுகளுடன் கிடைத்தால் அது அசுத்தங்களை நீக்குவதன் மூலம் பிறித்தெடுக்கப்படுகிறது.பிளாட்டினமானது அதன் அசுத்தங்களை விட அடர்த்தியானது எனவே நீரோட்டமுறைகள் மூலம் எளிதாக பிரித்தெடுக்கலாம்.மேலும் இது காந்தத்தால் ஈர்க்கப்படுவதில்லை எனவே நிக்கல் மற்றும் இரும்பு தாது கலவையில் இருந்து இயங்கும் மின்காந்தம் மூலம் நீக்கப்படும். பிளாட்டினம் மற்ற பொருட்களை விட மிகவும் அதிக உருகுநிலையை கொண்டுள்ளதால் அதன் அசுத்தங்களை உருக்கியும் பிரித்தெடுக்கலாம். மேலும் வேதியல் முறைகளில் பிளாட்டின,தங்க கலவையை இராஜ திரவகத்தில் கரைத்து பின் தனித்தனியே மற்ற பொருட்களை படியசெஇவதன் மூலம் பிரித்தெடுக்கலாம் .
கிடப்பும் மலிவும்


பிளாட்டினம் மிகவும் அரிதாகக் கிடைக்கும் ஒரு தனிமம். நில உருண்டையின் மேல் ஓட்டில் 0.003 ppb (பில்லியன் பகுதியின் பங்குகள்) மட்டுமே உள்ளது. தங்கத்தைக் காட்டிலும் 30 மடங்கு அரிதானது.[6]
2005 இல், தென் ஆப்பிரிக்காதான் உலகின் மிகக் கூடுதலான அளவில் பிளாட்டினம் உற்பத்தி செய்த நாடு. உலக உற்பத்தியில் ஏறத்தாழ 80% தென் ஆப்பிரிக்காவைச் சேர்ந்தது. அடுத்ததாக ரஷ்யாவும் கனடாவும் நிற்கின்றன.[7]
அடிக்குறிப்புகளும் மேற்கோள்களும்
- ↑ Krebs, Robert E. (1998). "Platinum". The History and Use of our Earth's Chemical Elements. Greenwood Press. பக். 124–127. பன்னாட்டுத் தரப்புத்தக எண்:0-313-30123-9.
- ↑ George B. Kauffman; Thurner, Joseph J.; Zatko, David A. (1967). "Ammonium Hexachloroplatinate(IV)". Inorganic Syntheses. Inorganic Syntheses 9: 182–185. doi:10.1002/9780470132401.ch51. பன்னாட்டுத் தரப்புத்தக எண்:978-0-470-13240-1.
- ↑ Smith, G. F.; Gring, J. L. (1933). "The Separation and Determination of the Alkali Metals Using Perchloric Acid. V. Perchloric Acid and Chloroplatinic Acid in the Determination of Small Amounts of Potassium in the Presence of Large Amounts of Sodium". Journal of the American Chemical Society 55 (10): 3957–3961. doi:10.1021/ja01337a007.
- ↑ Ahrens, Sebastian; Strassner, Thomas (2006). "Detour-free synthesis of platinum-bis-NHC chloride complexes, their structure and catalytic activity in the CH activation of methane". Inorganica Chimica Acta 359 (15): 4789–4796. doi:10.1016/j.ica.2006.05.042.
- ↑ http://www.thehindu.com/news/cities/Chennai/article495603.ece
- ↑ "Platinum: Pure, Rare, Eternal". பார்க்கப்பட்ட நாள் 2007-10-27.
- ↑ "PLATINUM-GROUP METALS" (PDF). U.S. Geological Survey, Mineral Commodity Summaries. January 2007. பார்க்கப்பட்ட நாள் 2007-08-19.
- Los Alamos National Laboratory — Platinum
- Nuclides and Isotopes Fourteenth Edition: Chart of the Nuclides, General Electric Company, 1989.
- Jefferson Lab — The Element Platinum