நைத்திரேட்டு

| |
| பெயர்கள் | |
|---|---|
| முறையான ஐயூபிஏசி பெயர்
நைட்ரேட்டு அல்லது நைத்திரேட்டு | |
| இனங்காட்டிகள் | |
| 14797-55-8 | |
| ChEBI | CHEBI:17632 |
| ChemSpider | 918 |
InChI
| |
| யேமல் -3D படிமங்கள் | Image |
| பப்கெம் | 943 |
SMILES
| |
| பண்புகள் | |
| NO− 3 | |
| வாய்ப்பாட்டு எடை | 62.00 g·mol−1 |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
| Infobox references | |
நைட்ரேட்டு (Nitrate) என்பது NO−
3 என்ற மூலக்கூற்று வாய்ப்பாட்டைக் கொண்ட ஒரு பல்லணு அயனியாகும். இதை நைத்திரேட்டு என்ற பெயராலும் அழைக்கலாம். நைத்திரேட்டு அயனியின் மூலக்கூற்று நிறை 62.0049 கி/மோல் ஆகும். நைட்ரேட்டு எசுத்தர்களை (RONO2) வேதிவினைக் குழுவாகக் கொண்ட கரிமச் சேர்மங்களும் நைட்ரேட்டுகள் என்றே அழைக்கப்படுகின்றன.
கட்டமைப்பு[தொகு]
நைட்ரிக் அமிலத்தின் இணைகாரமான இந்த எதிர்மின் அயனியில் ஒரு மைய நைட்ரசன் அணுவும் அதனைச்சுற்றி முக்கோணத்தள அமைப்பில் ஒரேமாதிரியாக பிணைக்கப்பட்ட மூன்று ஆக்சிசன் அணுக்களும் சூழ்ந்துள்ளன. நைட்ரேட்டு அயனி முறையாக -1 என்ற எதிர்மின் சுமையைக் கொண்டுள்ளது. ஒவ்வோர் ஆக்சிசன் அணுவும் −2⁄3 என்ற எதிர் மின்னேற்றத்தையும், நைட்ரசன் +1 என்ற நேர் மின்னேற்றத்தையும் கொண்டிருப்பதால், நைத்திரேட்டு அயனியின் முறையான மின்னேற்றம் எதிர்மின்னேற்றமாக அமைந்து பல்லணு நைத்திரேட்டு அயனியாக உருவாகிறது. இவ்வொழுங்கமைவு பொதுவாக உடனிசைவு கட்டமைப்புக்கு உதாரணமாகப் பயன்படுத்தப்படுகிறது. ஒத்த இலத்திரன் எண்ணிக்கை கொண்ட கார்பனேட்டு அயனியைப் போல நைத்திரேட்டு அயனியையும் உடனிசைவுக் கட்டமைப்பாகக் குறிக்கலாம்.
பண்புகள்[தொகு]

திட்டவெப்பநிலை மற்றும் அழுத்த்த்தில் கிட்டத்தட்ட அனைத்து கனிம நைட்ரேட் உப்புகளும் நீரில் கரையக்கூடியவையாக உள்ளன. . கனிம நைட்ரேட் உப்புக்கான ஒரு பொதுவான எடுத்துக்காட்டாக சால்ட்டுபீட்ட எனப்படும் பொட்டாசியம் நைட்ரேட்டு உப்பைக் குறிப்பிடலாம். மனித உடலில் கனிம நைட்ரேட்டு உப்பு கீரை மற்றும் அருகுலா போன்ற பச்சை உணவுகள் மூலம் கிடைக்கிறது. பீட்ரூட் சாறு மற்றும் பிற காய்கறிகளுக்குள் கனிம நைட்ரேட்டு செயல்படக்கூடிய ஓர் உட்கூறாக உள்ளது. பதப்படுத்தப்பட்ட இறைச்சிகள், பல்வேறு இலை காய்கறிகள் மற்றும் குடிநீரில் நைட்ரேட்டு உணவு காணப்படுகிறது. உண்ணப்படும் பதப்படுத்தப்பட்ட இறைச்சிகளின் அளவு மற்றும் அந்த இறைச்சிகளில் உள்ள நைட்ரேட்டுகளின் செறிவு ஆகியவற்றைக் கொண்டு நைட்ரேட்டின் நுகர்வு அளவு தீர்மானிக்கப்படுகிறது. உடலில் நைட்ரேட்டு மற்றும் நீர் நைட்ரிக் ஆக்சைடாக மாற்றப்படுகின்றன. இது உயர் இரத்த அழுத்தத்தைக் குறைக்கும். உயர் இரத்த அழுத்த எதிர்ப்பு உணவுகளில் பொதுவாக அதிக அளவு நைட்ரேட்டுகள் உள்ளன. அவை முதலில் உமிழ்நீரில் நைட்ரைட்டாக குறைக்கப்படுகின்றன. நைட்ரிக் ஆக்சைடு உருவாதலுக்கு முன்னரான உமிழ்நீர் பரிசோதனையில் இது உறுதிப்படுத்தப்படுகிறது [1].
தோற்றம்[தொகு]
நைட்ரேட்டு உப்புகள் இயற்கையாக பூமியில் பெரிய படிவுகளாகக் காணப்படுகின்றன. குறிப்பாக சோடியம் நைட்ரேட்டின் முக்கியமான மூலம் நைட்ராட்டின் ஆகும்.
பல்வேறு நைட்ரேட்டாக்கும் பாக்டீரியா இனங்கள் நைட்ரேட்டுகளை உற்பத்தி செய்கின்றன. துப்பாக்கி ரவைகளுக்காகவும் வரலாற்றில் நைட்ரேட்டுகள் தயாரிக்கப்படுகின்றன. நைட்ரேட்டு கனிமங்கள் பற்றாக்குறை ஏற்படும் நிகழ்வுகளில் சிறுநீர், சாணம் ஆகியவற்றைப் பயன்படுத்தி பலவிதமான நொதித்தல் செயல்முறைகளில் நைட்ரேட்டுகள் தயாரிப்பதுண்டு. உரங்களில் நைட்ரேட்டுகள் காணப்படுகின்றன.
பூமியின் நைட்ரஜன்-ஆக்சிசன் நிறைந்த வளிமண்டலத்தில் மின்னல் தாக்கப்படுவதால், நைட்ரசன் டை ஆக்சைடு நீராவியுடன் வினைபுரியும் போது நைட்ரிக் அமிலம் தயாரிக்கப்படுகிறது.
தொடர்புடைய வேதிப்பொருட்கள்[தொகு]
நைத்திரசு அமிலத்தின் உப்பான நைத்திரைட்டு (NO−
2), நைத்திரேட்டிலிருந்தும் வேறானது. நைத்திரேட்டுக்களைப் போன்ற வாய்பாடும் அமைப்பும் கொண்டனவும், ஆனால், O− அணுக்களில் ஒன்று நைத்திரோ வினைத் தொகுதியினால் பதிலிடப்பட்டுள்ளதுமான கரிமச் சேர்மங்கள் நைத்திரோ சேர்மங்கள் எனப்படுகின்றன. நைத்திரோ மீதேனும், பெயர்பெற்ற டி.என்.டி எனப்படும் முந்நைத்திரோ தொலுயீனும் இவ்வகைச் சேர்மங்களுக்கு எடுத்துக்காட்டுகளாகும்.
மனித உடல்நலத் தாக்கங்கள்[தொகு]
குடலீரல் வளர்சிதைமாற்றத்தின் ஊடாக நைத்திரேட்டு அமோனியாவாக மாறுவதால் மனிதரில் நைத்திரேட்டு நச்சேற்ற நோய் ஏற்படுகிறது. இதில் நைத்திரைட்டு ஒரு இடைவிளைவாக உள்ளது.[2] நைத்திரைட்டுக்கள், இரத்தப் புரதத்தில் உள்ள இரும்பை பெரசு (2+) அயனிகளில் இருந்து பெரிக்கு (3+) அயனிகளாக மாற்றுகிறது. இதன் மூலம் இது ஒட்சிசனை எடுத்துச் செல்ல இயலாததாக ஆகிறது.[3] இது உறுப்புக்களின் இழையங்களில் ஒட்சிசன் பற்றாக்குறையை எற்படுத்துவதால் "குருதி இரும்புக்கனிமக்குறை" (methemoglobinemia) எனப்படும் ஆபத்தான நிலைமை ஏற்படுகிறது. இந்நிலையை மீதைலீன் நீலம் எனப்படும் சேர்வையைக் கொண்டு குணப்படுத்த முடியும். இது பாதிக்கப்பட்ட குருதியில் காணப்படும் பெரிக்கு வடிவில் உள்ள இரும்பைப் பழையபடி பெரசு இரும்பாக மாற்றுகிறது.
குழந்தைப்பருவ வளர்ச்சிக் கட்டத்தில் நைத்திரேட்டு வளர்சிதை மாற்றத்தை ஏற்படுத்தும் முக்கிளிசரைட்டுகள் அதிக செறிவில் இருப்பதால், குழந்தைகள் குருதி இரும்புக்கனிமக்குறை நோயினால் தாக்கப்படுவதற்கான வாய்ப்புக்கள் அதிகம். குழந்தைகளில் காணப்படும் குருதி இரும்புக்கனிமக்குறை, நீலக் குழந்தைக் கூட்டறிகுறி (blue baby syndrome) எனப்படும். தற்காலத்தில், நீலக் குழந்தைக் கூட்டறிகுறிக்கும், குடிக்கும் நீரில் காணப்படும் நைத்திரேட்டுக்கும் தொடர்புகள் உள்ளனவா என்பது பற்றிக் குறிப்பிடத்தக்க அளவில் அறிவியல் ஐயங்கள் உள்ளன.[4][5] இப்போது, நீலக் குழந்தைக் கூட்டறிகுறி பல காரணிகளின் விளைவாக ஏற்படக்கூடும் என எண்ணுகிறார்கள். வயிற்றுக் குழப்பத்தை உண்டுபண்ணும் காரணிகள், அடர் உலோக நச்சுத்தன்மை என்பன இவ்வாறான காரணிகளாக இருக்கலாம் என்றும் நைத்திரேட்டு இதில் மிகச் சிறிய பங்களிப்பையே செய்கிறது என்றும் கருத்து நிலவுகிறது. நைத்திரேட்டும் ஒரு காரணியாக இருக்கலாம் என்று ஐயப்படக்கூடிய இடங்களில், அதிக நைத்திரேட்டுச் செறிவுள்ள நீரைக் குடிப்பதால் ஏற்பட்டிருக்கக்கூடும். தவிர, கூடிய நைத்திரேட்டுக்கள் காணப்படும் காய்கறிகளை உண்பதனாலும் மனித உடலில் நைத்திரேட்டுகள் உட்செல்லக்கூடும். "லெட்டியூசு" எனப்படும் கீரை வகையில், அது வளரும்போதுள்ள நிலைமைகளைப் பொறுத்து நைத்திரேட்டு அளவு கூடுதலாக இருக்கலாம். குறைவான சூரிய ஒளி; மொலிப்டினம், இரும்பு போன்ற நுண்ணூட்டங்கள் போதாமை; நைத்திரேட்டுக்களைத் தாவரம் தன்வயப்படுத்துவதில் குறைபாடு என்பன காய்கறிகளில் நைத்திரேட்டு அளவு கூடுதலாகக் காணப்படுவதற்குக் காரணங்கள் ஆகலாம். நைத்திரேட்டு உரங்களைக் கூடிய அளவில் இடுவது மூலமும், அறுவடை செய்யும் காய்கறிகளில் நைத்திரேட்டு அளவு கூடுதலாக இருப்பதற்கு வாய்ப்புக்கள் உண்டு.[6]
கடல் நச்சூட்டம்[தொகு]
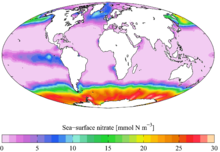
நன்னீர்நிலைகளில் அல்லது கழிமுகச் சூழல்களில் நிலத்துக்கு அண்மையான பகுதிகளில் நைத்திரேட்டுக்களின் அளவு கூடுதலாகி மீன்கள் போன்ற உயிரினங்கள் இறப்பதற்கான வாய்ப்புக்கள் உண்டு. நைத்திரைட்டுக்கள், அமோனியா போன்றவற்றிலும் பார்க்க நைத்திரேட்டுக்கள் குறைவான நச்சுத்தன்மை கொண்டவையெனினும்,[7] மில்லியன்களில் 30 பகுதிகள் (ப/மில் - ppm) அளவுக்கு நைத்திரேட்டு நீரில் இருக்குமானால், இது சில நீர்வாழ் இனங்களின் வளர்ச்சியைக் குறைக்கவும், நோய்த்தடுப்பு வல்லமையைக் குறைக்கவும் கூடுமெனக் கருதப்படுகிறது.[8] ஆயினும், தீவிர நைத்திரேட்டு நஞ்சாதல் சோதனைகள் தொடர்பான நடபடிகளில் உள்ள குறைபாடுகள் தெரிய வந்திருப்பதால், நைத்திரேட்டு நச்சுத்தன்மையின் அளவு பற்றிய விடயம் இப்போது விவாதிக்கப்பட்டு வருகிறது.[9] நீர்சார் சூழல்களில் அளவுக்கு மீறிய நைத்திரேட்டுச் செறிவு காணப்படும் பெரும்பாலான தருணங்களில், அளவுக்கு அதிகமான நைத்திரேட்டு உரங்கள் பயன்படுத்தப்பட்ட வேளாண்மை நிலங்களில் இருந்தும், நிலத்தோற்றப் பகுதிகளில் இருந்தும் வடியும் நீரின் காரணமாகவே இது ஏற்படுகிறது.
பயன்கள்[தொகு]

நைட்ரேட்டுகள் முக்கியமாக விவசாயத்திற்குத் தேவையான உரங்களாகப் பயன்படுத்தப்படுகின்றன, ஏனெனில் அவை அதிக கரைதிறன் மற்றும் மக்கும் தன்மை கொண்டவையாக உள்ளன. அம்மோனியம், சோடியம், பொட்டாசியம், கால்சியம் மற்றும் மெக்னீசியம் உப்புகள் முக்கியமான நைட்ரேட்டு உரங்களாகும். இந்த நோக்கத்திற்காக ஆண்டுக்கு பல மில்லியன் கிலோகிராம் நைட்ரேட்டு உற்பத்தி செய்யப்படுகிறது [10].
ஆக்சிசனேற்ற முகவர்களாகப் பயன்படுவது நைட்ரேட்டுகளின் இரண்டாவது பெரிய பயன்பாடாகும். குறிப்பாக வெடிபொருட்களில் உள்ள கார்பன் சேர்மங்களின் விரைவான ஆக்சிசனேற்றம் பெரிய அளவிலான வாயுக்களை விடுவிக்கிறது. உருகிய கண்ணாடி மற்றும் சில மட்பாண்ட வகைகளிலிருந்து காற்று குமிழ்களை அகற்ற சோடியம் நைட்ரேட்டு பயன்படுத்தப்படுகிறது. உருகிய நைட்ரேட்டு உப்பின் கலவைகள் சில உலோகங்களை கடினப்படுத்த பயன்படுத்தப்படுகின்றன.
வெடிபொருட்கள் மற்றும் மேசைப் பந்து விளையாட்டுப் பந்துகள் செலுலாய்டில் இருந்து தயாரிக்கப்படுகின்றன. 20 ஆம் நூற்றாண்டின் முற்பகுதியில், பெரும்பாலான இயங்கு படச்சுருள்கள் நைட்ரோசெல்லுலோசால் ஆக்கப்பட்டன. ஆனால் அப்படச்சுருள்களின் தீவிரமான எரியக்கூடிய தன்மை காரணமாக 20 ஆம் நூற்றாண்டின் நடுப்பகுதியில் அவை பாதுகாப்புப் படச்சுருள்களாக மாற்றப்பட்டன. நைட்ரைட்டுகள் முக்கியமாக இறைச்சி பதப்பபடுத்துதலில் பயன்படுத்தப்படும் நைட்ரஜன் சேர்மம் என்றாலும், சில சிறப்பு பதப்படுத்தும் செயல்முறைகளில் நைட்ரேட்டுகள் பயன்படுத்தப்படுகின்றன. இங்கு மூல நைட்ரேட்டு இருப்பிலிருந்து நைட்ரைட்டின் நீண்ட வெளியீடு தேவைப்படுகிறது. உணவுப் பாதுகாப்பில் நைட்ரேட்டுகளின் பயன்பாடு சர்ச்சைக்குரியதாக உள்ளது. நைட்ரேட்டுகள் அதிக செறிவுகளில் இருக்கும்போதும் உணவு தயாரிப்பு அதிக வெப்பநிலையில் சமைக்கப்படும் போதும் நைட்ரோசமீன்கள் உருவாகும் சாத்தியம் இதற்குக் காரணமாகும் [11]. இவ்விளைவை மீன் அல்லது வெள்ளை இறைச்சிகளில் வெளிப்படுவதில்லை ஆனால் பதப்படுத்தப்பட்ட இறைச்சிகளில் காணமுடிகிறது [12][13]. புற்றுநோயூக்கிகளான நைட்ரோசமீன்கள் உருவாதலை ஆக்சிச்னேற்ற எதிர்ப்பிகள், உயிர்ச்சத்து சி மற்றும் ஆல்பா-டோகோபீரோல் எனப்படும் உயிர்ச்சத்து இ போன்றவற்றை பதப்படுத்தலின்போது பயன்படுத்தினால் தடுக்க முடியும் [14].
போலியான இரைப்பைச் சமிபாடு நிபந்தனைகளில் நைட்ரோசமீன்கள் உருவாதலுக்குப் பதிலாக நைட்ரசோதயோல்கள் உருவாகின்றன. எனவே இவ்விரண்டு சேர்மங்களின் பயன்பாடும் முறைப்படுத்தப்படவேண்டும். எடுத்துக்காட்டாக, அமெரிக்காவில் நைட்ரேட்டுகள் மற்றும் நைட்ரைட்டுகளின் செறிவு பொதுவாக மில்லியனுக்கு 200 பகுதிகள் அல்லது அதற்கும் குறைவாக வரையறுக்கப்படுகின்றன [11]. வித்துகள் முளைப்பதைத் தடுப்பதன் மூலம் பதப்படுத்தப்பட்ட உலர்ந்த இறைச்சிகளை உட்கொள்வதில் ஏற்படும் நச்சைத் தடுப்பதில் அவை ஈடுசெய்ய முடியாதவை என்று கருதப்படுகிறது [15]. உடற்பயிற்சி செயல்திறனை சோதிக்கும்போது நைட்ரேட்டு உணவு கூடுதல் நேர்மறையான முடிவுகளை அளிக்கிறது என்று ஆராய்ச்சிகள் காட்டுகின்றன [16].
கண்டறிதல்[தொகு]
காட்மியம் ஒடுக்கச் செயல்முறை சோதனையின் வழியாக நைட்ரேட்டை சோதித்து கண்டறிய முடியும். காட்மியத்தை அடிப்படையாக கொண்டிருந்தாலும் இம்முறையே துல்லியமாகவும் நம்பகத்தன்மையுடனும் இருக்கிறது. எல்லாபயன்பாடுகளுக்கும் இம்முறை பொருந்தாது. நைட்ரேட்டு ரிடக்டேசு நொதியை உபயோகித்து ஒடுக்குதல் நைட்ரேட்டையும் நைட்ரைட்டையும் கண்டறிய உதவும் மாற்று வழிமுறையாகும் [17][18][19]. அமெரிக்க சுற்றுச்சூழல் பாதுகாப்பு முகமை சமீபத்தில் இம்முறையை பரிந்துரைத்தது
| HNO3 | He | ||||||||||||||||
| LiNO3 | Be(NO3)2 | B(NO 3)− 4 |
RONO2 | NO− 3 NH4NO3 |
HOONO2 | FNO3 | Ne | ||||||||||
| NaNO3 | Mg(NO3)2 | Al(NO3)3 | Si | P | S | ClONO2 | Ar | ||||||||||
| KNO3 | Ca(NO3)2 | Sc(NO3)3 | Ti(NO3)4 | VO(NO3)3 | Cr(NO3)3 | Mn(NO3)2 | Fe(NO3)2 Fe(NO3)3 |
Co(NO3)2 Co(NO3)3 |
Ni(NO3)2 | CuNO3 Cu(NO3)2 |
Zn(NO3)2 | Ga(NO3)3 | Ge | As | Se | BrNO3 | Kr |
| RbNO3 | Sr(NO3)2 | Y(NO3)3 | Zr(NO3)4 | Nb | Mo | Tc | Ru(NO3)3 | Rh(NO3)3 | Pd(NO3)2 Pd(NO3)4 |
AgNO3 Ag(NO3)2 |
Cd(NO3)2 | In(NO3)3 | Sn(NO3)4 | Sb(NO3)3 | Te | INO3 | Xe(NO3)2 |
| CsNO3 | Ba(NO3)2 | Hf(NO3)4 | Ta | W | Re | Os | Ir | Pt(NO3)2 Pt(NO3)4 |
Au(NO3)3 | Hg2(NO3)2 Hg(NO3)2 |
TlNO3 Tl(NO3)3 |
Pb(NO3)2 | Bi(NO3)3 BiO(NO3) |
Po(NO3)4 | At | Rn | |
| FrNO3 | Ra(NO3)2 | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| ↓ | |||||||||||||||||
| La(NO3)3 | Ce(NO3)3 Ce(NO3)4 |
Pr(NO3)3 | Nd(NO3)3 | Pm(NO3)3 | Sm(NO3)3 | Eu(NO3)3 | Gd(NO3)3 | Tb(NO3)3 | Dy(NO3)3 | Ho(NO3)3 | Er(NO3)3 | Tm(NO3)3 | Yb(NO3)3 | Lu(NO3)3 | |||
| Ac(NO3)3 | Th(NO3)4 | PaO2(NO3)3 | UO2(NO3)2 | Np(NO3)4 | Pu(NO3)4 | Am(NO3)3 | Cm(NO3)3 | Bk(NO3)3 | Cf | Es | Fm | Md | No | Lr | |||
மேற்கோள்கள்[தொகு]
- ↑ "Food sources of nitrates and nitrites: the physiologic context for potential health benefits". The American Journal of Clinical Nutrition 90 (1): 1–10. July 2009. doi:10.3945/ajcn.2008.27131. பப்மெட்:19439460. https://archive.org/details/sim_american-journal-of-clinical-nutrition_2009-07_90_1/page/1.
- ↑ "Nitrate and Nitrite Poisoning: Introduction". The Merck Veterinary Manual. பார்க்கப்பட்ட நாள் 2008-12-27.
- ↑ Kim-shapiro, D.B.; Gladwin, M.T.; Patel, R.P.; Hogg, N. (2005). "… between nitrite and hemoglobin: the role of nitrite in hemoglobin-mediated hypoxic vasodilation". Journal of Inorganic Biochemistry 99 (1): 237–246. doi:10.1016/j.jinorgbio.2004.10.034. பப்மெட்:15598504. http://linkinghub.elsevier.com/retrieve/pii/S0162013404003411
- ↑ T.M Addiscott & N Benjamin 2004 Nitrate and human health
- ↑ A A Avery Infant Methemoglobemia - reexamining the role of drinking water nitrates
- ↑ Marschner H 1999 Mineral nutrition of higher plants. Academic Press, London. 889
- ↑ Romano, N.; Zeng, C. (2007). "Acute toxicity of sodium nitrate, potassium nitrate and potassium chloride and their effects on the hemolymph composition and gill structure of early juvenile blue swimmer crabs (Portunus pelagicus, L. 1758) (Decapoda, Brachyura, Portunidae)." Environmental Toxicology and Chemistry 26: 1955–1962.
- ↑ Nitrates in the Aquarium
- ↑ Romano N., Zeng, C. (2007). "Effects of potassium on nitrate mediated changes to osmoregulation in marine crabs". Aquatic Toxicology 85 (3): 202–208. doi:10.1016/j.aquatox.2007.09.004. பப்மெட்:17942166.
- ↑ Laue, Wolfgang; Thiemann, Michael; Scheibler, Erich; Wiegand, Karl Wilhelm (2006). "Nitrates and Nitrites". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a17_265. பன்னாட்டுத் தரப்புத்தக எண்:978-3527306732.
- ↑ 11.0 11.1 "Curing Food". Edinformatics. பார்க்கப்பட்ட நாள் 21 February 2010.
- ↑ "Dietary meat, endogenous nitrosation and colorectal cancer". Biochemical Society Transactions 35 (Pt 5): 1355–7. November 2007. doi:10.1042/BST0351355. பப்மெட்:17956350.
- ↑ "Effect of white versus red meat on endogenous N-nitrosation in the human colon and further evidence of a dose response". The Journal of Nutrition 132 (11 Suppl): 3522S–3525S. November 2002. doi:10.1093/jn/132.11.3522S. பப்மெட்:12421881.
- ↑ "Sodium nitrite: the "cure" for nitric oxide insufficiency". Meat Science 92 (3): 274–9. November 2012. doi:10.1016/j.meatsci.2012.03.001. பப்மெட்:22464105.
- ↑ De Vries, John (1997). Food Safety and Toxicity. CRC Press. பக். 70. பன்னாட்டுத் தரப்புத்தக எண்:978-0-8493-9488-1. https://archive.org/details/foodsafetytoxici0000unse.
- ↑ "The Effect of Dietary Nitrate Supplementation on Endurance Exercise Performance in Healthy Adults: A Systematic Review and Meta-Analysis". Sports Medicine (Auckland, N.Z.) 47 (4): 735–756. April 2017. doi:10.1007/s40279-016-0617-7. பப்மெட்:27600147. http://espace.library.uq.edu.au/view/UQ:407817/uq407817_OA.pdf.
- ↑ "Nitrate reductase for nitrate analysis in water". Environmental Chemistry Letters 4 (2): 69–73. 28 March 2006. doi:10.1007/s10311-006-0035-4.
- ↑ Patton CJ, Kryskalla JR (2016). "Analytical properties of some commercially available nitrate reductase enzymes evaluated as replacements for cadmium in automated, semiautomated, and manual colorimetric methods for determination of nitrate plus nitrite in water". Report No.: 2013–5033: U.S. Geological Survey Scientific Investigations Report. p. 366.
{{cite web}}: CS1 maint: location (link) - ↑ "Colorimetric determination of nitrate plus nitrite in water by enzymatic reduction, automated discrete analyzer methods". U.S. Geological Survey Techniques and Methods: 34. 2011.
புற இணைப்புகள்[தொகு]
| HNO3 | He | ||||||||||||||||
| LiNO3 | Be(NO3)2 | B(NO 3)− 4 |
RONO2 | NO− 3 NH4NO3 |
HOONO2 | FNO3 | Ne | ||||||||||
| NaNO3 | Mg(NO3)2 | Al(NO3)3 | Si | P | S | ClONO2 | Ar | ||||||||||
| KNO3 | Ca(NO3)2 | Sc(NO3)3 | Ti(NO3)4 | VO(NO3)3 | Cr(NO3)3 | Mn(NO3)2 | Fe(NO3)2 Fe(NO3)3 |
Co(NO3)2 Co(NO3)3 |
Ni(NO3)2 | CuNO3 Cu(NO3)2 |
Zn(NO3)2 | Ga(NO3)3 | Ge | As | Se | BrNO3 | Kr |
| RbNO3 | Sr(NO3)2 | Y(NO3)3 | Zr(NO3)4 | Nb | Mo | Tc | Ru(NO3)3 | Rh(NO3)3 | Pd(NO3)2 Pd(NO3)4 |
AgNO3 Ag(NO3)2 |
Cd(NO3)2 | In(NO3)3 | Sn(NO3)4 | Sb(NO3)3 | Te | INO3 | Xe(NO3)2 |
| CsNO3 | Ba(NO3)2 | Hf(NO3)4 | Ta | W | Re | Os | Ir | Pt(NO3)2 Pt(NO3)4 |
Au(NO3)3 | Hg2(NO3)2 Hg(NO3)2 |
TlNO3 Tl(NO3)3 |
Pb(NO3)2 | Bi(NO3)3 BiO(NO3) |
Po(NO3)4 | At | Rn | |
| FrNO3 | Ra(NO3)2 | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| ↓ | |||||||||||||||||
| La(NO3)3 | Ce(NO3)3 Ce(NO3)4 |
Pr(NO3)3 | Nd(NO3)3 | Pm(NO3)3 | Sm(NO3)3 | Eu(NO3)3 | Gd(NO3)3 | Tb(NO3)3 | Dy(NO3)3 | Ho(NO3)3 | Er(NO3)3 | Tm(NO3)3 | Yb(NO3)3 | Lu(NO3)3 | |||
| Ac(NO3)3 | Th(NO3)4 | PaO2(NO3)3 | UO2(NO3)2 | Np(NO3)4 | Pu(NO3)4 | Am(NO3)3 | Cm(NO3)3 | Bk(NO3)3 | Cf | Es | Fm | Md | No | Lr | |||


