தையோ அசிட்டால்
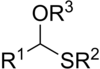

தையோஅசிட்டால்கள் (Thioacetals) என்பவை அசிட்டால்களின் கந்தக ஒப்புமை சேர்மங்களாகும். அசிட்டால்கள் தயாரிப்பது போலவே ஆல்டிகைடுடன் தையோல் சேர்த்து வினைபுரிவதன் மூலமாக இவற்றைத் தயாரிக்க முடியும்.
- RSH + R'CHO → R'CH(OH)SR
இடைநிலைச் சேர்மமான டைதையோ அசிட்டால்கள்,தையோ அசிட்டால்கள் தயாரிப்பது போலவே தயாரிக்கப்படுகின்றன.
- RSH + R'CH(OH)SR → R'CH(SR)2 + H2O
குறிப்பாக இத்தகைய வினைகள் இலூயிக்கமிலம் அல்லது பிரோன்சுடெட்டமிலம் போன்ற வினையூக்கிகளின் உதவியால் நிகழ்கின்றன. ஆல்டிகைடுடன் 1,2 ஈத்தேன் டைதயோல் வினைபுரிவதால் உண்டாகும் டைதையோ அசிட்டால்கள் கரிமத் தொகுப்பு வினைகளில் உபயோகமாக உள்ளன.
- C2H4(SH)2 + R'CHO → R'CHS2C2H4 + H2O
ஆதலால் ஆல்டிகைடில் உள்ள கார்பனைல் கார்பன் அதாவது இரட்டை பிணைப்பில் ஆக்சிசனைக் கொண்டுள்ள கார்பன் அணு எலக்ட்ரான் கவரியாக உள்ளது. டைதையோ அசிட்டால்களின் புரோட்டான் நீங்கும் வழிப்பொருள் சிறப்புறுப்பாக அணுக்கருகவர் கார்பன் மையங்கள் உள்ளன.
- R'CHS2C2H4 + R2NLi → R'CLiS2C2H4 + R2NH
பொதுவாக இவ்வினை 1,3 டைதையோலேன்களில் நடைபெறுகிறது. R'(H)Cδ+Oδ− மற்றும் R'CLi(SR)2 இடையிலான முனைவுத்தன்மை தலைகீழாகிறது. இவ்வாறு முனைவுத்தன்மை தலைகீழாதலை உம்போலங்கு என்கிறார்கள்[1][2]
மேற்கோள்கள்[தொகு]
- ↑ எஆசு:10.1002/anie.197902393 10.1002/anie.197902393
This citation will be automatically completed in the next few minutes. You can jump the queue or expand by hand - ↑ எஆசு:10.1055/s-1977-24412 10.1055/s-1977-24412
This citation will be automatically completed in the next few minutes. You can jump the queue or expand by hand
