மதுசாரம்


வேதியியலில் மதுச்சாரம் (Alcohol) என்பது ஐதராக்சில் வேதி வினைக்குழுவைக் (–OH) கொண்டுள்ள எந்தவொரு கரிமச் சேர்மத்தையும் குறிக்கும். இவ்வினைக்குழு நிறைவுற்ற ஐதரோகார்பன் அணுவுடன் பிணைக்கப்பட்டிருக்கும் [2]. ஆல்ககால் என்ற பொதுப்பெயர் பொதுவாக எத்தனால் அல்லது எத்தில் ஆல்ககாலைக் குறிக்கிறது. மதுபானங்களில் மிகவும் பிரபலமான ஆல்ககால் வகையும் இதுவேயாகும்.
வேதிப்பொருட்களில் எங்கெல்லாம் ஐதராக்சில் குழு வேதி வினைக்குழுவாக முதன்மை பெற்றுள்ளதோ அங்கெல்லாம் ஆல் என்ற பின்னொட்டை அச்சேர்மத்தின் பெயருடன் சேர்க்க ஐயுபிஏசி பரிந்துரைக்கிறது. இவ்வாறில்லாமல் வினைக்குழு முதன்மை பெறும் இடங்களில் ஐதராக்சி என்ற முன்னொட்டு சேர்மத்தின் பெயருடன் இணைக்கப்படுகிறது. முறைப்படி திட்டமிடப்படாத பெயர் வைக்கப்பட்டுள்ள பாராசிட்டமால், கொலசுடிரால் போன்ற பொருள்களில் உள்ள ’ஆல்’ பின்னொட்டும் அப்பொருளில் ஐதராக்சில் குழு இடம்பெற்றுள்ளதைக் குறிப்பிட்டுக் காட்டுகிறது. ஆனால் பல சேர்மங்களில் குறிப்பாக குளுக்கோசு, புருக்டோசு போன்ற சர்க்கரைப் பொருட்களில் பின்னொட்டு ஆல் பயன்படுத்தப்படாமல் ஐதராக்சில் குழுவைப் பெற்றுள்ளன. மெத்தனாலும் எத்தனாலும் நிறைவுற்ற நேர்கோட்டு சங்கிலி அமைப்புள்ள எளிய ஆல்ககால்கள் ஆகும். இவற்றின் மூலக்கூற்று அமைப்பு பொது வாய்ப்பாடு CnH2n+1OH. ஆகும்.
பெயரிடல்[தொகு]
பெயர்க்காரணம்[தொகு]
ஆல்ககால் என்ற சொல் அரபு (அரபு: الكحل, மொழிபெயர். Al-kuḥl) மொழியில் இருந்து வரப்பெற்றுள்ளது. இது கண் மையாகப் பயன்படுத்தப்பட்ட ஒரு தூள் ஆகும் [3]. அல் – என்ற அரபு மொழிச்சொல் ஆங்கில மொழியிலுள்ள இன் என்ற சுட்டிடைச் சொல்லுக்குச் சமமான சொல்லாகும்.
இயற்கையில் கிடைக்கும் சிடிப்னைட்டு அல்லது ஆண்டிமோனைட்டு கனிமம் ஆண்டிமனி டிரைசல்பைடாக (Sb2S3) பதங்கமாகும் போது நுண் தூளாக உருவாக ஆல்ககால் பயன்படுத்தப்பட்டது. மேலும், கிருமி நாசினி, கண்மை மற்றும் ஒப்பனை போன்ற பல்வேறு செயல்களிலும் ஆல்ககால் பயன்படுத்தப்பட்டது. காய்ச்சி வடிக்கப்பட்ட பொருள் என்பதைக் குறிப்பிடவும், ஆல்ககால் என்ற பொதுப்பெயரின் பொருள் விரிவடைந்தது. பின்னர் எத்தனால் என்ற கடின மதுவைக் குறிப்பிடும் சொல்லாக குறுகியது [4].
முறையான பெயரிடல்[தொகு]
ஐயுபிஏசி முறை பெயர்கள் அறிவியல் வெளியீடுகளில் பயன்படுத்தப்படுகிறது, மேலும், பொருளின் துல்லியமான அடையாளம் எங்கெல்லாம் முக்கியமோ அங்கெல்லாம் இப்பெயர் பயன்படுத்தப்படுகிறது . எளிய ஆல்ககால்களுக்கு இம்முறையில் பெயரிடும்போது ஆல்க்கேன் சங்கிலியின் இறுதியில் ஆல் சேர்க்கப்படுகிறது. உதாரணம்: மெத்தனால், எத்தனால்[5] அவசியமான இடங்களில் தேவைப்பட்டால் ஐதராக்சில் குழு இருக்கும் இடம் எண்ணால் சுட்டிக்காட்டப்படுகிறது. ஆல்க்கேன் பெயருக்கும் ஆல் பின்னொட்டுக்கும் இடையில் இந்த எண் அமைகிறது. உதாரனம்: புரோப்பேன்-1-ஆல் CH3CH2CH2OH, புரோப்பேன்-2-ஆல் CH3CH(OH)CH3. ஆல்டிகைடு, கீட்டோன், கார்பாக்சிலிக் அமிலம் போன்ற உயர் முன்னுரிமை குழுக்கள் ஒருவேளை இடம்பெற்றிருந்தால் ஐதராக்சி என்ற முன்னொட்டு பெயருடன் சேர்க்கப்படுகிறது. உதாரணம்:1-ஐதராக்சி-2-புரோப்பனோன் (CH3C(O)CH2OH).[5] e.g., as in 1-hydroxy-2-propanone (CH
3C(O)CH
2OH).[6]

பொதுப்பெயர்கள்[தொகு]
ஆல்ககால் பெரும்பாலும் அதனுடன் தொடர்புடைய ஆல்க்கைல் குழுவின் பெயரில் அழைக்கப்படுகிறது, இதன்படி "ஆல்ககால்" என்ற சொல் ஆல்க்கேனின் பெயருடன் சேர்க்கப்பட்டு அழைக்கப்படுகிறது. , எ.கா., மெத்தில் ஆல்ககால் எத்தில் ஆல்ககால் என்பன. ஐதராக்சில் குழு இறுதியில் அல்லது புரோப்பேன் சங்கிலியில் நடுத்தர கார்பனுடன் பிணைக்கப்பட்டுள்ளதைப் பொறுத்து புரோப்பைல் ஆல்ககால் நே-புரோப்பைல் ஆல்க்ககால் அல்லது ஐசோபுரோப்பைல் ஆல்ககால் என அழைக்கப்படுகிறது. இங்கும் ஏற்கனவே கூறப்பட்டது போல உயர் முன்னுரிமை குழுக்கள் ஒருவேளை இருந்தால் ஐதராக்சி முன்னொட்டு சேர்க்கப்பட்டு அழைக்கப்படுகிறது[7]. ஐதராக்சில் செயல்பாட்டுக் குழுவைக் கொண்டிருக்கும் கார்பன் அணுவுடன் தொடர்புடைய கார்பன் அணுக்களின் எண்ணிக்கையை அடிப்படையாகக் கொண்டு முதன்மை, இரண்டாம் நிலை மற்றும் மூன்றாம் நிலை ஆல்ககால்கள் என்றும் வகைப்படுத்தப்படுகிறது. இவை முறையே எண்ணியல் சுருக்கமாக 1°, 2°, மற்றும் 3° எனப்படுகின்றன [8])
முதனிலை ஆல்ககால்களின் பொது வாய்ப்பாடு RCH2OH ஆகும். மெத்தனால் (CH3OH) ஒரு எளிய முதனிலை ஆல்ககாலாகும். (இங்கு R=H). அடுத்த எளிய முதனிலை ஆல்ககால் எத்தனால் (இங்கு R= CH3,). இரண்டாம் நிலை ஆல்ககால்கள் RR'CHOH என்ற அமைப்பில் உருவாகின்றன. இதன்படி முதலாவது எளிய இரண்டாம்நிலை ஆல்ககால் 2-புரோப்பனால் (R=R'=CH3). மூன்றாம் நிலை ஆல்ககால்கள் RR'R"COH உருவாகின்றன. மூன்றாமை-பியூட்டனால் ஓர் எளிய மூன்றாம்நிலை ஆல்ககாலாகும். (இங்கு R, R', மற்றும் R" = CH3).
| வேதி வாய்ப்பாடு | ஐயுபிஏசி பெயர் | பொதுப்பெயர் |
|---|---|---|
| ஓரைதராக்சி ஆல்ககால்கள் | ||
| CH3OH | மெத்தனால் | மரச்சாராயம் |
| C2H5OH | எத்தனால் | ஆல்ககால் |
| C3H7OH | புரோப்பேன்-2-ஆல் | ஐசோபுரோப்பைல் ஆல்ககால் |
| C4H9OH | பியூட்டேன்-1-ஆல் | பியூட்டனால், பியூட்டைல் ஆல்ககால் |
| C5H11OH | பென்டேன்-1-ஆல் | பென்டனால், அமைல் ஆல்ககால் |
| C16H33OH | எக்சாடெக்கான்-1-ஆல் | சிடைல் ஆல்ககால் |
| பல்லைதராக்சி ஆல்ககால்கள் | ||
| C2H4(OH)2 | ஈத்தேன்-1,2-டையால் | எத்திலீன் கிளைக்கால் |
| C3H6(OH)2 | புரோப்பேன்-1,2-டையால் | புரோப்பைலீன் கிளைக்கால் |
| C3H5(OH)3 | புரோப்பேன்-1,2,3-டிரையால் | கிளிசரால் |
| C4H6(OH)4 | பியூட்டேன்-1,2,3,4-டெட்ரால் | எரித்திரிட்டால், திரெய்டால் |
| C5H7(OH)5 | பென்டேன்-1,2,3,4,5-பென்டால் | சைலிட்டால் |
| C6H8(OH)6 | எக்சேன்-1,2,3,4,5,6-எக்சால் | மேனிட்டால், சார்பிட்டால் |
| C7H9(OH)7 | எப்டேன்-1,2,3,4,5,6,7-எப்டால் | வாலிமிட்டால் |
| நிறைவுறா அலிபாட்டிக் ஆல்ககால்கள் | ||
| C3H5OH | புரோப்-2-யீன்-1-ஆல் | அல்லைல் ஆல்க்கால் |
| C10H17OH | 3,7-டைமெத்திலாக்டா-2,6-டையீன்-1-ஆல் | கெரானியால் |
| C3H3OH | புரோப்-2-ஐன்-1-ஆல் | புரோப்பார்கைல் ஆல்ககால் |
| அலிவளைய ஆல்ககால்கள் | ||
| C6H6(OH)6 | வளையயெக்சேன்-1,2,3,4,5,6-எக்சால் | ஐனோசிட்டால் |
| C10H19OH | 2 - (2-புரோப்பைல்)-5-மெத்தில்-வளையயெக்சேன்-1-ஆல் | மெந்தால் |
ஆல்ககால்களில் உள்ள கார்பன் அணுக்களின் எண்ணிக்கை அடிப்படையில் இவற்றை குறுகிய சங்கிலி, நடுத்தர சங்கிலி, நீண்ட சங்கிலி ஆல்ககால்கள் எனப் பிரிக்கின்றனர். 1-3 கார்பன் அணுக்களைக் கொண்ட ஆல்க்கைல் சங்கிலி ஆல்ககால்களை குறுகிய சங்கிலி ஆல்ககால்கள் என்றும், 4-7 கார்பன் அணுக்களைக் கொண்ட சங்கிலிகளால் ஆக்கப்பட்டுள்ள ஆல்ககால்கள் நடுத்தர சங்கிலி ஆல்ககால்கள் என்றும், 8-21 கார்பன்களைக் கொண்ட சங்கிலிகளால் ஆக்கப்பட்டுள்ள ஆல்ககால்கள் நீண்ட சங்கிலி ஆல்ககால்கள் அல்லதுகொழுப்பு ஆல்ககால்கள் என்றும் 22 கார்பன்களுக்கும் அதிகமான சங்கிலிகளால் ஆனவற்றை மிக்நீண்ட சங்கிலி ஆல்ககால்கள் என்றும் அழைக்கின்றனர்.
"எளிய ஆல்ககால் என்ற சொற்பிரயோகம் முற்றிலும் வரையறுக்கப்படாத ஒன்றாகவே தோன்றுகிறது. இருப்பினும், எளிமையான ஆல்ககால் என்பது, பெரும்பாலும் "ஆல்ககால்" என்ற வார்த்தையை பொருத்தமான ஆல்க்கைல் குழுவின் பெயருடன் சேர்த்து குறிப்பிடப்படும் பொதுப்பெயராகவே அமைகிறது. உதாரணமாக, ஒரு கார்பனுடன் இணைக்கப்பட்ட ஒரு OH குழுவோடு பெறப்படும் ஒரு கார்பன் (ஒரு மெதில் குழு, CH3) கொண்ட சங்கிலி ஆல்ககால்கள் மெத்தில் ஆல்ககால் என்று அழைக்கப்படுகிறது, அதே நேரத்தில் இரண்டு கார்பன்கள் (ஒரு எத்தில் குழு, CH2CH3) கொண்ட சங்கிலியால் ஆக்கப்பட்ட ஆல்ககால் எத்தில் ஆல்ககால் என்று அழைக்கப்படுகிறது. மிகவும் சிக்கலான அமைப்புடன் உருவாகும் ஆல்ககால்களை IUPAC பெயரை வைத்து பயன்படுத்தப்பட வேண்டும் [9].
எத்தனால் போன்றே நொதித்தல் செயல்முறைகளால் பியூட்டனாலும் உற்பத்தி செய்யப்படுகிறது. 75 டிகிரி பாரன்கீட் (24 ° செல்சியசு) வெப்பநிலைக்கு மேலான வெப்பநிலைகளில் இந்த உயர் ஆல்ககால் உற்பத்தி செய்யப்படுகிறது. சாக்கரோமைசெசு ஈசுடு இந்நொதித்தல் செயல்முறையை நிகழ்த்துகிறது. குளோசுடிரைடியம் அசெட்டோபியூட்டைலிக்கம் பாக்டீரியத்தை செல்லுலோசுட சேர்த்தால் பியூட்டனாலை தொழில்முறையாக பேரளவில் தயாரிக்க முடியும் [10].
பயன்பாடுகள்[தொகு]
ஆல்க்ககால் உலகளாவிய அளவில் பல பயன்பாடுகளைக் கொண்டு ஒரு நீண்ட வரலாற்றையும் கொண்டுள்ளது. பெரியவர்களிடம் மதுபானமாக விற்கப்படுகிறது. எரிபொருளாகப் பயன்படுகிறது.மேலும் பல விஞ்ஞான, மருத்துவ மற்றும் தொழிற்துறை பயன்பாடுகளுக்கும் உதவுகிறது. மேலும் சொல்வதென்றால் இப்பொருளில் ஆல்ககால் பயன்படுத்தப்படவில்லை என்று சான்றளித்து தயாரிப்புகள் விற்பனைக்கு வருகின்றன என்ற அளவிற்கு ஆல்ககால் பயன்பாட்டில் உள்ளது.
மதுபானங்களாக[தொகு]
மதுபானங்கள், பொதுவாக அவற்றின் கன அளவில் 3-40% வரை எத்தனாலைக் கொண்டிருக்கும், இந்த விகிதத்திலேயே வரலாற்றுக்கு முந்தைய காலங்கள் தொட்டு மனிதர்கள் மதுபானத்தை உற்பத்தி செய்து உட்கொண்டு வருகிறார்கள். பியரில் காணப்படும் 2-மீதைல்-2-பியூட்டனால் மற்றும் γ- ஐதராக்சிபியூட்டைரிக் அமிலம் போன்ற மற்ற ஆல்ககால்களையும் மனிதர்கள் தங்கள் மனோவியல் தூண்டல்களாக உட்கொள்கின்றனர். 4 முதல் 10 கார்பன் அணுக்கள் கொண்டிருக்கும் உயர் ஆல்ககால்கள் சற்றே பாகுத்தன்மை கொண்டவை அல்லது எண்ணெய் பசையுடன் கொழுப்பு நிறைந்தவையாக இருக்கின்றன என்றும் பழங்களின் மணம் கொண்டவையாகும் என்றும் என்சைக்ளோபீடியா பிரிட்டானிக்கா கூறுகிறது. அதிகமான கிளைகளைக் கொண்ட ஆல்ககால்களும் குறிப்பாக 12 கார்பன் அணுக்களுக்கு மேல் கொண்டுள்ள ஆல்ககால்களும் அறை வெப்பநிலையில் திண்மங்களாக உள்ளன [11].
உறைதல் தடுப்பி[தொகு]
தண்ணீர் கலக்கப்பட்ட எத்திலீன் கிளைக்காலின் 50% கரைசல் பொதுவாக உறைதல் தடுப்பியாகப் பயன்படுத்தப்படுகிறது.
நுண்ணுயிர் எதிர்ப்பிகள்[தொகு]
சருமத்தை சீர்செய்வதற்கு ஒரு நுண்ணுயிர் எதிர்ப்பியாக எத்தனாலை அயோடினுடன் சேர்த்துப் பயன்படுத்த முடியும். எத்தனால் அடிப்படையிலான சோப்புகள் உணவகங்களில் பொதுவானவையாகப் பயன்படுத்தப்பட்டு வருகின்றன, ஏனெனில் மாறும் தன்மை காரணமாக அவை உலர்த்தப்பட வேண்டிய தேவையில்லை. ஆல்ககால் சார்ர்ந்த கூழ்மங்கள் கை சுத்திகரிப்பான்களாகப் பயன்படுகின்றன.
எரிபொருளாக[தொகு]
சில ஆல்ககால்கள் முக்கியமாக எத்தனால் மற்றும் மெத்தனால் போன்றவை ஆல்ககால் எரிபொருளாக பயன்படுத்தப்படுகின்றன. உள்ளெரி இயந்திரங்களில் காற்றுடன் ஆல்ககாலைச் சேர்ப்பதன் மூலம் எரிபொருள் செயல்திறனை அதிகரிக்கலாம் எனக் கூறப்படுகிறது.
பாதுகாப்புப் பொருளாக[தொகு]
அறிவியல் மற்றும் மருத்துவத்துறையில் மாதிரிகளைப் பாதுகாக்கும் பாதுகாப்புப் பொருளாக சில ஆல்ககால்கள் பயன்படுத்தப்படுகின்றன.
கரைப்பான்கள்[தொகு]
ஆல்ககால்களில் காணப்படும் ஐதராக்சில் குழுக்கள் (-OH) முனைவுத்தன்மை கொண்டுள்ளன. எனவே இவை நீர் விரும்பும் வேதிப்பொருட்களாக உள்ளன. ஆனால் இவற்றின் கார்பன் சங்கிலி பகுதியானது முனைவற்று இருப்பதால் அவை நீர் மறுப்பு வேதிப்பொருட்களாக இருக்கின்றன. ஒட்டுமொத்தமாக கார்பன் சங்கிலி நீளும் போது கார்பன் மூலக்கூறுகளின் எண்ணிக்கை அதிகரித்து நீர்மறுப்புத் தன்மையும் அதிகரிக்கின்றது. முனைவுத் தன்மை மிக்க தண்ணிரில் சிறிதளவே இவை கரைகின்றன[12]. அனைத்து ஆல்ககால்களிலும் குறுகிய கார்பன் சங்கிலியாக (ஒரு கார்பன் அணு),மெத்தனாலும் அதைத் தொடர்ந்து எத்தனாலும் (இரண்டு கார்பன் அணுக்கள்) உள்ளன.
நச்சுத்தன்மை[தொகு]

Ethanol is thought to cause harm partly as a result of direct damage to DNA caused by its metabolites.[16]

டி.என்.ஏ வின் வளர்சிதை மாற்றத்தில் எத்தனால் பாதிப்பை உண்டாக்குவதாக நம்பப்படுகிறது. முதன்மை வளர் சிதைமாற்ற விளைபொருளான ஆல்டிகைடும் இரண்டாம் நிலை விளைபொருளான அசிட்டிக் அமிலமும் எத்தனாலின் நச்சுத்தன்மைக்கு காரணமாகின்றன.
எலிகளில் அசிட்டைல்சிசுடெய்ன், தையமின் வளர்சிதைமாற்றத்தில் இந்நச்சுத்தன்மை குறைகிறது. எத்தனால் அருந்துபவர்களுக்கு புற்று நோய் வருவதற்கான சாத்தியங்கள் அதிகரிக்கின்றன என்று பல்வேறு ஆய்வுகள் தெரிவிக்கின்றன[17][18]. மூன்றாம்நிலை ஆல்ககால்கள் வளர்சிதை மாற்றத்தின் போது ஆல்டிகைடுகளை உருவாக்குவதில்லை என்பதால் இவற்றினால் ஏற்படும் நச்சுத்தன்மை அளவு குறைவாகும் [19]. இவை எத்தனாலைக் காட்டிலும் நச்சுத்தன்மை குறைவானவையாக உள்ளன. ஏனெனில் கல்லீரல் இவற்றின் வளர்சிதை மாற்றத்தில் நச்சுப்பொருட்களை உருவாக்குவதில்லை [20]. எனவே மருந்துப் பொருட்கள் தயாரிப்புக்கு இவை பொருத்தமானவையாக உள்ளன. எத்குளோர்வைனாலும் மூன்றாமை அமைல் ஆல்ககாலும் மருத்துவப்பயனும் பொழுதுபோக்கு பானமாகவும் பயன்படுகின்றன [21].
மற்ற ஆல்ககால்கள் எத்தனாலைக் காட்டிலும் அதிகம் நச்சானவையாகும். ஏனென்றால் அவை நீண்ட காலத்தை வளர்சிதை மாற்றத்திற்காக எடுத்துக் கொள்கின்றன. மேலும் அவற்றின் வளர்சிதை மாற்றமானது நச்சுத்தன்மையுள்ள பொருட்களை உற்பத்தி செய்கின்றது. உதாரணமாக, மெத்தனால் (மரச் சாராயம்) பார்மால்டிகைடையும் தொடர்ந்து பார்மிக் அமிலத்தையும் உருவாக்குகிறது. பார்மிக் அமில அதிகரிப்பு குருட்டுத்தன்மையையும் இறப்பையும் உண்டாக்கும் [22]. எலிகளில் மெத்தனாலின் உயிர் கொல்லும் அளவு 5628 மி.கி/கி.கி என்று கணக்கிடப்பட்டுள்ளது [23]).
சிகிச்சை[தொகு]
மெத்தனால் அல்லது எத்திலீன் கிளைக்கால் உட்செலுத்தப்பட்டால் உண்டாகும் நச்சுத்தன்மையைத் தடுக்க எத்தனாலை நிர்வகிப்பது ஒரு பயனுள்ள சிகிச்சையாகும். ஆல்ககால் டி ஐதரசனேசு எத்தனாலுடன் மிக உயர்ந்த நாட்டத்தைக் கொண்டுள்ளது, இதனால் மெத்தனால் செயல்படுவது தடுக்கப்படும். மீதமுள்ள மெத்ததனால் பின்னர் சிறுநீரகங்கள் மூலம் வெளியேற்றப்படும் [22][24][25].
ஈசுட்டுகளின் வளர்சிதை மாற்றத்தில் இயற்கையாக எத்தனால் தோன்றுகிறது. எனவே ஈச்ட்டு உள்ள இடங்களில் எல்லாம் எத்தனால் காணப்படுகிறது. சில பழங்களிலும் எத்தனால் உள்ளது. மெத்தனால் சுற்றுச் சூழலில் சில இடங்களிலும் காற்றில்லா சுவாசத்தில் இயற்கையாகவும் தோன்றுகிறது. குறைவான அடர்த்தியில் சூரிய மண்டலத்திற்கு வெளியே ஆல்ககால்கள் காணப்படுகின்றன [26][27].
இயற்பியல் மற்றும் வேதியியல் பண்புகள்[தொகு]
ஆல்ககால்கள் பெரும்பாலும் கசப்புச் சுவையுடன் நாசிப் பாதைகளில் தேங்கும் சுவையைக் கொண்டவை என்று விவரிக்கப்படுகின்றன. மற்ற ஆல்ககால்களைக் காட்டிலும் எத்தனால் சற்று இனிப்பானது அல்லது நெருக்கமாக பழம் போன்ற நெடியைக் கொண்டதாகும்.
பொதுவாக ஐதராக்சில் குழு ஆல்ககால் மூலக்கூறை முனைவுள்ளதாக்குகிறது. தங்களுக்குள் ஐதரசன் பிணைப்புகளை உருவாக்கிக் கொள்ளும் சேர்மங்கள் அடுத்துள்ள குழுக்களின் இடத்தடங்கல் காரணமாகப் பாதுகாக்கப்படுகின்றன. தொடர்புடைய ஐதரோ கார்பன்களைவிட ஆல்ககால்கள் உயர் கொதிநிலையைப் பெற்றுள்ளன. எத்தனாலின் கொதிநிலை 78.29 பாகை செல்சியசு ஆகும். எக்சேனின் கொதிநிலை 69 பாகை செல்சியசு மற்றும் டை எத்தில் ஈதரின் கொதிநிலை 34.6 பாகை செல்சியசு வெப்பநிலை ஆகும்.
தண்ணீரைப் போலவே ஆல்ககால்களில் உள்ள -OH குழு அமிலம் அல்லது காரத்தன்மையையை வெளிப்படுத்துகிறது. இதனுடைய காடித்தன்மை சுட்டெண் 16-19 என்ற அளவில் உள்ளது. சோடியம் அல்லது சோடியம் ஐதரைடு போன்ற வலிமையான காரங்களுடன் இவை வினைபுரிந்து ஆல்காக்சைடுகளை உருவாக்குகின்றன. ஆல்காக்சைடுகளின் பொதுவான வாய்ப்பாடு RO− M+.ஆகும்.
இதற்கிடையில், ஆக்சிசன் அணுவானது சார்பற்ற அமிலங்களைக் கொண்ட தனி இணை எலக்ட்ரான்களைக் கொண்டுள்ளது, இது கந்தக அமிலம் போன்ற வலுவான அமிலங்கள் முன்னிலையில் பலவீனமான ஒரு காரத்தை அளிக்கிறது. உதாரணம் மெத்தனால்:
ஆல்ககால்களை ஆக்சிசனேற்றம் செய்து ஆல்டிகைடுகள், கீட்டோன்கள் அல்லது கார்பாக்சிலிக் அமிலங்களைத் தயாரிக்க முடியும். மேலும் ஆல்ககால்களை நீரிறக்கம் செய்து ஆல்கீன்களும் பெற முடியும். கார்பாக்சிலிக் அமிலங்களுடன் ஆல்ககால்கள் வினையில் ஈடுபட்டு எசுத்தர்களைக் கொடுக்கின்றன. இவை கருநாட்டப் பதிலீட்டு வினைகளில் ஈடுபடுகின்றன [28].
ஓரிணைய ஆல்ககாலில் இருந்து ஈரினைய ஆல்ககால் மற்றும் மூவிணைய ஆல்ககால் என அதே கட்டமைப்பில் உருவாகும் போது ஐதரசன் பிணைப்பின் வலிமை, கொதிநிலை, அமிலத்தன்மை முதலியன குறைகின்றன.
உற்பத்தி[தொகு]
சீக்ளர் மற்றும் ஆக்சோ செயல்முறை[தொகு]
சீக்ளர் செயல்முறையில் எத்திலீன் மற்றும் டிரையெத்தில் அலுமினியம் சேர்த்து தொடர்ந்து ஆக்சிசனேற்றம் மற்றும் நீராற்பகுப்பு வினைகள் [29] மூலம் நேர்கோட்டு ஆல்ககால்கள் உருவாக்கப்படுகின்றன. தனித்தன்மை மிக்க 1-ஆக்டனால் தயாரிக்கும் தொகுப்பு வினை இங்கு தரப்பட்டுள்ளது.
- Al(C2H5)3 + 9 C2H4 → Al(C8H17)3
- Al(C8H17)3 + 3 O + 3 H2O → 3 HOC8H17 + Al(OH)3
இவ்வினையில் உருவாகும் பல்வேறு ஆல்ககால்கள் காய்ச்சி வடித்தல் மூலம் பிரிக்கப்படுகின்றன.
ஐதரோபார்மைலேற்ற வினையைத் தொடர்ந்து ஐதரசனேற்றம் செய்வதால் ஆல்கீன்கள் உயர் ஆல்ககால்களைக் கொடுக்கின்றன. இதுவே விளிம்பு நிலை ஆல்ககால்களுக்கு பொதுவாகப் பயன்படுத்தினால் நேர்கோட்டு ஆல்ககால்கள் தோன்றுகின்றன :[29]. RCH=CH2 + H2 + CO → RCH2CH2CHO
- RCH2CH2CHO + 3 H2 → RCH2CH2CH2OH
இத்தகைய வினைகளால் கொழுப்பு ஆல்ககால்கள் தோன்ருகின்றன. இவை துப்புரவாக்கிகளில் பயன்படுகின்றன.
நீரேற்றம்[தொகு]
குறைந்த மூலக்கூற்று எடை கொண்ட தொழிற்துறை முக்கியத்துவம் உள்ள ஆல்ககால்கள் ஆல்கீன்களுடன் நிரைச் சேர்த்து தயாரிக்கப்படுகின்றன. எத்தனால், ஐசோபரோபனால், 2-பியூட்டனால் மற்றும் மூவிணைய பியூட்டனால் ஆகியவை இத்தலைய பொது முறையால் உற்பத்தி செய்யப்படுகின்றன. நேரடி முறை, மறைமுக முறை என்ற இரண்டு தயாரிப்பு முறைகள் இதற்காகப் பின்பற்றப்படுகின்றன. நேரடி முறையில் குறிப்பாக அமில வினையூக்கிகள் பயன்படுத்தி நிலைத்தன்மை மிகுந்த இடைநிலை விளைபொருட்கள் உருவாவது தடுக்கப்படுகிறது. மறைமுக முறையில் ஆல்கீன் சல்பேட்டு எசுத்தராக மாற்றப்படுகிறது. பின்னர் நீராற்பகுக்கப்படுகிறது. எத்திலீனைப் பயன்படுத்தி நேரடியான நீரேற்றம் [30] அல்லது பண்படுத்தா எண்ணெயை சிதைத்து பிற ஆல்கீன்கள் பெறப்படுகின்றன.
எத்திலீன் ஆக்சைடிலிருந்து எத்திலீன் கிளைக்காலை பேரளவில் தயாரிப்பதற்கும் நீரேற்ற முறை பயன்படுகிறது.
உயிரியல் பாதைகள்[தொகு]
37 ° செல்சியசுக்கு குறைவான வெப்பநிலையில் ஈசுடு முன்னிலையில், சிடார்ச்சை நீராற்பகுத்து குளுக்கோசு தயாரித்து பின்னர் நொதித்தல் முறையில் எத்தானால் தயாரிக்கப்படுகிறது. உதாரணமாக, சுக்ரோசை குளுக்கோசு மற்றும் பிரக்டோசாக மாற்றி பின்னர் சைமேசு நொதியால் குளுக்கோசை நொதிக்கச் செய்தும் எத்தனால் தயாரிக்கலாம்.
குடலில் உள்ள பல தீங்கற்ற பாக்டீரியாக்கள் நொதித்தலை வளர்சிதை மாற்றத்தின் ஒரு வடிவமாகப் பயன்படுத்துகின்றன. இந்த வளர்சிதைமாற்ற வினையில் எத்தனால் ஒரு கழிவுப்பொருளாக உற்பத்தி செய்யப்படுகிறது. அதாவது காற்றுச் சுவாசத்தில் கார்பன் டை ஆக்சைடும் மற்றும் நீரும் உருவாவது போல இங்கு எத்தனால் உருவாகிறது. இந்த பாக்டீரியாக்களால் உற்பத்தி செய்யப்படும் சில ஆல்ககால்கள் இவ்வாறுதான் மனித உடலில் சேர்ந்துக் கொண்டிருக்கின்றன. அரிதான சந்தர்ப்பங்களில், இது ஆல்ககால் அளவைக் கொணர்வதால் மது அருந்திய நோய்க்குறி ஏற்படுவதற்கு போதுமானதாக உள்ளது [31][32][33].
முதன்மை ஆல்கைல் ஆலைடுகள் நீர்த்த NaOH அல்லது KOH உடன் முக்கியமாக கருகவர் அலிபாட்டிக் பதிலீட்டு வினைகளில் முதனிலை ஆல்ககால்களைத் தருகின்றன. இரண்டாம் நிலை மற்றும் குறிப்பாக மூன்றாம் நிலை ஆல்கைல் ஆலைடுகள் நீக்கல் விளைபொருளாகத் தருகின்றன. கிரிக்னார்டு வினைப்பொருள்கள் கார்போனைல் குழுக்களுடன் வினைபுரிந்து இரண்டாம் மற்றும் மூன்றாம் நிலை ஆல்ககால்களைத் தருகின்றன. பார்பியர் வினை மற்றும் நொசாகி-இயாமா வினை போன்றவை இவ்வினையுடன் தொடர்புடைய வினைகளாகும். சோடியம் போரோ ஐதரைடு அல்லது இலித்தியம் அலுமினியம் ஐதரைடைப் பயன்படுத்தி ஆல்டிகைடுகள் அல்லது கீட்டோன்களை ஒடுக்கினால் ஆல்ககால்கள் உருவாக்கப்படுகின்றன. இதேபோல அலுமினியம் ஐசோபுரோப்பைலேட்டுகள் மீர்வெயின்-போண்டோர்ப்-வெர்லெய் ஒடுக்கம், நொயோரி சமச்சிரற்ற ஐதரசனேற்றம் போன்ற முறைகளிலும் இதைத் தயாரிக்கலாம்.
அடர் கந்தக அமிலத்தைப் பயன்படுத்தி அமில வினையூக்க நீரேற்ற வினையினால் ஈரிணைய அல்லது மூவிணைய ஆல்ககால்களைப் பெறலாம். ஆல்கீன்களை ஐதரோபோரானேற்றம்-ஆக்சிசனேற்றம் மற்றும் ஆக்சிபாதரசமேற்ற ஒடுக்கம் செய்யும் கரிமத் தொகுப்பு வினைகளாலும் இதைத் தயாரிக்கலாம். ஒடுக்கம் மற்றும் நீரேற்றம் மூலம் ஓர் இரண்டாம் நிலை ஆல்ககால் உருவாக்கம் இங்கு கொடுக்கப்பட்டுள்ளது.
வினைகள்[தொகு]
புரோட்டான் நீக்கவினை[தொகு]
ஆல்ககால்கள் வலிமை குறைந்த அமிலங்களாகச் செயல்பட்டு புரோட்டான் நீக்கம் அடைகின்றன. ஆனால் வலைமையான காரங்களுக்கு புரோட்டான்கள் தேவைப்படுகின்றன. சோடியம் ஐதரைடு அல்லது சோடியம் உலோகத்துடன் வலிமையான காரத்தைச் சேர்த்து வினைபுரியச் செய்து ஆல்காக்சைடு உப்பை புரோட்டான் நீக்க வினையின் மூலம் உருவாக்கலாம்.
2 R-OH + 2 NaH → 2 R-O−Na+ + 2 H2
2 R-OH + 2 Na → 2 R-O−Na+ + H2
தண்ணீரும் இதே அளவு pKa மதிப்பை பல ஆல்ககால்களுடன் சமமாகக் கொண்டுள்ளது. சோடியம் ஐதராக்சைடுடன் ஒரு சம்நிலையில் உள்ளது. இது பெரும்பாலும் இடது புறத்தில் இருக்கிறது.
R-OH + NaOH ⇌ R-O−Na+ + H2O (இடபபுறம் சமநிலையுடன்)
ஆல்ககால்களின் அமிலத்தன்மை கரைப்பானேற்றத்தால் கடுமையாகப் பாதிக்கப்படுகின்றன. வாயு நிலையில் ஆல்ககால்கள் தண்ணிரைக் காட்டிலும் அமிலத்தன்மை மிகுந்துள்ளன[34].
அணுக்கரு கவர் பதிலிட்டு வினைகள்[தொகு]
OH குழு அணுக்கரு கவர் பதிலிட்டு வினைகளில் ஒரு நல்ல விடுபடும் குழுவாக இருப்பதில்லை. எனவே நடுநிலை ஆல்ககால்கள் இவ்வகை வினைகளில் வினைபுரிவதில்லை.
இருப்பினும் ஆக்சிசன் முதலில் புரோட்டானேற்றம் அடைந்து R−OH2+,அயனியைக் கொடுக்கிறது. விடுபடும் குழுவான தண்ணிர் அதிக நிலைத்தன்மை கொண்டிருப்பதால் அணுக்கரு கவர் பதிலிட்டு வினை நிகழ்கிறது. உதாரணமாக மூவிணைய ஆல்ககால்கள் ஐதரோகுளோரிக் அமிலத்துடன் வினைபுரிந்து மூவிணைய ஆல்கைல் ஆலைடுகளைக் கொடுக்கின்றன. இங்கு ஐதராக்சில் குழுவானது குளோரின் அணுவால் ஒரு மூலக்கூறு கருகவர் பதிலீட்டு வினையால் நீக்கப்படுகிறது.
ஓரிணைய, ஈரிணைய ஆல்ககால்கள் ஐதரோகுளோரிக் அமிலத்துடன் வினைபுரிவதற்கு துத்தநாகக் குளோரைடு போன்ற ஒரு செயலூக்கி தேவைப்படுகிறது. மாறாக தயோனைல் குளோரைடைப் பயன்படுத்தினால் நேரடியாக மாற்றம் நிகழ்கிறது.
இவ்வாறே ஐதரோபுரோமிக் அமிலத்தைப் பயன்படுத்தினால் ஆல்ககால்கள் ஆல்கைல் புரோமைடுகளைக் கொடுக்கின்றன. மாற்றாக ஐதரோபுரோமிக் அமிலத்திற்குப் பதிலாக பாசுபரசு முப்புரோமைடையும் பயன்படுத்தலாம்.
- 3 R-OH + PBr3 → 3 RBr + H3PO3
உதாரணமாக பார்டன் மெக்கோம்பி ஆக்சிசன்நீக்க வினையில் ஓர் ஆல்ககால் ஆக்சிசன் நீக்கப்பட்டு ஓர் ஆல்கேன் உருவாகிறது.
நீர்நீக்க வினைகள்[தொகு]
ஆல்ககால்கள், அவைகளே அணுக்கரு கவரியாக இருப்பதால் R−OH2+ அயனியால் ROH உடன் வினைபுரிய முடிகிறது. நீர்நீக்க வினை நிகழ்ந்து ஈதர்களும் தண்ணீரும் உருவாகின்றன. டை ஈத்தைல் ஈத்தரை பேரளவில் தயாரிப்பதைத் தவிர்த்து இவ்வினை அரிதாகவே பயன்படுத்தப்படுகிறது.
ஆல்ககால்களில் இருந்து ஆல்க்கீனை உருவாக்குவதற்கு உதவும் இ1 வினைகளில் (இரு படிநிலைகளில் நிகழும் நீக்கல் வினை இ1 வினை எனப்படும்.)பொதுவாக இவ்வினை சையித்சேவ் விதிக்கு கட்டுப்படுகிறது. இவ்விதியில் குறிப்பிட்டுள்ளபடி அதிக நிலைத்தன்மையுள்ள அதாவது அதிக பதிலீசெய்யப்பட்டுள்ள ஆல்க்கீன் இவ்வினையில் உருவாகிறது. மூவிணைய ஆல்ககால்கள் எளிமையாக அறை வெப்பநிலையிலேயே நீக்கம் செய்கின்றன. ஆனால் ஓரிணைய ஆல்ககால்கள் நீக்கம் செய்ய அதிக வெப்பநிலை அவசியமாகிறது. எத்தனாலில் இருந்து எத்தீன் பெறப்பட அமில வினையூக்க நீர்நீக்க வினை பயன்படுகிறது என்பதை விளக்கும் வரைபடம் இங்கு கொடுக்கப்பட்டுள்ளது.
கார்பன் டைசல்பைடு மற்றும் ஐயோடோமெத்தேன் இரண்டும் வினைபுரியும் சுகேவ் நீக்கல்வினை கட்டுப்பாட்டிலுள்ள ஒரு நீக்கல் வினையாகும்.
எசுத்தராக்கல் வினை[தொகு]
ஒர் ஆல்ககால் மற்றும் ஒரு கார்பாக்சிலிக் அமிலம் ஆகியவற்றிலிருந்து எசுத்தரை உருவாக்கும் முறை பிசர் எசுத்தராக்கல் முறை எனப்படும். வழக்கமாக செறிவூட்டப்பட்ட கந்தக அமிலம் வினையூக்கியாக மறுசுழற்சி செய்யப்படுகிறது:
R-OH + R'-COOH → R'-COOR + H2O
அதிக அளவு எசுத்தர் உருவாக்கும் சமநிலையை உருவாக்க வினையில் விளையும் தண்ணிர் நீக்கப்படுகிறது. கந்தக அமிலத்தை அதிகமாக சேர்த்து அல்லது தீன்-சிடார்க்கு உபகரணம் மூலம் தண்ணீரை நீக்கலாம். பிரிடின் போன்ற காரத்தின் முன்னிலையில் ஓர் அமிலக் குளோரைடை ஆல்ககாலுடன் வினைபுரியச் செய்வதன் மூலமாகவும் எசுத்தரை தயாரிக்கலாம்.
பிறவகை எசுத்தர்களும் இதே முறையில் எசுத்தராக்கப்படுகின்றன. உதாரணமாக தொசில் எசுத்தர் ஆல்ககாலுடன் பாரா-தொகுயீன்சல்போனைல் குளோரைடு வினைபுரிவதால் உருவாகிறது.
ஆக்சிசனேற்றம்[தொகு]
ஓரிணைய ஆல்ககால்களை (R-CH2-OH) ஆக்சிசனேற்றம் செய்தால் ஆல்டிகைடுகள் (R-CHO) அல்லது கார்பாக்சிலிக் அமிலங்கள் (R-CO2H) உருவாகின்றன. ஈரிணைய ஆல்ககால்களை (R1R2CH-OH) ஆக்சிசனேற்றம் செய்தால் அவை கீட்டோன்களைத் தருகின்றன. மூவிணைய ஆல்ககால்களில் ஆக்சிசனேற்றம் நிகழ்வதில்லை. நேரடியாக ஓரினைய ஆல்ககால்களை கார்பாக்சிலிக் அமிலங்களாக ஆக்சிசனேற்றம் செய்யும்போது தொடர்புடைய ஆல்டிகைடு வழியாகவே வினை நிகழ்கிறது. இவ்வினையும் கார்பாக்சிலிக் அமிலமாக மாறுவதற்கு முன்னர் நீருடன் வினைபுரிந்து ஆல்டிகைடு நீரேற்று (R-CH(OH)2) உருவாகிய பின்னர் மாற்றமடைகிறது.
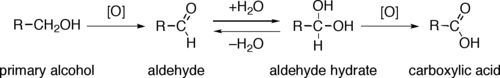
ஓரிணைய ஆல்ககால்களை ஆல்டிகைடுகளாக மாற்றுவதற்குப் பயன்படும் வினையாக்கிகளே ஈரிணைய ஆல்ககால்களை கீட்டோன்களாக மாற்றவும் பயன்படுகின்றன. காலின்சு வினையாக்கி, தெசு-மார்டின் பீரியாதினேன் போன்ற வினையாக்கிகள் இதற்கு உதவுகின்றன. பொட்டாசியம் பெர்மாங்கனேட்டு அல்லது யோன்சு வினையாக்கி ஓரிணைய ஆல்ககால்களை நேரடியாக கார்பாக்சிலிக் அமிலமாக மாற்ற உதவுகிறது.
மேற்கோள்கள்[தொகு]
- ↑ "alcohols". IUPAC Gold Book. பார்க்கப்பட்ட நாள் 16 December 2013.
- ↑ தனி மற்றும் பயன்பாட்டு வேதியியல் அனைத்துலக ஒன்றியம். "Alcohols". Compendium of Chemical Terminology Internet edition.
- ↑ http://www.etymonline.com/index.php?allowed_in_frame=0&search=alcohol
- ↑ Lohninger, H. "VIAS Encyclopedia: Etymology of the Word "Alcohol"". vias.org.
- ↑ 5.0 5.1 William Reusch. "Alcohols". VirtualText of Organic Chemistry. Archived from the original on 19 September 2007. பார்க்கப்பட்ட நாள் 14 September 2007.
- ↑ Organic chemistry IUPAC nomenclature. Alcohols Rule C-201.
- ↑ "How to name organic compounds using the IUPAC rules". www.chem.uiuc.edu. THE DEPARTMENT OF CHEMISTRY AT THE UNIVERSITY OF ILLINOIS. பார்க்கப்பட்ட நாள் 14 November 2016.
- ↑ Reusch, William. "Nomenclature of Alcohols". chemwiki.ucdavis.edu/. பார்க்கப்பட்ட நாள் 17 March 2015.
- ↑ "Molecule Gallery - Alcohols". பார்க்கப்பட்ட நாள் 31 December 2013.
- ↑ Zverlov, W; Berezina, O; Velikodvorskaya, GA; Schwarz, WH (August 2006). "Bacterial acetone and butanol production by industrial fermentation in the Soviet Union: use of hydrolyzed agricultural waste for biorefinery.". Applied Microbiology Technology 71 (5): 587–97. doi:10.1007/s00253-006-0445-z. பப்மெட்:16685494.
- ↑ "alcohol (chemical compound)". Encyclopædia Britannica. அணுகப்பட்டது 31 December 2013.
- ↑ "Alcohols, Phenols, Thiols, and Ethers". Chemistry - Louisiana Tech University. Archived from the original on 2 அக்டோபர் 2013. பார்க்கப்பட்ட நாள் 31 December 2013.
- ↑ Analytical Toxicology for Clinical, Forensic and Pharmaceutical Chemists. 1997. பக். 401. பன்னாட்டுத் தரப்புத்தக எண்:3-11-010731-7. https://books.google.com/books?id=ZhYtynyC4kAC&pg=PA401#v=onepage&q&f=false.
- ↑ D. W. Yandell (1888). "Amylene hydrate, a new hypnotic". The American Practitioner and News (Louisville KY: John P. Morton & Co) 5: 88–89. https://books.google.com/books?id=Ra5YAAAAMAAJ&pg=PA88#v=onepage.
- ↑ Carey, Francis. Organic Chemistry (4 ). பன்னாட்டுத் தரப்புத்தக எண்:0072905018. http://www.mhhe.com/physsci/chemistry/carey/student/olc/ch15oxidationalcohols.html. பார்த்த நாள்: 5 February 2013.
- ↑ Brooks PJ (1997). "DNA damage, DNA repair, and alcohol toxicity-a review". Alcoholism: Clinical and Experimental Research 21 (6): 1073–1082. doi:10.1111/j.1530-0277.1997.tb04256.x.
- ↑ "Alcohol consumption and site-specific cancer risk: a comprehensive dose-response meta-analysis". British Journal of Cancer 112 (3): 580–93. 2015. doi:10.1038/bjc.2014.579. பப்மெட்:25422909.
- ↑ http://www.otago.ac.nz/news/news/otago617874.html[full citation needed]
- ↑ "oxidation of alcohols". chemguide.co.uk.
- ↑ "Methylparafynol--a new type hypnotic. Preliminary report on its therapeutic efficacy and toxicity". American practitioner and digest of treatment 3 (1): 23–26. 1952. பப்மெட்:14903452.
- ↑ Adriani, John (1962). The Chemistry and Physics of Anesthesia. Second Edition. Illinois: Thomas Books. பக். 273–274. பன்னாட்டுத் தரப்புத்தக எண்:9780398000110.
- ↑ 22.0 22.1 "A seaman with blindness and confusion". BMJ 339: b3929. 30 September 2009. doi:10.1136/bmj.b3929. பப்மெட்:19793790. http://www.bmj.com/cgi/content/full/339/sep30_1/b3929.
- ↑ "ChemIDplus Advanced - Chemical information with searchable synonyms, structures, and formulas". nih.gov.
- ↑ Zimmerman, HE; Burkhart, KK; Donovan, JW (1999). "Ethylene glycol and methanol poisoning: diagnosis and treatment". Journal of Emergency Nursing 25 (2): 116–20. doi:10.1016/S0099-1767(99)70156-X. பப்மெட்:10097201. https://archive.org/details/sim_journal-of-emergency-nursing_1999-04_25_2/page/116.
- ↑ Lobert, S (2000). "Ethanol, isopropanol, methanol, and ethylene glycol poisoning". Critical care nurse 20 (6): 41–7. பப்மெட்:11878258. https://archive.org/details/sim_critical-care-nurse_2000-12_20_6/page/41.
- ↑ Charnley, S. B.; Kress, M. E.; Tielens, A. G. G. M.; Millar, T. J. (1995). "Interstellar Alcohols". Astrophysical Journal 448: 232. doi:10.1086/175955. Bibcode: 1995ApJ...448..232C. http://hdl.handle.net/2060/19970007168.
- ↑ Giant cloud of space alcohol found பரணிடப்பட்டது 2016-11-17 at the வந்தவழி இயந்திரம் labnews.co.uk/
- ↑ Sfetcu, Nicolae (2014). Health & Drugs Disease, Prescription & Medication. North Carolina: Lulu.com. பன்னாட்டுத் தரப்புத்தக எண்:9781312039995.
- ↑ 29.0 29.1 Jürgen Falbe, Helmut Bahrmann, Wolfgang Lipps, Dieter Mayer "Alcohols, Aliphatic" in Ullmann's Encyclopedia of Chemical Technology Wiley-VCH Verlag; Weinheim, 2002. எஆசு:10.1002/14356007.a01_279
- ↑ Lodgsdon J.E. (1994). "Ethanol". in Kroschwitz J.I.. Encyclopedia of Chemical Technology. 9 (4th ). New York: John Wiley & Sons. பக். 820. பன்னாட்டுத் தரப்புத்தக எண்:0-471-52677-0.
- ↑ P. Geertinger MD; J. Bodenhoff; K. Helweg-Larsen; A. Lund (1 September 1982). "Endogenous alcohol production by intestinal fermentation in sudden infant death". Zeitschrift für Rechtsmedizin (Springer-Verlag) 89 (3): 167–172. doi:10.1007/BF01873798.
- ↑ "Endogenous ethanol 'auto-brewery syndrome' as a drunk-driving defence challenge". Medicine, science, and the law 40 (3): 206–15. July 2000. பப்மெட்:10976182.
- ↑ Cecil Adams (20 October 2006). "Designated drunk: Can you get intoxicated without actually drinking alcohol?". The Straight Dope. பார்க்கப்பட்ட நாள் 27 February 2013.
- ↑ வார்ப்புரு:March6th
புற இணைப்புகள்[தொகு]
![]() விக்சனரி விக்சனரி
விக்சனரி விக்சனரி
![]() நூல்கள் விக்கிநூல்
நூல்கள் விக்கிநூல்
![]() மேற்கோள் விக்கிமேற்கோள்
மேற்கோள் விக்கிமேற்கோள்
![]() மூலங்கள் விக்கிமூலம்
மூலங்கள் விக்கிமூலம்
![]() விக்கிபொது
விக்கிபொது
![]() செய்திகள் விக்கிசெய்தி
செய்திகள் விக்கிசெய்தி
- Alcohol (Ethanol) at The Periodic Table of Videos (University of Nottingham)



