வெள்ளிக் கார்பனேட்டு
| |

| |
| பெயர்கள் | |
|---|---|
| ஐயூபிஏசி பெயர்
வெள்ளி(I) கார்பனேட்டு, வெள்ளி கார்பனேட்டு
| |
| இனங்காட்டிகள் | |
| 534-16-7 | |
| ChemSpider | 83768 |
| EC number | 208-590-3 |
| யேமல் -3D படிமங்கள் | Image |
| ம.பா.த | silver+carbonate |
| பப்கெம் | 92796 |
SMILES
| |
| UNII | V9WU3IKN4Q |
| பண்புகள் | |
| CAg2O3 | |
| வாய்ப்பாட்டு எடை | 275.74 g·mol−1 |
| தோற்றம் | வெளிர் மஞ்சள் படிகங்கள் |
| மணம் | மணமற்றது |
| அடர்த்தி | 6.077 கி/செ.மீ3 |
| உருகுநிலை | 218 °C (424 °F; 491 K) decomposes from 120 °C[3][4] |
| 0.031 g/L (15 °C) 0.032 g/L (25 °C) 0.5 g/L (100 °C)[1] | |
கரைதிறன் பெருக்கம் (Ksp)
|
8.46·10−12 |
| கரைதிறன் | ஆல்ககால், திரவ அமோனியா, அசிடேட்டுகள், அசிட்டோன் ஆகியவற்றில் கரையாது.[2] |
| −8.09·10−5 cm3/mol | |
| கட்டமைப்பு | |
| படிக அமைப்பு | ஒற்றைச்சரிவு, mP12 (295 K) முக்கோணம், hP36 (β-form, 453 K) அறுகோணம், hP18 (α-form, 476 K)[5] |
| புறவெளித் தொகுதி | P21/m, No. 11 (295 K) P31c, No. 159 (β-form, 453 K) P62m, No. 189 (α-form, 476 K)[5] |
| வெப்பவேதியியல் | |
| Std enthalpy of formation ΔfH |
−505.8 கியூ/மோல் |
| நியம மோலார் எந்திரோப்பி S |
167.4 யூ/மோல்·K |
| வெப்பக் கொண்மை, C | 112.3 யூ/மோல்·K |
| தீங்குகள் | |
| GHS pictograms |  [6] [6]
|
| GHS signal word | Warning |
| H315, H319, H335[6] | |
| P261, P305+351+338[6] | |
| S-சொற்றொடர்கள் | S26, S36 |
| உள்மூச்சு இடர் | எரிச்சலூட்டும் |
| Lethal dose or concentration (LD, LC): | |
LD50 (Median dose)
|
3.73 கி/கி.கி (எலி, வாய்வழி)[7] |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
| | |
| Infobox references | |
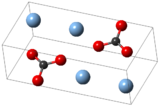
வெள்ளி கார்பனேட்டு (Silver carbonate) என்பது Ag2CO3 என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட ஒரு வேதிச் சேர்மம் ஆகும். மஞ்சள் நிறத்துடன் காணப்படும் இச்சேர்மத்தின் சில மாதிரிகள், தனிமநிலை வெள்ளி இடம்பெறும் மாதிரிகள் சாம்பல் நிறத்தில் காணப்படுகின்றன. தாண்டல் உலோகங்களின் கார்பனேட்டுகள் போல வெள்ளி கார்பனேட்டும் தண்ணீரில் மிகச் சிறிதளவே கரைகிறது.
சோடியம் கார்பனேட்டு மற்றும் வெள்ளி நைட்ரேட் உப்புகளின் நீர்த்த கரைசல்களை சேர்ப்பதனால் வெள்ளி கார்பனேட்டு உருவாகிறது. புதியதாக உருவாகும் வெள்ளி கார்பனேட்டு நிறமற்றதாக இருக்கும் , ஆனால் விரைவாக இது மஞ்சள் நிறத் திண்மமாக மாறிவிடும்.[8] அமோனியாவுடன் வெள்ளி கார்பனேட்டு வினைபுரிந்து வெள்ளி பல்மினேட்டு என்ற வெடிபொருள் உருவாகிறது. இவ்வாறே ஐதரோ புளோரிக் அமிலத்துடன் வெள்ளி கார்பனேட்டு வினைபுரிந்து வெள்ளி புளோரைடு உருவாகிறது.
பயன்கள்[தொகு]
நுண்மின்னியல் துறைக்குத் தேவையான வெள்ளித் தூள் தயாரிப்பில் வெள்ளி கார்பனேட் முக்கியப்பங்கு வகிக்கிறது. வெள்ளி கார்பனேட்டுடன் பார்மால்டிகைடு சேர்த்து ஒடுக்க வினைக்கு உட்படுத்துவதால் வெள்ளியில்லாத காரவுலோகங்களை உற்பத்தி செய்யமுடிகிறது:[8]
- Ag2CO3 + CH2O → 2 Ag + 2 CO2 + H2
கரிமத் தொகுப்புமுறை தயாரிப்பு வினைகளில் வெள்ளி கார்பனேட்டு ஒரு வினைப்பொருள் அல்லது செயலியாக பயன்படுத்தப்படுகிறது. உதாரணம்: கொயினிக்சு – குநோர் வினை. பேட்டிசான் வினை ஆக்சிசனேற்ற வினையில் டையால்களில் இருந்து லாக்டோன் தயாரிப்பதில் சீலைட்டை ஆக்சிசனேற்றம் செய்யும் செயலியாக வெள்ளி கார்பனேட்டு பயன்படுகிறது[9]
மேற்கோள்கள்[தொகு]
- ↑ Seidell, Atherton; Linke, William F. (1919). Solubilities of Inorganic and Organic Compounds (2nd ). New York: D. Van Nostrand Company. பக். 605. https://archive.org/details/solubilitiesino01seidgoog.
- ↑ Comey, Arthur Messinger; Hahn, Dorothy A. (1921-02). A Dictionary of Chemical Solubilities: Inorganic (2nd ). New York: The MacMillan Company. பக். 203. https://archive.org/details/dictionaryofchem00comerich.
- ↑ Lide, David R., தொகுப்பாசிரியர் (2009). CRC Handbook of Chemistry and Physics (90th ). Boca Raton, Florida: CRC Press]isbn = 978-1-4200-9084-0.
- ↑ Anatolievich, Kiper Ruslan. "silver nitrate". chemister.ru. பார்க்கப்பட்ட நாள் 2014-07-21.
- ↑ 5.0 5.1 Norby, P.; Dinnebier, R.; Fitch, A.N. (2002). "Decomposition of Silver Carbonate; the Crystal Structure of Two High-Temperature Modifications of Ag2CO3". Inorganic Chemistry 41 (14). doi:10.1021/ic0111177.
- ↑ 6.0 6.1 6.2 Sigma-Aldrich Co., Silver carbonate. Retrieved on 2014-05-06.
- ↑ 7.0 7.1 "Silver Carbonate MSDS". http://www.saltlakemetals.com. Salt Lake City, Utah: Salt Lake Metals. பார்க்கப்பட்ட நாள் 2014-06-08.
{{cite web}}: External link in|website= - ↑ 8.0 8.1 Andreas Brumby et al. "Silver, Silver Compounds, and Silver Alloys" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2008. எஆசு:10.1002/14356007.a24_107.pub2
- ↑ McCloskey C. M.; Coleman, G. H. (1955). "β-d-Glucose-2,3,4,6-Tetraacetate". Organic Syntheses. http://www.orgsyn.org/demo.aspx?prep=cv3p0434.; Collective Volume, vol. 3, p. 434
