இரும்பு(II) அசிட்டேட்டு
| |
| பெயர்கள் | |
|---|---|
| ஐயூபிஏசி பெயர்
இரும்பு(II) அசிட்டேட்டு
| |
| வேறு பெயர்கள்
பெரசு அசிட்டேட்டு
| |
| இனங்காட்டிகள் | |
| 3094-87-9 | |
| ChemSpider | 17323 |
| யேமல் -3D படிமங்கள் | Image
ஒருங்கிணைவு வடிவம் |
| பப்கெம் | 18344 |
| வே.ந.வி.ப எண் | AI3850000 |
| |
| UNII | L80I7M6D3Q |
| பண்புகள் | |
| C4H6FeO4 | |
| வாய்ப்பாட்டு எடை | 173.93 g·mol−1 |
| தோற்றம் | வெண் படிகங்கள் (நீரிலி) இளம் பச்சை நிறப் படிகங்கள் (நான்கு நீரேற்று) |
| மணம் | Odorless |
| அடர்த்தி | 1.734 கி/செ.மீ3 (−73 °C)[1] |
| உருகுநிலை | 190–200 °C (374–392 °F; 463–473 K) decomposes[2][3] |
| கரையும்[2] | |
| கட்டமைப்பு | |
| படிக அமைப்பு | Orthorhombic, oP75 (200 K) |
| புறவெளித் தொகுதி | Pbcn, எண். 60 (200 K)[1] |
| Lattice constant | a = 18.1715(4) Å, b = 22.1453(5) Å, c = 8.2781(2) Å (200 K) |
படிகக்கூடு மாறிலி
|
|
| தீங்குகள் | |
| GHS pictograms |  [3] [3]
|
| GHS signal word | எச்சரிக்கை |
| H315, H319, H335[3] | |
| P261, P305+351+338[3] | |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
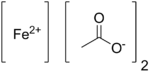
இரும்பு(II) அசிட்டேட்டு (Iron(II) acetate) என்பது Fe(CH3COO)2 என்ற மூலக்கூற்று வாய்ப்பாட்டால் விவரிக்கப்படும் ஒரு கனிம வேதியியல் ஒருங்கிணைவு அணைவுச் சேர்மமாகும். அசுத்த மாதிரிகள் சிறிது நிறத்தில் இருந்தாலும் இது ஒரு வெள்ளை நிற திண்மப் பொருளாகும்.[1] ஓர் இளம் பச்சை நிற நான்கு நீரேற்று அறியப்படுகிறது. இது தண்ணீரில் நன்றாகக் மிகவும் கரையும்.
தயாரிப்பு
[தொகு]
இரும்புத் தூள் மின்னாற்பகுப்பில் அசிட்டிக் அமிலத்துடன் வினைபுரிந்து ஐதரசன் வாயுவை வெளியேற்றி இரும்பு அசிடேட்டைக் கொடுக்கிறது.[1]
- Fe + 2 CH3CO2H → Fe(CH3CO2)2 + H2
இரும்பு ஆக்சைடு அல்லது இரும்பு ஐதராக்சைடுடன் அசிட்டிக் அமிலத்தைச் சேர்த்து வினைபுரியச் செய்தால் நீரேற்றப்பட்ட இரும்பு(II) அசிட்டேட்டு வடிவம் உருவாக்கப்படுகிறது.[5]
அசிட்டிக் அமிலத்துடன் இரும்புத் துண்டுகளை சேர்த்து வினைபுரியச் செய்யும் போது பல்வேறு இரும்பு(II) மற்றும் இரும்பு(III) அசிடேட்டுகளின் பழுப்பு நிற சேர்மம் கிடைக்கிறது. இது சாயமிடுதலில் பயன்படுத்தப்படுகிறது.[6]
கட்டமைப்பு
[தொகு]அசிடேட்டு ஈந்தணைவிகள் ஒன்றோடொன்று இணைக்கப்பட்ட எண்முக Fe(II) மையங்களைக் கொண்ட பல்லுருவக் கட்டமைப்பை இரும்பு(II) அசிட்டேட்டு ஏற்றுக்கொள்கிறது. இது ஓர் ஒருங்கிணைப்பு பலபடியாகும்.
பயன்கள்
[தொகு]சாயத் தொழிலில் இரும்பு அசிடேட்டு ஒரு நிறங்கௌவி சாயமாகப் பயன்படுத்தப்படுகிறது. கருங்காலி மரத்தை உருவாக்குவது இத்தகைய ஒரு செயல்முறையாகும்.[7]
மேற்கோள்கள்
[தொகு]- ↑ 1.0 1.1 1.2 1.3 1.4 Weber, Birgit; Betz, Richard; Bauer, Wolfgang; Schlamp, Stephan (2011). "Crystal Structure of Iron(II) Acetate". Zeitschrift für anorganische und allgemeine Chemie 637: 102–107. doi:10.1002/zaac.201000274.
- ↑ 2.0 2.1 Lide, David R., ed. (2009). CRC Handbook of Chemistry and Physics (90th ed.). Boca Raton, Florida: CRC Press]isbn = 978-1-4200-9084-0.
- ↑ 3.0 3.1 3.2 3.3 Sigma-Aldrich Co., Iron(II) acetate. Retrieved on 2014-05-03.
- ↑ "MSDS of Ferrous acetate". fishersci.ca. Fair Lawn: Fisher Scientific. பார்க்கப்பட்ட நாள் 2014-08-02.
- ↑ "Synthesis of Iron(II) acetate hydrate (ferrous acetate)". Archived from the original on 2013-08-25. பார்க்கப்பட்ட நாள் 2009-01-07.
- ↑ Wildermuth, Egon; Stark, Hans; Friedrich, Gabriele; Ebenhöch, Franz Ludwig; Kühborth, Brigitte; Silver, Jack; Rituper, Rafael (2005), "Iron Compounds", Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, எண்ணிம ஆவணச் சுட்டி:10.1002/14356007.a14_591
- ↑ Ebonizing Wood with Ferric Acetate
