பெர்மாங்கனேட்டு

| |
| |
| பெயர்கள் | |
|---|---|
| முறையான ஐயூபிஏசி பெயர்
பெர்மாங்கனேட்டு | |
| பண்புகள் | |
| MnO− 4 | |
| வாய்ப்பாட்டு எடை | 118.93 g·mol−1 |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
| Infobox references | |
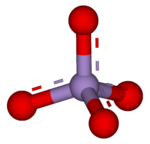
பெர்மாங்கனேட்டு அல்லது பரமங்கனேற்று (Permanganate) என்பது மாங்கனேட்டு (VII) அயனியைப் பெற்றுள்ள வேதிச் சேர்மத்தின் பெயர் ஆகும். இவ்வயனியில் மாங்கனீசு +7 ஆக்சிசனேற்ற நிலையில் உள்ளது. பெர்மாங்கனேட்டு(VII) ஒரு வலிமையான ஆக்சிசனேற்றியாகும். இவ்வயனி நான்குமுக படிக வடிவமைப்பைக் கொண்டுள்ளது[1]. பெர்மாங்கனேட்டு கரைசல்கள் பெரும்பாலும் கருஞ்சிவப்பு வண்ணத்தில் காணப்படும். நடுநிலை அல்லது இலேசான காரக் கரைசல் ஊடகத்தில் இது நிலைப்புத்தன்மையுடன் காணப்படுகிறது. உபயோகப்படுத்தப்படும் ஆக்சிசனேற்றிகள் கலந்துள்ள மாசுக்கள் இவற்றைப் பொருத்து இதனுடைய வேதிப் பண்புகள் அமைகின்றன. உதாரணமாக சோடியம் பெர்மாங்கனேட்டால் ஆக்சிசனேற்றம் செய்யப்படும் முக்குளோரோ ஈத்தேனில் இருந்து கார்பன் டை ஆக்சைடு, மாங்கனீசு டை ஆக்சைடு, சோடியம் அயனிகள், ஐதரோனியம் அயனிகள், குளோரைடு அயனிகள் ஆகியன உருவாகின்றன[2]
பெர்மாங்கனேட்டு(VII) நீர்த்த அமிலக் கரைசலில் +2 ஆக்சிசனேற்ற நிலையில் உள்ள மாங்கனீசு(II) அயனியாக குறைக்கப்படுகிறது.
- 8 H+
+ MnO4− + 5 e− → Mn2+ + 4 H2O
வலிமையான காரக் கரைசலுடன் சேர்ந்து பெர்மாங்கனேட்டு(VII) +6 ஆக்சிசனேற்ற நிலையில் உள்ள மாங்கனேட்டு அயனியாக குறைகிறது
- MnO4− + e− → MnO42−
நடுநிலைச் சூழலில் பெர்மாங்கனேட்டு(VII) +4 ஆக்சிசனேற்ற நிலையில் உள்ள பழுப்பு நிற மாங்கனீசு ஈராக்சைடாக ஒடுங்குகிறது.
- 2 H2O + MnO4− + 3 e− → MnO2 + 4 OH−
தயாரிப்பு[தொகு]
மாங்கனீசு குளோரைடு அல்லது மாங்கனீசு சல்பேட்டு போன்ற மாங்கனீசு சேர்மங்கள் வலிமையான ஆக்சிசனேற்றிகளான சோடியம் ஐப்போகுளோரைட் அல்லது ஈய ஈராக்சைடுகளால் ஆக்சிசனேற்றப்பட்டு பெர்மாங்கனேட்டுகள் உருவாகின்றன.
- 2 MnCl2 + 5 NaClO + 6 NaOH → 2 NaMnO4 + 9 NaCl+ 3 H2O
- 2 MnSO4 + 5 PbO2+ 3 H2SO4 → 2 HMnO4 + 5 PbSO4 + 2 H2O
மாங்கனேட்டுகள் விகிதச்சமமாதலின்றி பிரிகை அடையும் போது உடன் விளையும் மாங்கனீசு ஈராக்சைடுடன் பெர்மாங்கனேட்டுகள் உருவாகின்றன.
- 3 Na2MnO4 + 2 H2O → 2 NaMnO4 + MnO2 + 4 NaOH
மாங்கனேட்டு உப்புகளின் காரக் கரைசலை மின்னாற்பகுப்பு செய்தல் அல்லது காற்றினால் ஆக்சிசனேற்றம் செய்தல் முறைகளில் வர்த்தக நோக்கிலான பெர்மாங்கனேட்டுகள் தயாரிக்கப்படுகின்றன.[3]
பண்புகள்[தொகு]
பெர்மாங்கனிக் அமிலத்தினுடைய உப்புகள் பெர்மாங்கனேட்டுகள்(VII) என்பனவாகும். இவை பெர்குளோரேட்டுகள் போல வலிமையான ஆக்சிசனேற்றிகளாகச் செயல்படுகின்றன. ஆக்சிசனேற்ற ஒடுக்க வினைகளில் பங்கேற்கும் இவை அளவறி பகுப்பாய்வில் பொதுவாகப் பயன்படுத்தப்படுகின்றன.
கோட்பாடுகளின் அடிப்படையில் நீரை ஆக்சிசனேற்றம் செய்யும் அளவுக்கு பெர்மாங்கனேட்டுகள் வலிமை கொண்டவை என்றாலும் இந்நிலை எப்போதுமே ஏற்படாது. இதைத் தவிர இது, நிலைப்புத் தன்மையுடைய ஒரு உபயோகமுள்ள கரிமச் சேர்மங்களுக்கான வினைப்பொருளாகும்.
மாங்கனேட்டு(VII) சேர்மங்கள் வெப்பத்தில் அதிக நிலைப்புத் தன்மையுடன் இருப்பதில்லை. உதாரணமாக 230 0 செ வெப்பநிலையில் பொட்டாசியம் பெர்மாங்கனேட்டு சேர்மமானது ஆக்சிசனை வெளியேற்றி பொட்டாசியம் மாங்கனேட்டு மற்றும் மாங்கனீசு ஈராக்சைடாக சிதைவடைகிறது.
- 2 KMnO4 → K2MnO4 + MnO2 + O2
ஓர் அமீனை நைட்ரோ சேர்மமாக,[4][5] ஒர் ஆல்ககாலை கீட்டோனாக[6], ஆல்டிகைடை கார்பாக்சிலிக் அமிலமாக[7][8] , ஒரு விளிம்புநிலை ஆல்க்கீனை கார்பாக்சிலிக் அமிலமாகவும்[9] ஆக்சாலிக் அமிலத்தை கார்பன் டை ஆக்சைடாக[10] மற்றும் ஒர் ஆல்க்கீனை டையால்[11] ஆகவும் பெர்மாங்கனேட்டால் ஆக்சிசனேற்றம் செய்ய முடியும். இவ்வாறு நீளும் இப்பட்டியல் இன்னும் நிறைவடையவில்லை என்பது குறிப்பிடத்தகுந்தது.
ஆல்க்கீன் ஆக்சிசனேற்ற வினைகளில் வளைய மாங்கனீசு(V) சேர்மம் ஒரு இடைநிலையாகத் தோன்றுகிறது.
மேற்கோள்கள்[தொகு]
- ↑ Sukalyan Dash, Sabita Patel and Bijay K. Mishra (2009). "Oxidation by permanganate: synthetic and mechanistic aspects". Tetrahedron 65 (4): 707–739. doi:10.1016/j.tet.2008.10.038.
- ↑ http://geocleanse.com/permanaganate.asp
- ↑ Cotton, F. Albert; Wilkinson, Geoffrey; Carlos A. Murillo; Manfred Bochmann (1999). Advanced Inorganic Chemistry (6th ). New York: John Wiley & Sons, Inc.. பக். 770. பன்னாட்டுத் தரப்புத்தக எண்:978-0471199571. https://archive.org/details/advancedinorgani0000unse.
- ↑ A. Calder, A. R. Forrester1, and S. P. Hepburn (1972). "2-methyl-2-nitrosopropane and its dimer". Organic Syntheses 6: 803. http://www.orgsyn.org/demo.aspx?prep=CV6P0803.; Collective Volume, vol. 52, p. 77
- ↑ Nathan Kornblum and Willard J. Jones (1963). "4-nitro-2,2,4-trimethylpentane". Organic Syntheses 5: 845. http://www.orgsyn.org/demo.aspx?prep=CV5P0845.; Collective Volume, vol. 43, p. 87
- ↑ J. W. Cornforth (1951). "Ethyl pyruvate". Organic Syntheses 4: 467. http://www.orgsyn.org/demo.aspx?prep=CV4P0467.; Collective Volume, vol. 31, p. 59
- ↑ R. L. Shriner and E. C. Kleiderer (1930). "Piperonylic acid". Organic Syntheses 2: 538. http://www.orgsyn.org/demo.aspx?prep=CV2P0538.; Collective Volume, vol. 10, p. 82
- ↑ John R. Ruhoff (1936). "n-heptanoic acid". Organic Syntheses 2: 315. http://www.orgsyn.org/demo.aspx?prep=CV2P0315.; Collective Volume, vol. 16, p. 39
- ↑ Donald G. Lee, Shannon E. Lamb, and Victor S. Chang (1981). "Carboxylic acids from the oxidation of terminal alkenes by permanganate: nonadecanoic acid". Organic Syntheses 7: 397. http://www.orgsyn.org/demo.aspx?prep=CV7P0397.; Collective Volume, vol. 60, p. 11
- ↑ Kovacs KA, Grof P, Burai L, Riedel M (2004). "Revising the Mechanism of the Permanganate/Oxalate Reaction". J. Phys. Chem. A 108 (50): 11026. doi:10.1021/jp047061u.
- ↑ E. J. Witzemann, Wm. Lloyd Evans, Henry Hass, and E. F. Schroeder (1931). "dl-glyceraldehyde ethyl acetal". Organic Syntheses 2: 307. http://www.orgsyn.org/demo.aspx?prep=CV2P0307.; Collective Volume, vol. 11, p. 52
சேர்மங்கள்[தொகு]
- அமோனியம் பெர்மாங்கனேட்டு, NH4MnO4
- கால்சியம் பெர்மாங்கனேட்டு, Ca(MnO4)2
- பொட்டாசியம் பெர்மாங்கனேட்டு, KMnO4
- சோடியம் பெர்மாங்கனேட்டு, NaMnO4
- வெள்ளி பெர்மாங்கனேட்டு, AgMnO4

