கார உலோக ஆலைடு
கார உலோக ஆலைடுகள் (Alkali metal halides) என்பவை MX என்ற பொது வாய்ப்பாட்டில் அமைந்த கனிம வேதியியல் சேர்மங்களாகும். இங்கு M என்பது கார உலோகத்தையும் X என்பது ஆலசனையும் குறிக்கிறது. இச்சேர்மம் கார ஆலைடுகள் என்றும் அழைக்கப்படுகின்றன. கார உலோக ஆலைடுகள் இவற்றின் பகுதிப் பொருட்களாக உள்ள உலோகங்களுக்கும் ஆலைடுகளுக்கும் வர்த்தகரீதியிலான மூலப்பொருளாக உள்ளன. நன்கு அறியப்பட்ட கார உலோக ஆலைடு மேசை உப்பு எனப்படும் சோடியம் குளோரைடு ஆகும்.[1]

அமைப்பு
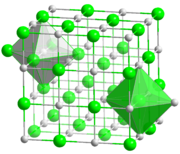
[தொகு]பெரும்பாலான கார உலோக ஆலைடுகள் முக மைய கனசதுர அணிக்கோவைகளாக படிகமாகின்றன. இவ்வமைப்பில், உலோகங்கள், ஆலைடுகள் இரண்டுமே எண்முக ஒருங்கிணைப்பு வடிவம் கொண்டுள்ளன. ஒவ்வொரு அயனியும் 6 என்ற அணைவு எண்ணைக் கொண்டுள்ளன. சீசியம் குளோரைடு, சீசியம் புரோமைடு மற்றும் சீசியம் அயோடைடு ஆகிய சேர்மங்கள் பொருள் மைய கனசதுர அணிக்கோவைகளாக படிகமாகின்றன. இதில் உள்ள ஒவ்வொரு அயனியும் 6 என்ற அணைவு எண்ணைக் கொண்டுள்ளன.[2]

பண்புகள்
[தொகு]நிறமற்ற படிகத் திண்மங்களாக கார உலோக ஆலைடுகள் காணப்படுகின்றன. பொடியாக அரைக்கப்பட்ட தூளாக இருக்கும் போது இவை வெண்மையாகக் காணப்படுகின்றன. மிக அதிக உருகுநிலை கொண்டுள்ள இச்சேர்மங்கள் பலநூறு பாகைகள் வெப்பநிலைக்கு பின்னரே திரவமாகின்றன. இச்சேர்மங்களின் அதிகமான உருகுநிலை இவற்றின் உயர் அணிக்கோவை ஆற்றல் மதிப்பைப் வெளிப்படுத்துகிறது. மிகவுயர் வெப்பநிலையில் இத்திரவங்கள் ஆவியாக மாற்றமடைந்து ஈரணு மூலக்கூற்று வாயுக்களைத் தருகின்றன.
முனைவுக் கரைப்பான்களில் கரைந்து இச்சேர்மங்கள், அதிக கரைப்பானேற்றம் மிக்க நேர்மின் அயனி மற்றும் எதிர்மின் அயனிகள் கொண்ட அயனி நீர்மங்களைத் தருகின்றன.
இங்கு தரப்பட்டுள்ள அட்டவணையில் உள்ள இணைப்புகள், அக்கலவைகள் தனிப்பட்ட கட்டுரைகளுடன் இணைக்கப்பட்டுள்ளது. கலவைகள் தவிர கொடுக்கப்பட்டிருக்கும் எண்கள் அவற்றூக்கிடையிலான பாலிங் அளவுகோல் சார்ந்த எலக்ட்ரான் கவர்திறன் வித்தியாசத்தைக் காட்டுகின்றன. எண் அதிகமாக இருந்தால் அச்சேர்மம் அதிக அயனத்தன்மையுடன் இருக்கிறது என்று பொருளாகும்.
| கார உலோகங்கள் | |||||||
|---|---|---|---|---|---|---|---|
| இலித்தியம் | சோடியம் | பொட்டாசியம் | ருபீடியம் | சீசியம் | |||
| H a l o g e n s |
புளோரின் | LiF (3.0) | NaF (3.1) | KF (3.2) | RbF (3.2) | CsF (3.3) | |
| குளோரின் | LiCl (2.0) | NaCl (2.1) | KCl (2.2) | RbCl (2.2) | CsCl (2.3) | ||
| புரோமின் | LiBr (1.8) | NaBr (1.9) | KBr (2.0) | RbBr (2.0) | CsBr (2.1) | ||
| அயோடின் | LiI (1.5) | NaI (1.6) | KI (1.7) | RbI (1.7) | CsI (1.8) | ||
மேற்கோள்கள்
[தொகு]- ↑ Greenwood, N. N.; & Earnshaw, A. (1997). Chemistry of the Elements (2nd Edn.), Oxford:Butterworth-Heinemann. பன்னாட்டுத் தரப்புத்தக எண் 0-7506-3365-4.
- ↑ Wells, A.F. (1984) Structural Inorganic Chemistry, Oxford: Clarendon Press. பன்னாட்டுத் தரப்புத்தக எண் 0-19-855370-6.
