அல்லைல் அசிட்டேட்டு

| |

| |
| பெயர்கள் | |
|---|---|
| விருப்பத்தெரிவு ஐயூபிஏசி பெயர்
புரோப்-2-யீன்-1-ஐல் அசிட்டேட்டு | |
| வேறு பெயர்கள்
2-புரோப்பீனைல் அசிட்டேட்டு
அல்லைல் அசிட்டேட்டு | |
| இனங்காட்டிகள் | |
| 591-87-7 | |
| ChEMBL | ChEMBL1890774 |
| ChemSpider | 13862665 |
| EC number | 209-734-8 |
InChI
| |
| யேமல் -3D படிமங்கள் | Image |
| பப்கெம் | 11584 |
| வே.ந.வி.ப எண் | AF1750000 |
SMILES
| |
| UNII | E4U5E5990I |
| UN number | 2333 |
| பண்புகள் | |
| C5H8O2 | |
| வாய்ப்பாட்டு எடை | 100.12 g·mol−1 |
| தோற்றம் | நிறமற்ற நீர்மம் |
| அடர்த்தி | 0.928 கி/செ.மீ3 |
| கொதிநிலை | 103 °C (217 °F; 376 K) |
| சிறிதளவு கரையும் | |
| -56.7·10−6 செ.மீ3/மோல் | |
| தீங்குகள் | |
| GHS pictograms |   
|
| GHS signal word | அபாயம் |
| H225, H301, H312, H319, H330 | |
| P210, P233, P240, P241, P242, P243, P260, P264, P270, P271, P280, P284, P301+310, P302+352 | |
Autoignition
temperature |
374 °C (705 °F; 647 K) |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
| | |
| Infobox references | |
அல்லைல் அசிட்டேட்டு (Allyl acetate) என்பது C3H5OC(O)CH3 என்ற மூலக்கூற்று வாய்ப்பாட்டால் விவரிக்கப்படும் ஒரு கரிம வேதியியல் சேர்மமாகும். நிறமற்ற நீர்மமான இச்சேர்மம் குறிப்பாக அல்லைல் ஆல்ககாலின் முன்னோடிச் சேமமாகக் கருதப்படுகிறது. ஒரு பயனுள்ள தொழில்துறை இடைநிலை வேதிப்பொருளாகவும் பயன்படுகிறது. அல்லைல் ஆல்ககாலின் அசிடேட்டு எசுதர் என்றும் வகைப்படுத்தப்படுகிறது.
தயாரிப்பு[தொகு]
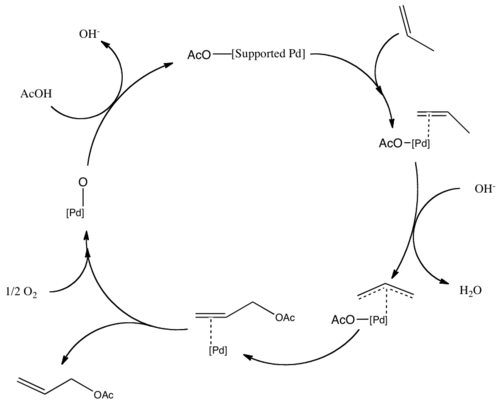
அசிட்டிக் அமிலத்தின் முன்னிலையில் பலேடியம் வினையூக்கி உதவியுடன் புரோப்பீனை வாயுநிலை வினைக்கு உட்படுத்தி அல்லைல் அசிட்டேட்டு தயாரிக்கப்படுகிறது.[1][2]
- C3H6 + CH3COOH + ½ O2 → CH2=CHCH2OCOCH3 + H2O
புரோப்பீன் விலை மலிவானது மற்றும் சுற்றுச்சூழலுக்கு ஊறு விளைவிக்காதது என்பதால் இத்தயாரிப்பு முறை ஒரு சாதகமான தயாரிப்பு முறையாகும். அல்லைல் ஆல்ககால் முதன்மையாக அல்லைல் குளோரைடிலிருந்து தயாரிக்கப்படுகிறது. ஆனால் நீராற்பகுப்பு முறையின் மூலம் உற்பத்தி செய்வது குளோரின் பயன்பாட்டைத் தவிர்க்கிறது. இதனால் பயன்பாட்டிலும் அதிகரித்து வருகிறது.
புரோப்பீனுக்குப் பதிலாக எத்திலீனைப் பயன்படுத்தி வினைல் அசிடேட்டும் இதேபோல் உற்பத்தி செய்யப்படுகிறது. அசிட்டாக்சைலேற்ற வினைகளுக்கு இவ்வினைகள் எடுத்துக்காட்டுகளாகும். பலேடியம் மையம் பின்னர் ஆக்சிசன் மூலம் மீண்டும் ஆக்சிசனேற்றப்படுகிறது. அசிட்டாக்சைலேற்ற்ற வினைக்கான வினைவழிமுறை இதேபோன்ற பாதையைப் பின்பற்றுகிறது. பலேடியத்தின் மீது புரோப்பீன் π-அலைல் பிணைப்பை உருவாக்குகிறது. [3]
வினைகள்[தொகு]
அல்லைல் அசிட்டேட்டை நீர்ராற்பகுப்பு வினைக்கு உட்படுத்தினால் அல்லைல் ஆல்ககால் உருவாகும்:
- CH2=CHCH2OCOCH3 + H2O → CH2=CHCH2OH + CH3COOH
பயன்கள்[தொகு]
உலர்த்தும் எண்ணெய்கள் போன்ற சிறப்பு பலபடிகள் தயாரிப்பதற்கான முன்னோடிச் சேர்மமாக அல்லைல் அசிட்டேட்டு பயன்படுகிறது. செயற்கை கிளிசரால் தயாரிப்பில் அல்லைல் ஆல்ககால் பயன்படுத்தப்படுகிறது. ஐதரசன் பெராக்சைடை எப்பாக்சைடேற்றம் செய்து கிளைசிடால் தயாரிக்கலாம். இதை நீராற்பகுத்தல் மூலம் கிளிசராலாக மாற்றலாம்.
- CH2=CHCH2OH + HOOH → CH2OCHCH2OH + H2O
- CH2OCHCH2OH + H2O → C3H5(OH)3
செயற்கை கிளிசரால் அழகுசாதனப் பொருட்களிலும் கழிப்பறைகளிலும் பயன்படுத்தப்படுகிறது. அதே சமயம் கொழுப்புகளின் நீராற்பகுப்பிலிருந்து கிடைக்கும் கிளிசரால் உணவில் பயன்படுத்தப்படுகிறது.[4]
பதிலீட்டு வினைகள்[தொகு]
ஐதரசன் குளோரைடை பயன்படுத்தி அல்லைல் அசிடேட்டில் உள்ள அசிட்டேட்டு குழுவை பதிலீடு செய்து அல்லைல் குளோரைடை தயாரிக்கலாம். தாமிர வினையூக்கியின் மேல் ஐதரசன் சயனைடுடன் வினையில் ஈடுபட்டு அல்லைல் அசிட்டேட்டு அல்லைல் சயனைடை கொடுக்கிறது.[5]
- CH2=CHCH2OCOCH3 + HCl → CH2=CHCH2Cl + CH3COOH
- CH2=CHCH2OCOCH3 + HCN → CH2=CHCH2CN + CH3COOH
பொதுவாக புரோப்பீனை நேரடியாக குளோரினேற்றம் செய்து அல்லைல் குளோரைடு தயாரிக்கப்படுகிறது.
மேற்கோள்கள்[தொகு]
- ↑ Harold Wittcoff; B. G. Reuben; Jeffrey S. Plotkin (2004) (Google Books excerpt). Industrial organic chemicals. பக். 212. பன்னாட்டுத் தரப்புத்தக எண்:978-0-471-54036-6. https://books.google.com/books?id=4KHzc-nYPNsC&pg=PA212#.
- ↑ Ludger Krähling (2002). Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH. DOI:10.1002/14356007.a01_425. பன்னாட்டுத் தரப்புத்தக எண் 978-3527306732.
- ↑ M. R. Churchill; R. Mason (1964). "Molecular Structure of π-allyl-palladium acetate". Nature 4960 (4960): 777. doi:10.1038/204777a0.
- ↑ H. A. Wittcoff; B. G. Reuben; J. S. Plotkin (2004). "Chemicals and Polymers from Propylene". Industrial Organic Chemicals. பக். 195–214. பன்னாட்டுத் தரப்புத்தக எண்:978-0-471-44385-8. https://archive.org/details/industrialorgani00witt.
- ↑ Ludger Krahling (2000). "Allyl Compounds". Ullmann's Encyclopedia of Industrial Chemistry. doi:10.1002/14356007.a01_425.