செருமேனியம்(IV) அயோடைடு
செருமேனியம்(IV) அயோடைடு
| |
| இனங்காட்டிகள் | |
|---|---|
| 13450-95-8 | |
| ChemSpider | 75317 |
| EC number | 236-613-7 |
InChI
| |
| யேமல் -3D படிமங்கள் | Image |
| பப்கெம் | 83479 |
| |
| பண்புகள் | |
| GeI4 | |
| வாய்ப்பாட்டு எடை | 580.25 g·mol−1 |
| தோற்றம் | சிவப்பு நிறப் படிகங்கள்[1] (வெவ்வேறு வெப்பநிலைகளுக்கான நிறங்களை, இந்த ஆவணங்களைப் பார்க்கவும்[2] |
| அடர்த்தி | 4.32 கி·செ.மீ−3 |
| உருகுநிலை | 146 °C (419 K)[1] |
| கரைதிறன் | கார்பன் டைசல்பைடு, குளோரோபாரம் மற்றும் பென்சீன் போன்ற முனைவற்ற கரைப்பான்களில் கரையும் [3] |
| தீங்குகள் | |
| GHS pictograms | 
|
| GHS signal word | அபாயம் |
| H314 | |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
செருமேனியம்(IV) அயோடைடு (Germanium(IV) iodide) என்பது GeI4 என்ற மூலக்கூற்று வாய்பாடால் விவரிக்கப்படும் ஒரு கனிம வேதியியல் சேர்மமாகும்.
தயாரிப்பு
[தொகு]செருமேனியமும் அயோடினும் சேர்ந்து இச்சேர்மம் உருவாகிறது. அல்லது செருமேனியம் ஈராக்சைடுடன் 57 சதவீத ஐதரயோடிக் அமிலத்தைச் சேர்த்து வினைபுரியச் செய்தாலும் செருமேனியம்(IV) அயோடைடு உருவாகும்.[1]
- GeO2 + 4 HI -> GeI4 + 2 H2O
வேதிப் பண்புகள்
[தொகு]செருமேனியம்(IV) அயோடைடு 250 ° செல்சியசு வெப்பநிலையில் டெட்ரா ஆல்க்கைல் வெள்ளீயத்துடன் வினைபுரிந்து R2SnI2 மற்றும் R2GeI2 (R= Et, Bu, Ph) ஆகியவற்றை உருவாக்குகிறது.[5] உயர் வெப்பநிலையில் செருமேனியம் மற்றும் கந்தகத்துடன் வினைபுரிந்து சிவப்பு நிற GeSI2 மற்றும் ஆரஞ்சு நிற Ge2S3I2 சேர்மத்தை உருவாக்குகிறது.[6] 130 பாகை செல்சியசு வெப்பநிலையில் அயனி திரவத்தில் ஈரிரும்பு நோனாகார்பனைலுடன் வினைபுரிந்து Ge12[Fe(CO)3]8I4 என்ற சேர்மத்தைக் கொடுக்கிறது.[7]
- 12GeI4 + 15Fe2(CO)9 -> Ge12[Fe(CO)3]8I4 + 22 FeI2 + 111CO↑
இயற்பியல் பண்புகள்
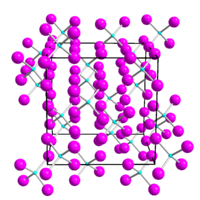
[தொகு]செருமேனியம்(IV) அயோடைடு ஆரஞ்சு-சிவப்பு நிறத்திலுள்ள ஒரு படிகத் திடப்பொருளாகும். இது தண்ணீரால் நீராற்பகுப்பு செய்யப்படுகிறது. கார்பன் டைசல்பைடு மற்றும் பென்சீனில் நன்றாக கரையக்கூடியதாகும். ஆனால் கார்பன் டெட்ராகுளோரைடு மற்றும் குளோரோஃபார்மில் குறைவாகக் கரைகிறது. உருகுநிலைக்கு மேலான வெப்பநிலையில் செருமேனியம்(II) அயோடைடு மற்றும் அயோடினாகச் சிதையத் தொடங்குகிறது.[8] செருமேனியம்(IV) அயோடைடு இடக்குழு Pa3 (எண். 205), அணிக்கோவை அளவுரு a = 11.89 Å என்ற அளவுகளுடன் கனசதுரப் படிக அமைப்பில் படிகமாக்குகிறது. படிக அமைப்பு நான்முகி GeI4 மூலக்கூறுகளைக் கொண்டுள்ளது.
மேற்கோள்கள்
[தொகு]- ↑ 1.0 1.1 1.2 A. W. Laubengayer, P. L. Brandt (Feb 1932). "The Preparation of Germanium Tetrabromide and Germanium Tetraiodide" (in en). Journal of the American Chemical Society 54 (2): 621–623. doi:10.1021/ja01341a502. பன்னாட்டுத் தர தொடர் எண்:0002-7863. https://pubs.acs.org/doi/abs/10.1021/ja01341a502. பார்த்த நாள்: 2021-01-12.
- ↑ L. M. Dennis, F. E. Hance (Dec 1922). "GERMANIUM. IV. GERMANIUM TETRA-IODIDE1" (in en). Journal of the American Chemical Society 44 (12): 2854–2860. doi:10.1021/ja01433a020. பன்னாட்டுத் தர தொடர் எண்:0002-7863. https://pubs.acs.org/doi/abs/10.1021/ja01433a020. பார்த்த நாள்: 2021-01-12.
- ↑ Schenk, P.W. (1963). "12. Silicon and Germanium". In Brauer, Georg (ed.). Handbook of preparative inorganic chemistry (Second ed.). Academic Press. p. 719. எண்ணிம ஆவணச் சுட்டி:10.1016/B978-0-12-395590-6.50020-X. பன்னாட்டுத் தரப்புத்தக எண் 978-0-12-395590-6.
- ↑ "Germanium tetraiodide". pubchem.ncbi.nlm.nih.gov (in ஆங்கிலம்).
- ↑ Kocheshkov, K. A.; Fomina, N. V.; Sheverdina, N. I.; Zemlyanskii, N. N.; Chernoplekova, V. A. Reaction of tetraalkyltin with germanium tetrahalides. Izvestiya Akademii Nauk SSSR, Seriya Khimicheskaya, 1973. 3: 711. ISSN: 0002-3353.
- ↑ A.P. Velmuzhov, M.V. Sukhanov, A.D. Plekhovich, A.I. Suchkov, V.S. Shiryaev (Mar 2015). "Thermal decomposition study of GeSI2 and Ge2S3I2 glassy alloys" (in en). Journal of Non-Crystalline Solids 411: 40–44. doi:10.1016/j.jnoncrysol.2014.09.018. Bibcode: 2015JNCS..411...40V. https://linkinghub.elsevier.com/retrieve/pii/S0022309314004736. பார்த்த நாள்: 2021-01-12.
- ↑ Silke Wolf, Wim Klopper, Claus Feldmann (2018). "Ge 12 {Fe(CO) 3 } 8 (μ-I) 4 : a germanium–iron cluster with Ge 4 , Ge 2 and Ge units" (in en). Chemical Communications 54 (10): 1217–1220. doi:10.1039/C7CC08091C. பன்னாட்டுத் தர தொடர் எண்:1359-7345. பப்மெட்:29336437. http://xlink.rsc.org/?DOI=C7CC08091C. பார்த்த நாள்: 2021-01-12.
- ↑ Holleman, Arnold F.; Wiberg, Egon; Wiberg, Nils (1995). Lehrbuch der anorganischen Chemie (101., verb. und stark erw. Aufl ed.). Berlin: de Gruyter. பன்னாட்டுத் தரப்புத்தக எண் 978-3-11-012641-9.
