மூலிகம்: திருத்தங்களுக்கு இடையிலான வேறுபாடு
No edit summary |
*விரிவாக்கம்* |
||
| வரிசை 2: | வரிசை 2: | ||
[[படிமம்:Hydroxyl_radical.png|thumb|உலூயிசின் கட்டமைப்பில் காட்டப்பட்டுள்ள ஐதரொட்சைல் மூலிகம் சோடியாக்கப்படாத ஓர் எதிர்மின்னியைக் கொண்டுள்ளது.]] |
[[படிமம்:Hydroxyl_radical.png|thumb|உலூயிசின் கட்டமைப்பில் காட்டப்பட்டுள்ள ஐதரொட்சைல் மூலிகம் சோடியாக்கப்படாத ஓர் எதிர்மின்னியைக் கொண்டுள்ளது.]] |
||
[[வேதியியல்|வேதியியலில்]], '''மூலிகம்''' (''Radical'') அல்லது '''கட்டுறாத மூலிகம்''' (''Free Radical'') என்பது சோடியாக்கப்படாத வலுவளவு எதிர்மின்னியைக் கொண்டுள்ள [[அணு]], [[மூலக்கூறு]] அல்லது [[அயனி]] ஆகும். சோடியாக்கப்படாத [[எதிர்மின்னி]]கள் இருப்பதால் பெரும்பாலான |
[[வேதியியல்|வேதியியலில்]], '''மூலிகம்''' (''Radical'') அல்லது '''கட்டுறாத மூலிகம்''' (''Free Radical'') என்பது சோடியாக்கப்படாத வலுவளவு எதிர்மின்னியைக் கொண்டுள்ள [[அணு]], [[மூலக்கூறு]] அல்லது [[அயனி]] ஆகும். சோடியாக்கப்படாத [[எதிர்மின்னி]]கள் இருப்பதால் பெரும்பாலான கட்டுறா மூலிகங்கள் உயர் [[வேதி வினை|வேதித் தாக்குதிறன்]] கொண்டவை. பெரும்பாலான கட்டுறா மூலிகங்கள் தன்னிச்சையாக [[இருபடிச் சேர்மம்|இருபகுதியங்களாகிக்]] கொள்ளும். பெரும்பாலான கரிம மூலிகங்களின் ஆயுட்காலம் மிகக்குறைவாகும். |
||
கட்டுறா மூலிகங்கள் இலகுவில் [[வேதி வினை|வேதித் தாக்கத்திற்கு]] ஆளாகக்கூடியவை. பெரும்பாலான கட்டுறா மூலிகங்கள் தன்னிச்சையாக [[இருபடிச் சேர்மம்|இருபகுதியங்களாகிக்]] கொள்ளும். பெரும்பாலான கரிம மூலிகங்களின் ஆயுட்காலம் மிகக்குறைவாகும். |
|||
கட்டுறாத மூலிகத்திற்கான எடுத்துக்காட்டாக, [[ஒட்சிசன்]] அணுவில் சோடியற்ற ஓர் எதிர்மின்னியைக் கொண்டுள்ள ஐதரொட்சைல் மூலிகத்தை (HO•) எடுத்துக்கொள்ளலாம். |
கட்டுறாத மூலிகத்திற்கான எடுத்துக்காட்டாக, [[ஒட்சிசன்]] அணுவில் சோடியற்ற ஓர் எதிர்மின்னியைக் கொண்டுள்ள ஐதரொட்சைல் மூலிகத்தை (HO•) எடுத்துக்கொள்ளலாம். |
||
| வரிசை 19: | வரிசை 18: | ||
[[File:Radical.svg|centre|300px]] |
[[File:Radical.svg|centre|300px]] |
||
== உருவாக்கம் == |
|||
மூலிகங்களைத் தோற்றுவிப்பதற்கு, [[சமப்பகுப்பு|சமப்பகுப்பின்]] மூலம் [[பிணைப்பு பிளவு|பங்கீட்டுவலுப் பிணைப்புகளை உடைக்க]] வேண்டிய தேவை இருக்கலாம். கூடிய [[ஆற்றல்]] இதற்குத் தேவைப்படும். Δ''H''{{px1}}° என்ற குறியீட்டின் மூலம் இச்சமப்பகுப்புப் பிணைப்புப் பிரிகை ஆற்றல்கள் குறித்துக்காட்டப்படும். எடுத்துக்காட்டாக, [[ஐதரசன்|H<sub>2</sub>]] ஐ 2H• ஆகப் பிரிகையடையச் செய்வதற்கு Δ''H''{{px1}}° = +435 kJ'''·'''mol{{smallsup|-1}} தேவைப்படும். அதேவேளை, Cl<sub>2</sub> ஐ 2Cl• ஆகப் பிரிகையடையச் செயவதற்கு Δ''H''{{px1}}° = +243 kJ'''·'''mol{{smallsup|-1}} தேவைப்படும். |
|||
== பல்பகுதியாக்கம் == |
|||
== மேற்கோள்கள் == |
== மேற்கோள்கள் == |
||
06:21, 31 மே 2018 இல் நிலவும் திருத்தம்
இந்தக்கட்டுரையினை தற்பொழுது இன்னொருவர் சிறிது நேரத்துக்கு தொகுத்துக் கொண்டிருக்கிறார். எனவே இந்த அறிவிப்பு இருக்கும் வரை, நீங்கள் இதனைத் தொகுப்பதைத் தவிர்க்கவும். இப்பக்கம் இறுதியாக 06:21, 31 மே 2018 (ஒ.அ.நே) (5 ஆண்டுகள் முன்னர்) தொகுக்கப்பட்டது. இது சில மணித்தியாலங்களாகத் தொகுக்கப்படாதிருப்பின், இந்த வார்ப்புருவை நீக்குங்கள். இவ்வார்புருவை நீங்கள் இப்பக்கத்தில் இணைத்திருந்தால், பல அமர்வுகளுக்கிடையே {{வேலை நடந்துகொண்டிருக்கிறது}} எனப் பயன்படுத்துக. |
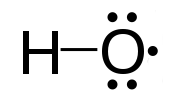
வேதியியலில், மூலிகம் (Radical) அல்லது கட்டுறாத மூலிகம் (Free Radical) என்பது சோடியாக்கப்படாத வலுவளவு எதிர்மின்னியைக் கொண்டுள்ள அணு, மூலக்கூறு அல்லது அயனி ஆகும். சோடியாக்கப்படாத எதிர்மின்னிகள் இருப்பதால் பெரும்பாலான கட்டுறா மூலிகங்கள் உயர் வேதித் தாக்குதிறன் கொண்டவை. பெரும்பாலான கட்டுறா மூலிகங்கள் தன்னிச்சையாக இருபகுதியங்களாகிக் கொள்ளும். பெரும்பாலான கரிம மூலிகங்களின் ஆயுட்காலம் மிகக்குறைவாகும்.
கட்டுறாத மூலிகத்திற்கான எடுத்துக்காட்டாக, ஒட்சிசன் அணுவில் சோடியற்ற ஓர் எதிர்மின்னியைக் கொண்டுள்ள ஐதரொட்சைல் மூலிகத்தை (HO•) எடுத்துக்கொள்ளலாம்.
தாழ்த்தல்-ஏற்றத் தாக்கங்கள், அயனியாக்கும் கதிர்ப்பு, வெப்பம், மின்னிறக்கங்கள், மின்பகுப்பு போன்ற செய்முறைகளின் மூலிகங்கள் உருவாக்கப்படுவதுண்டு.
வேதித் தாக்கங்களில்
வேதிச் சமன்பாடுகளில், அணுக் குறியீட்டுக்கோ மூலக்கூற்று வாய்பாட்டுக்கோ வலப்பக்கத்தில் ஒரு புள்ளியை இடுவதன் மூலம் கட்டுறா மூலிகங்கள் பொதுவாக அடையாளப்படுத்தப்படுகின்றன.
- குளோரின் வளிமமானது புறவூதாக் கதிர்களின் முன்னிலையில் குளோரின் அணு மூலிகங்களாகப் பிரிகையடையும்.
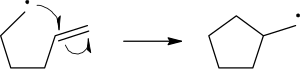
மூலிகத் தாக்கப் பொறிமுறைகளில் தனி எதிர்மின்னிகளின் நகர்வைக் காட்ட ஒருதலை அம்புக்குறிகள் பயன்படுத்தப்படும்:
உருவாக்கம்
மூலிகங்களைத் தோற்றுவிப்பதற்கு, சமப்பகுப்பின் மூலம் பங்கீட்டுவலுப் பிணைப்புகளை உடைக்க வேண்டிய தேவை இருக்கலாம். கூடிய ஆற்றல் இதற்குத் தேவைப்படும். ΔHவார்ப்புரு:Px1° என்ற குறியீட்டின் மூலம் இச்சமப்பகுப்புப் பிணைப்புப் பிரிகை ஆற்றல்கள் குறித்துக்காட்டப்படும். எடுத்துக்காட்டாக, H2 ஐ 2H• ஆகப் பிரிகையடையச் செய்வதற்கு ΔHவார்ப்புரு:Px1° = +435 kJ·mol-1 தேவைப்படும். அதேவேளை, Cl2 ஐ 2Cl• ஆகப் பிரிகையடையச் செயவதற்கு ΔHவார்ப்புரு:Px1° = +243 kJ·mol-1 தேவைப்படும்.

