அலோகம்: திருத்தங்களுக்கு இடையிலான வேறுபாடு
உள்ளடக்கம் நீக்கப்பட்டது உள்ளடக்கம் சேர்க்கப்பட்டது
No edit summary |
No edit summary |
||
| வரிசை 1: | வரிசை 1: | ||
[[File:Periodic table (polyatomic).svg|thumb|right|350px|தனிம வரிசை அட்டவணையில் அலோகங்கள்:<br/>{{legend|{{Element color|polyatomic nonmetal}}|[[#polyatomic nonmetal|பலவணு அலோகங்கள்]]}}{{legend|{{Element color|diatomic nonmetal}}|[[#Diatomic nonmetals|ஈரணு அலோகங்கள்]]}}{{legend|{{Element color|Noble gas}}|[[#Noble gases|மந்த வாயுக்கள்]]}} அட்டவணையில் [[ஐதரசன்]] தவிர மற்ற அலோகங்கள், [[p-தொகுதி]] யில் அடுக்கப்பட்டுள்ளன. [[ஹீலியம்]], s-தொகுதி தனிமம் பொதுவாக மந்த வாயுக்களுக்கான பண்புகளைப் பெற்றிருப்பதால் [[நியான்| நியானுக்கு மேலாக ( p-தொகுதி) வைக்கப்பட்டுள்ளது]].]] |
[[File:Periodic table (polyatomic).svg|thumb|right|350px|தனிம வரிசை அட்டவணையில் அலோகங்கள்:<br/>{{legend|{{Element color|polyatomic nonmetal}}|[[#polyatomic nonmetal|பலவணு அலோகங்கள்]]}}{{legend|{{Element color|diatomic nonmetal}}|[[#Diatomic nonmetals|ஈரணு அலோகங்கள்]]}}{{legend|{{Element color|Noble gas}}|[[#Noble gases|மந்த வாயுக்கள்]]}} அட்டவணையில் [[ஐதரசன்]] தவிர மற்ற அலோகங்கள், [[p-தொகுதி]] யில் அடுக்கப்பட்டுள்ளன. [[ஹீலியம்]], s-தொகுதி தனிமம் பொதுவாக மந்த வாயுக்களுக்கான பண்புகளைப் பெற்றிருப்பதால் [[நியான்| நியானுக்கு மேலாக ( p-தொகுதி) வைக்கப்பட்டுள்ளது]].]] |
||
உலோகப் பண்புகளை பெற்றிருக்காத வேதியியல் தனிமங்கள் [[அலோகங்கள்]] என்று அழைக்கப்படுகின்றன. அலோகங்கள் எளிதில் ஆவியாகக் கூடியனவாகவும், வெப்பத்தையும் மின்சாரத்தையும் எளிதில் கடத்தாத காப்புப் பொருட்களாகவும், குறைவான நெகிழ்வுத் தன்மை கொண்டவையாகவும் காணப்படுகின்றன. |
உலோகப் பண்புகளை பெற்றிருக்காத வேதியியல் தனிமங்கள் [[அலோகங்கள்]] என்று அழைக்கப்படுகின்றன. அலோகங்கள் எளிதில் ஆவியாகக் கூடியனவாகவும், வெப்பத்தையும் மின்சாரத்தையும் எளிதில் கடத்தாத காப்புப் பொருட்களாகவும், குறைவான நெகிழ்வுத் தன்மை கொண்டவையாகவும் காணப்படுகின்றன.வேதியியல் பண்புகளின் அடிப்படையில் இவை அதிக அயனியாக்கும் ஆற்றல் மற்றும் எலக்ட்ரான் கவர் ஆற்றல் மதிப்புகளைக் கொண்டுள்ளன. அலோகங்கள் மற்ற தனிமங்கள் அல்லது சேர்மங்களுடன் வினைபுரியும் போது எலக்ட்ரான்களைப் பெற அல்லது பகிர்ந்து கொள்ள முனைகின்றன |
||
07:43, 30 ஆகத்து 2014 இல் நிலவும் திருத்தம்
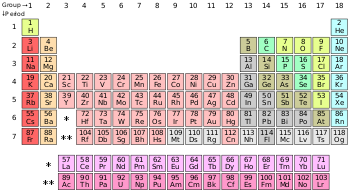
அட்டவணையில் ஐதரசன் தவிர மற்ற அலோகங்கள், p-தொகுதி யில் அடுக்கப்பட்டுள்ளன. ஹீலியம், s-தொகுதி தனிமம் பொதுவாக மந்த வாயுக்களுக்கான பண்புகளைப் பெற்றிருப்பதால் நியானுக்கு மேலாக ( p-தொகுதி) வைக்கப்பட்டுள்ளது.
உலோகப் பண்புகளை பெற்றிருக்காத வேதியியல் தனிமங்கள் அலோகங்கள் என்று அழைக்கப்படுகின்றன. அலோகங்கள் எளிதில் ஆவியாகக் கூடியனவாகவும், வெப்பத்தையும் மின்சாரத்தையும் எளிதில் கடத்தாத காப்புப் பொருட்களாகவும், குறைவான நெகிழ்வுத் தன்மை கொண்டவையாகவும் காணப்படுகின்றன.வேதியியல் பண்புகளின் அடிப்படையில் இவை அதிக அயனியாக்கும் ஆற்றல் மற்றும் எலக்ட்ரான் கவர் ஆற்றல் மதிப்புகளைக் கொண்டுள்ளன. அலோகங்கள் மற்ற தனிமங்கள் அல்லது சேர்மங்களுடன் வினைபுரியும் போது எலக்ட்ரான்களைப் பெற அல்லது பகிர்ந்து கொள்ள முனைகின்றன
