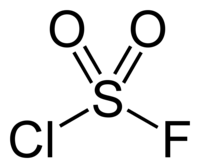
சல்பியூரைல் குளோரைடு புளோரைடு
| |||
| |||
| பெயர்கள் | |||
|---|---|---|---|
| ஐயூபிஏசி பெயர்
சல்பியூரைல் குளோரைடு புளோரைடு
| |||
| வேறு பெயர்கள்
சல்பியூரைல் புளோரைடு குளோரைடு
| |||
| இனங்காட்டிகள் | |||
| 13637-84-8 | |||
| ChEBI | CHEBI:39445 | ||
| ChemSpider | 24370 | ||
| யேமல் -3D படிமங்கள் | Image | ||
| பப்கெம் | 26159 | ||
| வே.ந.வி.ப எண் | WT4900000 | ||
SMILES
| |||
| பண்புகள் | |||
| ClFO2S | |||
| வாய்ப்பாட்டு எடை | 118.52 கிராம்/மோல் | ||
| தோற்றம் | நிறமற்ற வாயு | ||
| அடர்த்தி | 1.623 கி/செ.மீ3 0 °செல்சியசில் | ||
| உருகுநிலை | −124.7 °C (−192.5 °F; 148.5 K) | ||
| கொதிநிலை | 7.1 °C (44.8 °F; 280.2 K) | ||
| நீராற்பகுப்பு | |||
| பிற கரைப்பான்கள்-இல் கரைதிறன் | SO2 மற்றும் ஈதர் | ||
| கட்டமைப்பு | |||
| ஒருங்கிணைவு வடிவியல் |
நான்முகி | ||
| தீங்குகள் | |||
| முதன்மையான தீநிகழ்தகவுகள் | மிதமான நஞ்சு, அரிக்கும் | ||
| பொருள் பாதுகாப்பு குறிப்பு தாள் | "External MSDS" | ||
| R-சொற்றொடர்கள் | R14 R34 | ||
| S-சொற்றொடர்கள் | S24/25 S26 S27 S28 S36/37/39 S38 S45 | ||
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |||
| | |||
| Infobox references | |||
சல்பியூரைல் குளோரைடு புளோரைடு (Sulfuryl chloride fluoride) என்பது SO2ClF என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட ஒரு கரிம வேதியியல் சேர்மமாகும். உயர் ஆக்சிசனேற்ற வேதிப்பொருள்களுக்கு இதை கரைப்பானாகப் பயன்படுத்துகிறார்கள்.
பொட்டாசியம் புளோரோசல்பைட்டு தயாரித்தலில், ஆய்வகத் தயாரிப்பு தொடங்குகிறது:[1]. இவ்வுப்பு பின்னர் குளோரினேற்றம் செய்யப்பட்டு சல்பியூரைல் குளோரைடு புளோரைடு தயாரிக்கப்படுகிறது:[2].
KSO2F + Cl2 → SO2ClF + KCl
மேலும் 180 பாகை செல்சியசு வெப்பநிலைக்கு சூடுபடுத்தினால் பொட்டாசியம் புளோரோசல்பைட்டும் சல்பியூரைல் குளோரைடு புளோரைடும் சேர்ந்த கலவை சல்பியூரைல் புளோரைடைத் தருகிறது.
இம்முறைக்கு மாறாக சல்பியூரைல் குளோரைடு புளோரைடை வாயுக்களை தொடக்க வினைபடுபொருட்களாக உபயோகிக்காமல் தயாரிக்க முடியும். சல்பியூரைல் குளோரைடுடன் அமோனியம் புளோரைடு அல்லது பொட்டாசியம் புளோரைடு சேர்த்து இவற்றுடன் டிரைபுளோரோ அசிட்டிக் அமிலம் சேர்த்து சூடுபடுத்தினாலும் சல்பியூரைல் குளோரைடு புளோரைடு தயாரிக்கலாம்[3].
SO2Cl2 + NH4F → SO2ClF + NH4Cl
மேற்கோள்கள்[தொகு]
- ↑ Seel, F.; Czerepinski, Ralph G.; Cady, George H. (1967). "Potassium Fluorosulfite". Inorg. Synth.. Inorganic Syntheses 9: 113–115. doi:10.1002/9780470132401.ch29. பன்னாட்டுத் தரப்புத்தக எண்:978-0-470-13240-1.
- ↑ Seel, F.; Czerepinski, Ralph G.; Cady, George H. (1967). "Potassium Fluorosulfite". Inorg. Synth.. Inorganic Syntheses 9: 113–115. doi:10.1002/9780470132401.ch29. பன்னாட்டுத் தரப்புத்தக எண்:978-0-470-13240-1.
- ↑ Prakash Reddy, V (1992). "A convenient preparation of sulfuryl chloride fluoride". Journal of Fluorine Chemistry 56 (2): 195–197. doi:10.1016/S0022-1139(00)81102-1.


