காப்மன் வோல்டாமீட்டா்
காப்மன் வோல்டாமீட்டா் (Hofmann voltameter) என்பது 1866ஆம் ஆண்டில் ஆகத்து வில்கெல்ம் வான் காப்மேன் (1818-1892)[1] என்பவரால் கண்டுபிடிக்கப்பட்ட தண்ணீரை மின்னாற்பகுப்பு செய்வதற்கான ஒரு கருவியாகும். இந்த ஆய்கருவியைப் பயன்படுத்தி நீரின் பருமன் அளவு இயைபைக் கண்டறியலாம். சற்றே கந்தக அமிலம் கலந்த நீரில் மின்னோட்டத்தை செலுத்தும் போது நீரானது மின்னாற் பகுக்கப்பட்டு நோ்மின் வாயில் உயிரகமும் எதிா்மின் வாயில் நீரகமும் கிடைக்கின்றன.
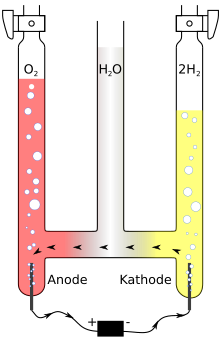
இதில் மூன்று செங்குத்தான கண்ணாடிக் குழல்கள் அடியில் இணைக்கப்பட்டுள்ளன. உள் குழல் சற்றே கந்தகம் கலந்த நீரை ஊற்ற திறந்துள்ளது. இந்தத் தாழ் அடர்த்தி அமிலநீர் மின்கடத்துமையைக் கூட்டி, மின்சுற்று இணைந்திருக்கவும் உதவுகிறது. இரு பக்கக் குழல் ஒவ்வொன்றிலும் அடியில் பிளாட்டின மின்முனை வைக்கப்படுகிறது; இதில் ஒன்று மின்வாயிலின் நேர்முனையிலும் மற்றொன்று எதிர் முனையிலும் இணைக்கப்படுகின்றன. மின்னோட்டம் காப்மன் வோட்டாமீட்டர் வழியாகப் பாயும்போது, நேர் மின்முனையில் வளிம உயிரகமும் எதிர்முனையில் வளிம நீரகமும் சேர்கின்றன. ஒவ்வொரு வளிமமும் நீரை இடம்பெயரச் செய்து வெளிப்பக்கக் குழல்களின் மேற்பகுதியில் திரள்கின்றன.[2]
வளிமங்கள் திரளும் குழல்கள் அளவீடு குறிக்கப்ப்ட்டவை. எனவே, அவற்றில் திரளும் வளிமத்தின் பருமனைக் கண்டுபிடிக்கலாம். நீரின் பருமன் இயைபும் நிறை அல்லது பொருண்மை இயைபும் பொருண்மைச் சதவீத இயைபும் பின்வருமாறு:
பருமன் அளவு இயைபு H : O = 2 : 1
பொருண்மை இயைபு H : O = 2 : 16
பொருண்மைச் சதவீத இயைபு H = 11.11 % O = 88.89 %
பெயர்[தொகு]
பாரடே பயன்படுத்திய "வோல்ட்டா- எலெக்ட்ரோமீட்டர்" என்ற சொல்லை ஜான் பிரெடெரிக் டானியல் "வோல்டா மீட்டர்" எனச் சுருக்கி வழங்கினார்.[3]
பயன்கள்[தொகு]
வளிமப் பருமனில் இருந்து அமிஅப்பின் ஊடாக பாய்ந்த மின் அளவைக் கணக்கிடலாம். தாமசு எடிசன் இவ்வகை வோல்ட்டாமீட்டரை மின்னளவிகளாகப் பயன்படுத்தினார்.
பருவேதியியல் இயைபுசார் நெறிமுறைகளைச் செயல்முறையில் விளக்க காப்மன் வோல்ட்டாமீட்டர்கள் பயன்படுகின்றன. மின்முனைகளில் திரளும் நீரக, உயிரகப் பருமன்களின் விகிதம் 2:இ ஆக அமைவது நீரின் வேதியியல் சமன்பாட்டை, H2O நிறுவுகிறது. இது இருவளிமங்களும் மூலக்குறு வடிவில் அமைந்தால் மட்டுமே உண்மையாகும். நீரகம் தனி அணுவாகவும் உயிரகம் இரட்டையணு மூலக்கூறாகவும் அமைந்தால் பருமன விகிதம் 4:1 ஆக அமையும்..[4]
மேற்கோள்கள்[தொகு]
- ↑ von Hofmann, A. W. Introduction to Modern Chemistry: Experimental and Theoretic; Embodying Twelve Lectures Delivered in the Royal College of Chemistry, London. Walton and Maberly, London, 1866. [1]
- ↑ "Electrolysis Of Water". Water structure and science. Martin Chaplin. பார்க்கப்பட்ட நாள் 15 March 2022.
- ↑ Frank A. J. L. James, (1991), The correspondence of Michael Faraday, IET, பன்னாட்டுத் தரப்புத்தக எண் 0-86341-249-1, letter 872, 9/1/1836
- ↑ "Electrolysis Of Water". Water structure and science. Martin Chaplin. பார்க்கப்பட்ட நாள் 15 March 2022.
மேலும் படிக்க[தொகு]
- ஏழாம் வகுப்பு அறிவியல் பாடநூல், தமிழ்நாட்டுப் பாடநூல் கழகம், சென்னை - 600 006.
- von Hofmann, A. W. Introduction to Modern Chemistry: Experimental and Theoretic; Embodying Twelve Lectures Delivered in the Royal College of Chemistry, London. Walton and Maberly, London, 1866. [1]
- Frank A. J. L. James, (1991), The correspondence of Michael Faraday, IET, பன்னாட்டுத் தரப்புத்தக எண் 0-86341-249-1, letter 872, 9/1/1836
