பெக்மன் மறுசீரமைப்பு வினை
பெக்மன் மறுசீரமைப்பு வினை (Beckmann rearrangement) என்பது ஓர் அமில வினையூக்கியின் முன்னிலையில் ஓர் ஆக்சைம் சேர்மமானது பதிலீடு செய்யப்பட்ட அமைடாக மாறும் வினையைக் குறிக்கிறது. வளைய ஆக்சைம்கள் இவ்வினையில் லாக்டம்களைக் கொடுக்கின்றன. செருமானிய வேதியியல் அறிஞர் எர்னசுட்டு ஆட்டோ பெக்மன் இவ்வினையைக் கண்டறிந்தார் என்பதால் இவ்வினைக்கு பெக்மன் மறுசீரமைப்பு வினை என்று பெயரிடப்பட்டது[1][2][3].
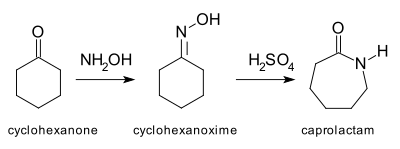
இந்த எடுத்துக்காட்டு வினை வளைய எக்சனோனில் தொடங்குகிறது. வினை இடைநிலையாக வளைய எக்சனோன் ஆக்சைம் தோன்றி முடிவாக காப்ரோலாக்டம் என்ற வளைய அமைடு உற்பத்தியாகிறது. காப்ரோலாக்டம் நைலான் 6 தயாரிப்பில் பயன்படும் மூலப்பொருளாகும். எனவே பெக்மன் மறுசீராக்கு வினையின் முக்கியப்பயன்பாடு காப்ரோலாக்டம் தயாரிப்பது என்றே கருதப்படுகிறது.
அசிட்டிக் அமிலம், ஐதரோகுளோரிக் அமிலம், அசிட்டிக் நீரிலி ஆகியவற்றைக் கொண்டு பெக்மன் கரைசல் உருவாக்கப்படுகிறது. அமைப்பு மாற்ற வினைகளுக்கு வினையூக்கியாக பரவலாக இக்கரைசல் பயன்படுத்தப்படுகிறது. இவற்றைத் தவிர கந்தக அமிலம் அல்லது பாலிபாசுபாரிக் அமிலம் போன்றவற்றையும் இதற்காகப் பயன்படுத்த இயலும். வணிக முறையில் லாக்டம் தயாரிப்புக்கு பொதுவாக கந்தக அமிலத்தைப் பயன்படுத்துகிறார்கள். ஏனெனில் லாக்டம் உருவாகும்போது இதை அமோனியா சேர்த்து நடுநிலையாக்கும் போது உடன் விளைபொருளாக அமோனியம் சல்பேட்டு என்ற பொதுவாகப் பயன்படுத்தப்படும் வேளாண்மை உரம் உருவாகிறது. இவ்வுரம் நைட்ரசனையும் கந்தகத்தையும் வழங்குகிறது.
வினை வழிமுறை
[தொகு]பெக்மன் மறுசீராக்கல் வினையின் வினை வழிமுறை ஆல்க்கைல் குழுவின் இடப்பெயர்ச்சியுடன் நைட்ரிலியம் அயனி உருவாக ஐதராக்சில் குழுவின் நீக்கம் மற்றும் தொடரும் நீராற்பகுப்பு ஆகிய செயல்முறைகளைக் கொண்டுள்ளது.
ஒர் ஆய்வில் [4], கரைப்பான் மூலக்கூறுகள் மற்றும் பதிலிகள் இருப்பதைக் கணக்கில் கொண்டு கணிப்பொறி தூண்டல் முறையில் வினைவழி முறை நிறுவப்பட்டது.
பெக்மன் கரைசலில் அசிட்டோன் ஆக்சைமின் அமைப்பு மாற்றத்தில் மூன்று அசிட்டிக் அமில மூலக்கூறுகளும், ஆக்சோனியம் அயனியில் காணப்படும் ஒரு மூலக்கூறும் பங்கேற்கின்றன. இடைநிலையில் இமினியம் அயனியான (σ-அணைவு) மெத்தில் குழு நைட்ரசன் குழுவை நோக்கி நகர்கிறது. அதே நேரத்தில் நிகழும் மற்றொரு வினையில் ஐதராக்சில் குழு வெளியேற்றப்படுகிறது. ஐதராக்சில் குழுவில் உள்ள ஆக்சிசன் அணு மூன்று அசிட்டிக் அமிலமூலக்கூறுகளால் நிலைப்படுத்தப்படுகிறது. அடுத்த படிநிலையில் நைட்ரிலியம் அயனியில் இருக்கும் மின்னணுகவரியான கார்பன் அணு தண்ணீரால் தாக்கபட்டு அசிட்டிக் அமிலத்திற்கு புரோட்டான் திருப்பி கொடையளிக்கப்படுகிறது. இந்த இடைநிலையில் என் – மெத்தில் அசிட்டமிடிக் அமிலம் உருவாகிறது. மற்றும் நீர் ஆக்சிசன் அணு நான்கு மற்ற அணுக்களுடன் ஒருங்கிணைவு அடைகிறது. மூன்றாவது படிநிலையில் ஒரு மாற்றியமாகும் படி நைட்ரசன் அணுவை புரோட்டானேற்றம் செய்து அமைடை உருவாக்குகிறது.

ஓர் ஐதரோ ஆக்சோனியம் மற்றும் ஆறு தண்ணீர் மூலக்கூறுகள் பங்கேற்கும் வினையென்றாலும் இதே முடிவுதான் கணிக்கப்படுகிறது. ஆனால், புரோட்டானேற்றம் பெற்ற அசிட்டிக் அமிலத்துடன் அசிட்டோபீனோன் ஆக்சைம் ஈடுபடும் வினையில், இடம்பெயரும் பதிலீடு பீனைலாக இருக்கும்போது மூன்று உறுப்பு π-அணைவு இடைநிலை உருவாகும் வினைவழி முறைக்கு வாய்ப்பாகிறது. இந்த π-அணைவு H3O+(H2O)6 இல் காணப்படுவதில்லை.

வளைய எக்சனோன் ஆக்சைமுடன் வளைய திரிபின் நிலையற்ற தன்மை நீங்கும் போது மூன்றாவது வகை வினைவழி முறை கிடைக்கிறது. π-அணைவு அல்லது σ-அணைவு இடைநிலைகள் தோன்றாமல் ஒரேநேர வினை படிநிலையில் புரோட்டானேற்றம் பெற்ற காப்ரோலாக்டம் உருவாகிறது.
சயனூரிக் அமிலத்தால் பெக்மன் வினை
[தொகு]சயனூரிக் குளோரைடு மற்றும் துத்தநாகக் குளோரைடு என்ற இணை வினையூக்கிகளால் வினையூக்கம் செய்யப்படும் பெக்மன் வினையும் அறியப்படுகிறது. உதாரணமாக வளைய டோடெக்கனோனை அதனுடன் தொடர்புடைய லாக்டம் ஆக மாற்ற முடியும். இந்த லாக்டம் நைலான்12 தயாரிப்புக்கான ஒருமம் ஆகும். [5][6]

ஒரு வினையூக்கியின் பலபடிநிலை வினையை அடிப்படையாகக் கொண்டு இவ்வினைவழிமுறை அமைகிறது. சயனூரிக் குளோரைடு ஐதராக்சில் குழுவை அணுக்கருகவர் அரோமாட்டிக் பதிலீடு மூலம் செயலூக்கம் அடையச் செய்கிறது. புதிய வினைபடுபொருளால் ஓர் இடைநிலை மெய்சென்னெய்மர் அணைவு உருவாக்கம் வழியாக வினைவிளை பொருள் நீக்கமடைகிறது.
பெக்மன் வினை துண்டாதல்
[தொகு]ஐதராக்சில் குழுவுக்கு எதிர் நிலையில் ஆக்சைம் ஒரு நான்கம்நிலை கார்பனைக் கொண்டிருக்கும் போது துண்டாதல் நிகழ்ந்து நைட்ரைல் உருவாகிறது.
இத்துண்டாதல் வினையில் புளோரின் வழங்கியாகச் செயல்படுவது டையெத்திலமினோகந்தக டிரைபுளோரைடு ஆகும் :[7].
செம்லர் உல்ப் வினை
[தொகு]வளைய எக்சனோனின் ஆக்சைம் உடன் ஓர் அமிலம் வினைப்படும் போது அனிலீன் உருவாகிறது. நீர்நீக்க-அரோமாட்டிக்காதல் வினையான இவ்வினை செம்லர் உல்ப் வினை அல்லது உல்ப் அரோமாட்டிக்காதல் வினை என்று அழைக்கப்படுகிறது [8][9][10][11].
மேற்கோள்கள்
[தொகு]- ↑ Ernst Otto Beckmann (1886). "Zur Kenntniss der Isonitrosoverbindungen". Berichte der Deutschen Chemischen Gesellschaft 19: 988–993. doi:10.1002/cber.188601901222. http://gallica.bnf.fr/ark:/12148/bpt6k90705g/f990.image.langEN.
- ↑ Donaruma, L. G.; Heldt, W. Z. (1960). "The Beckmann rearrangement. (Review)". Org. React. 11: 1–156.
- ↑ Gawley, R. E. (1988). "The Beckmann reactions: rearrangement, elimination-additions, fragmentations, and rearrangement-cyclizations. (Review)". Org. React. 35: 14–24.
- ↑ Yamabe, S.; Tsuchida, N.; Yamazaki, S. (2005). "Is the Beckmann Rearrangement a Concerted or Stepwise Reaction? A Computational Study". Journal of Organic Chemistry 70 (26): 10638–10644. doi:10.1021/jo0508346. பப்மெட்:16355980. http://pubs.acs.org/cgi-bin/abstract.cgi/joceah/2005/70/i26/abs/jo0508346.html.
- ↑ Furuya, Y.; Ishihara, K.; Yamamoto, H. (2005). "Cyanuric Chloride as a Mild and Active Beckmann Rearrangement Catalyst". Journal of the American Chemical Society 127 (32): 11240–11241. doi:10.1021/ja053441x. பப்மெட்:16089442. http://pubs.acs.org/cgi-bin/abstract.cgi/jacsat/2005/127/i32/abs/ja053441x.html.
- ↑ Taber, Douglass F.; Straney, Patrick J. (2010). "The Synthesis of Laurolactam from Cyclododecanone via a Beckmann Rearrangement". J. Chem. Educ. 87 (12): 1392. doi:10.1021/ed100599q. Bibcode: 2010JChEd..87.1392T.
- ↑ Kirihara, Masayuki; Niimi, Kanako; Momose, Takefumi (1997). "Fluorinative -cleavage of cyclic ketoximes with diethylaminosulfur trifluoride: an efficient synthesis of fluorinated carbonitriles". Chemical Communications 6 (6): 599–600. doi:10.1039/a607749h.
- ↑ W. Semmler, Ber. 25, 3352 (1892)
- ↑ L. Wolff, Amp. 322, 351 (1902)
- ↑ Name reactions and reagents in organic synthesis, Bradford P. Mundy,Michael G. Ellerd,Frank G. Favaloro
- ↑ Beckmann Rearrangements. An Investigation of Special Cases E. C. Horning, V. L. Stromberg, H. A. Lloyd J. Am. Chem. Soc., 1952, 74 (20), pp 5153–5155 எஆசு:10.1021/ja01140a048




