சமச்சீரற்ற கரிமம்
சமச்சீரற்ற காபன் அணு என்பது நான்கு வித்தியாசமான அணுக்கள் அல்லது அணுக்கூட்டங்கள் இணைக்கப்பட்ட காபன் அணுவாகும்.[1][2] எந்தவொரு சேதனச் சேர்வையினதும் சமச்சீரற்ற காபன் அணுக்களின் எண்ணிக்கையை அறிவதன் மூலம் அதன் திண்மச் சமபகுதியங்களின் எண்ணிக்கையை அறிய முடியும். அதற்கான வழி பின்வருமாறு:
- n என்பது சமச்சீரற்ற காபன் அணுக்களின் எண்ணிக்கையாயின் சமபகுதியங்களின் எண்ணிக்கை = 2n
உதாரணமாக, மாலிக் அமிலம் நான்கு காபன் அணுக்களைக் கொண்டுள்ளது. இவற்றுள் ஒரு அணு சமச்சீரற்றது. சமச்சீரற்ற காபனில், இரண்டு காபன் அணுக்களும், ஒரு ஒட்சிசன் அணுவும் ஒரு ஐதரசன் அணுவும் இணைக்கப்பட்டுள்ளது. இதில் இரண்டு காபன் அணுக்கள் உள்ளமையால் இது சமச்சீரற்ற காபனா என்பதில் குழப்பம் ஏற்படலாம். ஆயினும், இவ்விரு காபன் அணுக்களும் ஒரே கூட்டத்தைச் சேர்ந்தவையல்ல. எனவே, இந் நான்கு அணுக் கூட்டங்களும் இணைக்கப்பட்ட காபன் அணு சமச்சீரற்றதாகும்:
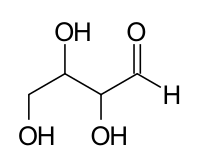
இரண்டு சமச்சீரற்ற காபன்களைக் கொண்ட டெற்றோசில் உள்ள சமபகுதியங்கள் 22 = 4 திண்மச் சமபகுதியங்கள்:
மூன்று சமச்சீரற்ற காபன்களைக் கொண்ட அல்டோபென்டோசில் உள்ள சமபகுதியங்கள் 23 = 8 திண்மச் சமபகுதியங்கள்:
நான்கு சமச்சீரற்ற காபன்களைக் கொண்ட அல்டோஎக்சோசில் உள்ள சமபகுதியங்கள் 24 = 16 திண்மச் சமபகுதியங்கள்:
நான்கு அணுக்கூட்டங்கள் இணைக்கப்பட்ட காபன் அணுவில், அக் கூட்டங்கள் ஒரு வெளியில் இரு வகையாக ஒழுங்கமைக்கப்படலாம். இவ்விரு மூலக்கூறுகளும் மற்றையதின் கண்ணாடி விம்பமாக அமையும். எனவே இங்கு, ஒரு மூலக்கூறின் வலப்புறமுள்ள கூட்டம் மற்றைய மூலக்கூறின் இடப்புறமாக அமையும். இவ்வாறு தமது விம்பத்துடன் மேற்பொருந்த முடியாத மூலக்கூறுகள் சமச்சீரற்றவை எனப்படும்.
References
[தொகு]- ↑ Stereochemistry of Organic Compounds Ernest L. Eliel, Samuel H. Wilen
- ↑ IUPAC definition http://goldbook.iupac.org/A00479.html