அரீனியசுச் சமன்பாடு: திருத்தங்களுக்கு இடையிலான வேறுபாடு
உள்ளடக்கம் நீக்கப்பட்டது உள்ளடக்கம் சேர்க்கப்பட்டது
அடையாளம்: 2017 source edit |
|||
| வரிசை 7: | வரிசை 7: | ||
:<math>k = A e^{-E_a/(R T)}</math> |
:<math>k = A e^{-E_a/(R T)}</math> |
||
Where |
|||
*{{mvar|k}} |
*{{mvar|k}} - [[வினைவேக மாறிலி]] |
||
*{{mvar|T}} |
*{{mvar|T}} - [[வெப்பநிலை]] ([[கெல்வின்]]) |
||
*{{mvar|A}} |
*{{mvar|A}} - [[அதிர்வு காரணி]] |
||
*{{mvar|E<sub>a</sub>}} |
*{{mvar|E<sub>a</sub>}} - [[செயலூக்க ஆற்றல்]] |
||
*{{mvar|R}} |
*{{mvar|R}} - [[வளிம மாறிலி]]:<ref name="Arrhenius96"/><ref name="Arrhenius226"/><ref name="Laidler42"/> |
||
இச்சமன்பாட்டைக் கீழ்க்கண்டவாறும் எழுதலாம். |
இச்சமன்பாட்டைக் கீழ்க்கண்டவாறும் எழுதலாம். |
||
:<math>k = A e^{-E_a/(k_B T)}</math> |
:<math>k = A e^{-E_a/(k_B T)}</math> |
||
Where |
|||
*{{mvar|k}} |
*{{mvar|k}} - [[வினைவேக மாறிலி]] |
||
*{{mvar|T}} |
*{{mvar|T}} - [[வெப்பநிலை]] ([[கெல்வின்]]) |
||
*{{mvar|A}} |
*{{mvar|A}} - [[அதிர்வு காரணி]] |
||
*{{mvar|E<sub>a</sub>}} |
*{{mvar|E<sub>a</sub>}} - [[செயலூக்க ஆற்றல்]] |
||
*{{mvar|k<sub>B</sub>}} |
*{{mvar|k<sub>B</sub>}} - [[போல்ட்சுமான் மாறிலி]] |
||
==மேற்கோள்கள்== |
==மேற்கோள்கள்== |
||
04:21, 9 சூன் 2017 இல் நிலவும் திருத்தம்
அரீனியசுச் சமன்பாடு (Arrhenius equation) என்பது வேதிவினைவேகத்தின் வெப்பநிலைச் சார்பைக் காட்டும் ஒரு வாய்பாடு ஆகும். யாக்கோபு என்றிக்கசு வான் தாஃபு என்னும் டச்சுக்காரரின் 1884ஆம் ஆண்டுப் பணியை ஒட்டி, 1889-இல் அரீனியசு இதனை முன்மொழிந்தார். இச்சமன்பாட்டிற்கு வினைவேகவியலிலும், செயலூக்க ஆற்றல் கணக்கிடவும் பெரும் பங்குண்டு. [1][2][3]
வரலாற்றடிப்படையில் பொதுவான கருத்தாகச் சொன்னால், அறைவெப்பத்தில் நிகழும் பரவலான சில வேதி வினைகளில், வெப்பநிலையில் ஒவ்வொரு 10 பாகை செல்சியசு அதிகரிப்பிற்கும், வினைவேகமானது இரட்டிக்கும்.[4]
சமன்பாடு
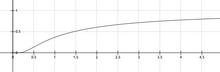
- k - வினைவேக மாறிலி
- T - வெப்பநிலை (கெல்வின்)
- A - அதிர்வு காரணி
- Ea - செயலூக்க ஆற்றல்
- R - வளிம மாறிலி:[1][2][3]
இச்சமன்பாட்டைக் கீழ்க்கண்டவாறும் எழுதலாம்.
- k - வினைவேக மாறிலி
- T - வெப்பநிலை (கெல்வின்)
- A - அதிர்வு காரணி
- Ea - செயலூக்க ஆற்றல்
- kB - போல்ட்சுமான் மாறிலி
மேற்கோள்கள்
- ↑ 1.0 1.1 Arrhenius, S.A. (1889). "Über die Dissociationswärme und den Einfluß der Temperatur auf den Dissociationsgrad der Elektrolyte". Z. Phys. Chem. 4: 96–116. doi:10.1515/zpch-1889-0108.
- ↑ 2.0 2.1 Arrhenius, S.A. (1889). "Über die Reaktionsgeschwindigkeit bei der Inversion von Rohrzucker durch Säuren". ibid. 4: 226–248.
- ↑ 3.0 3.1 Laidler, K. J. (1987) Chemical Kinetics,Third Edition, Harper & Row, p.42
- ↑ Pauling, L.C. (1988) General Chemistry, Dover Publications


