2-சயனோகுவானிடின்
| |||
| பெயர்கள் | |||
|---|---|---|---|
| ஐயூபிஏசி பெயர்
2- சயனோகுவானிடின்
| |||
| வேறு பெயர்கள்
சயனோகுவானிடின், டைசயனோடையமைடு, என்-சயனோகுவானிடின், 1-சயனோகுவானிடின், குவானிடின்-1-கார்போநைட்ரைல், டைசயன்டையமீன், டைடின், டி.சி.டி, டை.சை
| |||
| இனங்காட்டிகள் | |||
| 461-58-5 | |||
| ChemSpider | 9611 | ||
| EC number | 207-312-8 | ||
| யேமல் -3D படிமங்கள் | Image | ||
| பப்கெம் | 10005 | ||
| வே.ந.வி.ப எண் | ME9950000 | ||
SMILES
| |||
| பண்புகள் | |||
| C2H4N4 | |||
| வாய்ப்பாட்டு எடை | 84.08 கி/மோல் | ||
| தோற்றம் | வெண் படிகங்கள் | ||
| அடர்த்தி | 1.400 கி/செ.மீ3 | ||
| உருகுநிலை | 209.5 °C (409.1 °F; 482.6 K) | ||
| கொதிநிலை | 252 °C (486 °F; 525 K) | ||
| 41.3 கி/லி | |||
| மட. P | -0.52 | ||
என்றியின் விதி
மாறிலி (kH) |
2.25•10−10 வளிமண்டல .மீட்டர்3/மோல் | ||
| -44.55•10−6 செ.மீ3/மோல் | |||
| தீங்குகள் | |||
| முதன்மையான தீநிகழ்தகவுகள் | தீங்கானது (Xn) | ||
| R-சொற்றொடர்கள் | R20/21/22 | ||
| S-சொற்றொடர்கள் | S24/25 | ||
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |||
| | |||
| Infobox references | |||
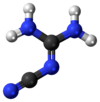
2-சயனோகுவானிடின் (2-Cyanoguanidine) என்பது C2H4N4 என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட ஒரு கரிம வேதியியல் சேர்மமாகும். குவானிடின் சேர்மத்திலிருந்து வழிப்பொருளாக வருவிக்கப்படும் நைட்ரைல் சேர்மம் இதுவாகும். சயனமைடினுடைய இருபடிச் சேர்மமாகவும் இது கருதப்படுகிறது. சயனமைடில் இருந்தே 2-சயனோகுவானிடின் தயாரிக்கப்படுகிறது. இதுவொரு நிறமற்ற திண்மமாகும். தண்ணீர், அசிட்டோன், ஆல்ககால் போன்ற முனைவுக் கரைப்பான்களில் 2-சயனோகுவானிடின் கரைகிறது. பென்சீன், எக்சேன் போன்ற முனைவற்ற கரிமக் கரைப்பான்களில் இது கரைவதில்லை[1].
தயாரிப்பும் பயனும்[தொகு]
சயனமைடுடன் ஒரு காரத்தைச் சேர்த்து சூடுபடுத்தி 2-சயனோகுவானிடினைத் தயாரிக்கிறார்கள். சயனமைடு சேர்மம் சிதைக்கப்படுவதால் மண்ணில் இது உருவாகிறது. 2-சயனோகுவானிடின், குவானிடின்கள், மெலாமைன்கள் போன்ற சேர்மங்களிலிருந்து பல்வேறு வகையான பயனுள்ள பொருட்கள் தயாரிக்கப்படுகின்றன. உதாரணமாக, அசிட்டோகுவானமைன், பென்சோகுவானமைன் போன்ற கரிமச் சேர்மங்கள் சயனோகுவானிடினுடன் நைட்ரைலைச் சேர்த்து ஒடுக்க வினைக்கு உட்படுத்துவதால் தயாரிக்கப்படுகிறது:[2][3]
- (H2N)2C=NCN + RCN → (CNH2)2(CR)N3.
சயனோகுவானிடினை மெது உரமாகவும் பயன்படுத்துகிறார்கள். முன்னதாக இது சில வெடிபொருட்களில் எரிபொருளாகப் பயன்படுத்தப்பட்டது. பிசின் தொழிற்சாலைகளில் ஈப்பாக்சி பிசின்களை நீராற்றும் முகவராகவும் பயன்படுத்துகிறார்கள்[1]
வேதியியல்[தொகு]
2-சயனோகுவானிடின் இரண்டு வகையான வடிவ மாற்றியங்களைக் கொண்டுள்ளது. இவை புரோட்டானேற்றத்திலும் நைட்ரைல் குழு இணைந்துள்ள நைட்ரசன் அணுவுடன் ஏற்பட்டுள்ள பிணைப்பிலும் வேறுபடுகின்றன.
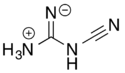
நைட்ரசன்களின் முறை சார்ந்த அமில கார வினை வழியாக உருவாகி இருமுனை அயனியாகவும் 2-சயனோகுவானிடின் காணப்படுகிறது.
இருமுனை அயனி வடிவிலிருந்து அமோனியா (NH3) நீக்கமும் தொடர்ந்து எஞ்சியுள்ள மைய நைட்ரசன் அணுவின் புரோட்டான் நீக்கத்தாலும் டைசயனமைடு [N(CN)2]− எதிர்மின் அயனி உருவாகிறது.
மேற்கோள்கள்[தொகு]
- ↑ 1.0 1.1 Thomas Güuthner (2006). "Cyanamides". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. DOI:10.1002/14356007.a08_139.pub2.
- ↑ "Amino Resins". Ullmann's Encyclopedia of Industrial Chemistry. (2012). Wiley-VCH. DOI:10.1002/14356007.a02_115.pub2.
- ↑ J. K. Simons, M. R. Saxton (1953). "Benzoguanamine". Organic Syntheses 33: 13. doi:10.15227/orgsyn.033.0013.