பொட்டாசியம் எத்தில் சேந்தேட்டு
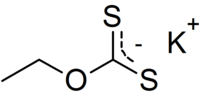
| |
| |
| பெயர்கள் | |
|---|---|
| ஐயூபிஏசி பெயர்
பொட்டாசியம் ஆ-எத்தில்கார்பனோடைதயோயேட்டு
| |
| வேறு பெயர்கள்
பொட்டாசியம் எத்தில்சேந்தோகெனேட்டு
பொட்டாசியம்-ஆ-எத்தில் டைதயோகார்பனேட்டு | |
| இனங்காட்டிகள் | |
| 140-89-6 | |
| ChemSpider | 8491 |
| யேமல் -3D படிமங்கள் | Image |
| பப்கெம் | 2735045 |
SMILES
| |
| பண்புகள் | |
| C3H5KOS2 | |
| வாய்ப்பாட்டு எடை | 160.29 g·mol−1 |
| தோற்றம் | வெளிர் மஞ்சள் தூள் |
| அடர்த்தி | 1.263 கி/செ.மீ3[1] |
| உருகுநிலை | 225 முதல் 226 °C (437 முதல் 439 °F; 498 முதல் 499 K) |
| கொதிநிலை | சிதைவடையும் |
| காடித்தன்மை எண் (pKa) | தோராயமாக 1.6 |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
| | |
| Infobox references | |
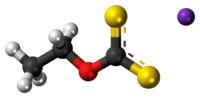
பொட்டாசியம் எத்தில் சேந்தேட்டு (Potassium ethyl xanthate) என்பது CH3CH2OCS2K என்ற மூலக்கூற்று வாய்ப்பாட்டால் விவரிக்கப்படும் ஒரு கனிமச் சேர்மம் ஆகும். கரிமக் கந்தகச் சேர்மமான இச்சேர்மம் வெளிர் மஞ்சள் நிறத்தில் தூளாகக் காணப்படுகிறது. தாதுக்களை தனித்துப் பிரிக்க கனிமவியல் துறையினர் இச்சேர்மத்தைப் பயன்படுத்துகிறார்கள். தொடர்புடைய சோடியம் எத்தில் சேந்தேட்டு போல அல்லாமல் பொட்டாசியம் எத்தில் சேந்தேட்டு ஓர் நீரிலி உப்பாக காணப்படுகிறது.
தயாரிப்பு[தொகு]
கார்பன் டை சல்பைடு மீது அல்காக்சைடுகள் வினைபுரிவதால் சேந்தேட்டு உப்புகள் உருவாகின்றன. வினைக்குத் தேவையான அல்காக்சைடு பொட்டாசியம் ஐதராக்சைடிலிருந்து வினைநிகழும் தளத்திலேயே தயாரித்துக் கொள்ளப்படுகிறது[2]
- CH3CH2OH + CS2 + KOH → CH3CH2OCS2K + H2O.
பண்புகள்[தொகு]
பொட்டாசியம் எத்தில் சேந்தேட்டு வெளிர் மஞ்சள் நிற தூளாகக் கிடைக்கிறது. உயர் pH நிலையில் நிலைப்புத்தன்மையோடு இருக்கும் இச்சேர்மம் 25 பாகை செல்சியசு வெப்பநிலையில் pH 9 நிலையில் விரைவாக நீராற்பகுப்பு அடைகிறது. சோடியம் வழிப்பெறுதிகளைப் போலல்லாமல் பொட்டாசியம் சேந்தேட்டு நீரிலி உப்பாக படிகமாகிறது. எனவே இச்சேர்மம் நீரை உறிஞ்சுவதில்லை.
பயன்பாடுகள்[தொகு]
தாமிரம், நிக்கல், வெள்ளி போன்ற தனிமங்களின் தாதுக்களைப் பிரித்தெடுக்கும் சுரங்கத் தொழிற்சாலைகளில் பொட்டாசியம் எத்தில் சேந்தேட்டு ஒரு நுரைமிதப்பு முகவராக பயன்படுத்தப்படுகிறது. [3] இத்தகைய மென் உலோகங்களை கரிமகந்தக ஈந்தணைவிகளுக்காக ஈர்ப்பதற்கு இம்முறை பயன்படுத்தப்படுகிறது. ஆல்க்கைல் மற்றும் அரைல் ஆலைடுகளிலிருந்து சேந்தேட்டு எசுத்தர்களை தயாரிப்பதற்கு பொட்டாசியம் சேந்தேட்டு ஒரு பயனுள்ள வினையாக்கியாகப் பயன்படுகிறது. கரிமத் தொகுப்பு வினைகளில் இச்சேந்தேட்டுகள் பயனுள்ள இடைநிலைகளாகப் பயன்படுகின்றன [4].
தற்காப்பு[தொகு]
எலிகளுக்கு வாய்வழியாகக் கொடுக்கும்போது பொட்டாசியம் சேந்தேட்டின் உயிர் கொல்லும் அளவு LD50 683 மி.கி/கி.கி ஆகும் [3].
மேற்கோள்கள்[தொகு]
- ↑ Report 5 (1995) p. 5
- ↑ This report gives a detailed procedure Charles C. Price and Gardner W. Stacy (1948). "p-nitrophenyl) sulfide". Organic Syntheses 28: 82. http://www.orgsyn.org/demo.aspx?prep=CV3P0667.; Collective Volume, vol. 3, p. 667
- ↑ 3.0 3.1 Kathrin-Maria Roy (2005). "Xanthates". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. DOI:10.1002/14356007.a28_423.
- ↑ One of several procedures using xanthate esters: Fabien Gagosz and Samir Z. Zard (1948). "A Xanthate-Transfer Approach to α-Trifluoromethylamines". Organic Syntheses 84: 32. http://www.orgsyn.org/demo.aspx?prep=V84P0032.; Collective Volume, vol. 11, p. 212
