சோடியம் டெட்ராகுளோரோ ஆரேட்டு
 | |
| பெயர்கள் | |
|---|---|
| ஐயூபிஏசி பெயர்
சோடியம் டெட்ராகுளோரோ ஆரேட்டு(III)
| |
| வேறு பெயர்கள்
சோடியம் தங்க குளோரைடு, மஞ்சள் தங்க குளோரைடு.
| |
| இனங்காட்டிகள் | |
| (நீரிலி), 13874-02-7 (இருநீரேற்று) 15189-51-2 (நீரிலி), 13874-02-7 (இருநீரேற்று) | |
| ChemSpider | 25247 |
| EC number | 239-241-3 |
InChI
| |
| யேமல் -3D படிமங்கள் | Image |
| பப்கெம் | 27127 |
SMILES
| |
| பண்புகள் | |
| NaAuCl4 | |
| வாய்ப்பாட்டு எடை | 361.756 கி/மோல் |
| தோற்றம் | ஆரஞ்சு தங்கநிற திண்மம் |
| அடர்த்தி | 0.8கி/மி.லி (20° செல்சியசு )[2] |
| 139 கி/மி.லி (10°செல்சியசு) 151 கி/மி.லி (20° செல்சியசு) 900 கி/மி.லி (60° செல்சியசு )[3] | |
| கரைதிறன் | டையெத்தில் ஈதரில் சிறிதளவு கரையும்[4] |
| தீங்குகள் | |
| GHS pictograms |  
|
| GHS signal word | அபாயம் |
| H315, H319, H335 | |
| P261, P264, P271, P280, P302+352, P332+313, P305+351+338, P337+313, P304+340, P312, P330, P333+313, P363, P403+233 | |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
| Infobox references | |
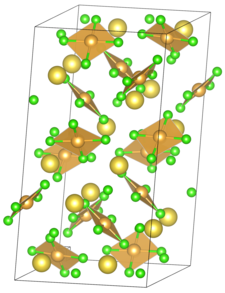
சோடியம் டெட்ராகுளோரோ ஆரேட்டு (Sodium tetrachloroaurate) என்பது NaAuCl4 என்ற மூலக்கூற்று வாய்ப்பாட்டால் விவரிக்கப்படும் ஒரு கனிம வேதியியல் சேர்மமாகும். Na+ மற்றும் AuCl4- அயனிகள் சேர்ந்து சோடியம் டெட்ராகுளோரோ ஆரேட்டு உருவாகிறது. நீரிலி மற்றும் இருநீரேற்று நிலைகளில் வணிக ரீதியாகவும் கிடைக்கிறது [6]. அறை வெப்பநிலையில் இச்சேர்மம் தங்க ஆரஞ்சு நிறத்தில் ஒரு திண்மமாக தோன்றுகிறது.
தயாரிப்பு[தொகு]
டெட்ராகுளோரோ ஆரிக் அமிலக் கரைசலுடன் சோடியம் குளோரைடு அல்லது சோடியம் கார்பனேட்டு சேர்த்து ஒரு கலவை தயாரிக்கப்படுகிறது. 100 பாகை செல்சியசு வெப்பநிலையில் இக்கலவை நன்றாக கிளறப்பட்டு ஆவியாக்கம், குளிரூட்டம், படிகமாக்கம் ஆகிய தொடர் நடவடிக்கைகள் மூலமாக பாரம்பரியமாக இவ்வுப்பு தயாரிக்கப்படுகிறது. இறுதியாக நன்கு உலர்த்தப்பட்டு சோடியம் டெட்ராகுளோரோ ஆரேட்டின் ஆரஞ்சு நிறப் படிகங்கள் பெறப்படுகின்றன[7] [4].
இருப்பினும் தற்காலத்தில் தங்கத்துடன் சோடியம் ஆக்சி-ஆலசன் உப்புகளும் ஐதரோகுளோரிக் அமிலமும் சேர்த்து சோடியம் டெட்ராகுளோரோ ஆரேட்டை தயாரிக்கும் நவீன் தயாரிப்பு முறைகள் பின்பற்றப்படுகின்றன[7].
பயன்கள்[தொகு]
அசிட்டிலீனை ஐதரோகுளோரினேற்றம் செய்யும் வினைக்கு வினையூக்கியாகப் பயன்படுதல், சல்பைடுகளை ஆக்சிசனேற்றுதல் போன்ற பல்வகை பயன்பாட்டுகளுக்கு இது பயன்படுகிறது [4]
மேற்கோள்கள்[தொகு]
- ↑ PubChem. "Sodium tetrachloroaurate". pubchem.ncbi.nlm.nih.gov (in ஆங்கிலம்). பார்க்கப்பட்ட நாள் 2019-05-19.
- ↑ "13874-02-7 - Sodium tetrachloroaurate(III) dihydrate, Premion®, 99.99% (metals basis), Au 49-50% - Sodium chloroaurate(III) - Gold sodium chloride - 12148 - Alfa Aesar". www.alfa.com. பார்க்கப்பட்ட நாள் 2019-05-19.
- ↑ Perry, Dale L. (2011). Handbook of Inorganic Compounds. CRC Press; 2 edition (May 18, 2011). பக். 380. பன்னாட்டுத் தரப்புத்தக எண்:9781439814611.
- ↑ 4.0 4.1 4.2 Westcott, Stephen A. (2001), "Sodium Tetrachloroaurate(III)", Encyclopedia of Reagents for Organic Synthesis (in ஆங்கிலம்), American Cancer Society, doi:10.1002/047084289x.rs108, ISBN 9780470842898
- ↑ "Sodium Tetrachloroaurate". www.espimetals.com. பார்க்கப்பட்ட நாள் 2019-05-20.
- ↑ PubChem. "Sodium tetrachloroaurate". pubchem.ncbi.nlm.nih.gov (in ஆங்கிலம்). பார்க்கப்பட்ட நாள் 2019-05-19.
- ↑ 7.0 7.1 20180208476, "Method of Making Inorganic Gold Compound", issued 2018-07-26

![{\displaystyle {\ce {H[AuCl4] + NaCl -> Na[AuCl4] + HCl}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/33a4338b58853589f262049d2a0b10f0ba9db840)
![{\displaystyle {\ce {2H[AuCl4] + Na2CO3 -> 2Na[AuCl4] + H2O + CO2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9f7b32ba19756b1e1480e2fa001033f139de3ffb)