கனிம வேதியியல்

A: டைபோரேன்
B: சீசியம் குளோரைடு
C: வளையபென்டாடையீனைல் இரும்பு டைகார்பனைல் இருபடி
D: பாலிடைமெத்தில்சிலாக்சேன்
E: கிரப்சு வினையூக்கி
F: சியோலைட்டுகள்
G: தாமிர(II) அசிட்டேட்டு
கனிம வேதியியல் (Inorganic chemistry) என்பது கரிமம் அல்லாத சேர்மங்கள் மற்றும் கரிமவுலோகச் சேர்மங்கள் முதலானவற்றின் நடத்தைகளையும் அவற்றின் தயாரிப்பு முறைகளையும் விவரிக்கின்ற ஓர் வேதியியல் பிரிவு ஆகும். அசேதன இரசாயணம் என்ற பெயராலும் அழைக்கப்படும் இப்பிரிவு மிகவிரிவாக வளர்ச்சியடைந்துள்ள கரிமச் சேர்மங்கள் (பெரும்பாலும் C-H பிணைப்புக் கொண்ட சேர்மங்கள்) தவிர்த்து, அனைத்து வகையான வேதிச் சேர்மங்களையும் ஆராய்கின்றது. C-H பிணைப்புக் கொண்ட சேர்மங்கள் கரிம வேதியியல் என்ற வேதியியல் பிரிவில் ஆராயப்படுகின்றன. இரண்டு துறைகளுக்கும் இடையில் உள்ள வேறுபாடானது, கரிமவுலோக வேதியியல் என்ற இவற்றின் துணைப்பிரிவு காரணமாக முழுமையில் இருந்து வெகு தொலைவுக்கு விலகியுள்ளது. வினையூக்கி, பொருள் அறிவியல், நிறமிகள், புறப்பரப்புச் செயலிகள், மேற்பூச்சுகள், மருந்துகள், எரிபொருட்கள் மற்றும் விவசாயம் உள்ளிட்ட அறிவியல் துறைகளின் ஒவ்வொரு அம்சத்திலும் கரிமவுலோக வேதியியல் பயன்பாடுகளை கொண்டிருக்கிறது [1].

பல கனிமச் சேர்மங்கள் நேர்மின் அயனிகளும் எதிர்மின் அயனிகளும் அயனிப் பிணைப்பால் பிணைக்கப்பட்டுள்ள அயனிச் சேர்மங்களாகும். மக்னீசியம் குளோரைடு, சோடியம் ஆக்சைடு போன்றவை அயனிச்சேர்மத்துக்கு எடுத்துக்காட்டுகளாகும். மக்னீசியம் நேர்மின் அயனியும் (Mg2+) குளோரைடு எதிர்மின் அயனியும் இணைந்து மக்னீசியம் குளோரைடும் சோடியம் நேர்மின் அயனியும் ஆக்சைடு (O2−) எதிர்மின் அயனியும் இணைந்து சோடியம் ஆக்சைடும் உருவாகியுள்ளன. எந்தவொரு உப்பை எடுத்துக் கொண்டாலும் அயனிகளின் மின்சுமைக்கு ஈடாக நடுநிலையாக்கப்படும் வகையில் எதிர் அயனிகளைப் பெற்று உப்பு நடுநிலையில் இருக்குமாறு அமைகிறது. உப்பில் உள்ள அயனிகள் ஆக்சிசனேற்ற நிலை எண்ணால் குறிக்கப்படுகின்றன. நேர்மின் அயனியெனில் அயனியாக்கும் திறனிலிருந்தும், எதிர்மின் அயனியெனில் அணுக்கரு நாட்டத்திலிருந்தும் தாய்த்தனிமங்களிலிருந்து உப்புகளின் உருவாக்கத்தை உய்த்துணர முடிகிறது.
ஆக்சைடுகள், கார்பனேட்டுகள், சல்பேட்டுகள், மற்றும் ஆலைடுகள் போன்றவை கனிமச் சேர்மங்களின் முக்கியமான சில வகைபாடுகளாகும். பல கனிமச் சேர்மங்கள் உயர் உருகுநிலையால் வகைப்படுத்தப்படுகின்றன. கனிம உப்புக்கள் பொதுவாக திட நிலையில் நல்ல கடத்திகள் என்று கருதப்படுவதில்லை. உயர் கொதிநிலையும் படிகமாகும் தன்மையும் கனிமச்சேர்மங்களின் சிறப்பு அம்சங்களாகும். சில உப்புகள் தண்ணீரில் அதிகமாக கரைகின்றன (சோடியம் குளோரைடு). சில உப்புகள் சரியாகக் கரைவதில்லை (சிலிக்கன் டையாக்சைடு).
இரட்டை இடப்பெயர்ச்சி வினை கனிம வேதியியலின் எளிய வினை வகையாகக் கருதப்படுகிறது. இரண்டு உப்புக்களை ஒன்றாகக் கலக்கும் போது அவற்றின் ஆக்சிசனேற்ற நிலையில் எந்த மாற்றமும் அடையாமல் அயனிகள் பரிமாறிக் கொள்ளப்படுகின்றன. ஒடுக்க-ஏற்ற வேதிவினைகளில் ஒரு வினைபடுபொருள் அதாவது ஆக்சிசனேற்றி அதன் ஆக்சிசனேற்ற நிலையில் குறைகிறது மற்றும் மற்றொரு வினைபடுபொருள் அதாவது ஒடுக்கி, அதன் ஆக்சிசனேற்ற நிலையில் உயர்கிறது. நிகர விளைவு எலக்ட்ரான்கள் பரிமாற்றப்படுகின்றன என்பதே இவ்வினையின் நிகர விளைவாகும். எலக்ட்ரான் பரிமாற்றம் மறைமுகமாகவும் சில சூழ்நிலைகளில் நிகழ்கிறது, உதாரணம், மின்வேதியியலின் முக்கிய அம்சமான மின்கலன்களில் மறைமுகமாக எலக்ட்ரான் பரிமாற்றம் நிகழ்கிறது.
ஒரு வினைபடுபொருளில் ஐதரசன் அணுக்கள் இருந்தால், அது ஈடுபடும் வினையில் புரோட்டான் பரிமாற்றம் நிகழ்கிறது. அமில கார வேதியியலில் இவ்வகை வினைகள் நிகழ்கின்றன. எலக்ட்ரான் இணைகளுடன் பிணையும் வல்லமை பெற்ற வேதியியல் இனங்கள் அனைத்தும் இலூயிக் அமிலங்கள் எனப்படுகின்றன என பொதுவாக வரையறுக்கப்படுகிறது. இதேபோல எலக்ட்ரான் இணையை வழங்கும் வல்லமை பெற்ற எந்தவொரு வேதி இனமும் இலூயிக் காரம் எனவும் பொதுவாக வரையறுக்கப்படுகிறது. அமில கார இடைவினைகளை ஆய்வுசெய்கையில் பியர்சன் அமிலக் காரக் கோட்பாடு கணக்கில் எடுத்துக் கொள்ளப்படுகிறது. முனைவாகுந்திறனும் அயனிகளின் அளவும் கணக்கில் எடுத்துக் கொள்ளப்படுகின்றன.
கனிமச் சேர்மங்கள் இயற்கையில் கனிமங்களாகக் காணப்படுகின்றன. மண்ணில் பைரைட்டு என்ற பெயரில் இரும்பு சல்பைடும் அல்லது கிப்சம் என்ற பெயரில் கால்சியம் சல்பேட்டும் கலந்துள்ளன. மேலும் உயிர்மூலக்கூறுகளில் கனிம சேர்மங்கள் பண்முகத்தன்மையை கொண்டுள்ளன. ஆற்றல் சேமிப்பில் மின்பகுளியாக (சோடியம் குளோரைடு), அல்லது கட்டுமானத்தில் பாலிபாசுபேட்டாக (டிஎன்ஏ வின் முதுகெலும்பாக) இவை செயல்படுகின்றன.
முதல் முக்கியமான மனிதனால் உருவாக்கப்பட்ட முதலாவது முக்கியமான கனிமச் சேர்மம் அமோனியம் நைட்ரேட்டு ஆகும். மண் வளத்தை அதிகரிப்பதற்காக ஏபர் செயல்முறை மூலம் இச்சேர்மம் உருவாக்கப்பட்டது. வனேடியம் (V) ஆக்சைடு, தைட்டானியம் (III) குளோரைடு போன்ற சேர்மங்கள் வினையூக்கியாகப் பயன்படுத்துவதற்காகத் தொகுப்பு முறையில் தயாரிக்கப்பட்டன. இலித்தியம் அலுமினியம் ஐதரைடு போன்ற சேர்மங்கள் கரிம வேதியியல் வினைப்பொருளாகப் பயன்படுத்த தொகுக்கப்பட்டன.
கரிம உலோக வேதியியல், கொத்து வேதியியல், உயிர்கனிம வேதியியல் முதலியன கனிம வேதியியலின் துணைப்பிரிவுகளாகும்.புதிய வினையூக்கிகள், மீக்கடத்திகள், சிகிச்சைகள் முதலியனவற்றை நோக்கமாகக் கொண்டு கனிம. வேதியியலின் இத்துறைகள் விரிவாக ஆராய்ச்சி செய்யப்படுகின்றன.
தொழிற்சாலைக் கனிம வேதியியல்[தொகு]
நடைமுறையில் மிகவும் பயனுள்ள ஒரு அறிவியல் பகுதியாக கனிம வேதியல் பிரிவு காணப்படுகிறது. பாரம்பரியமாக, கந்தக அமிலத்தின் உற்பத்தியை மதிப்பீடு செய்து ஒரு நாட்டின் பொருளாதாரத்தின் அளவை மதிப்பிட முடியும். கனடா, சீனா, இந்தியா, சப்பான் ஐரோப்பா அமெரிக்கா போன்றவை 2005 ஆம் கணக்கீட்டின்படி உச்சத்தில் உள்ள 20 கனிமவேதியியல் சேர்மங்களை உற்பத்தி செய்துள்ளன :[2].
அலுமினியம் சல்பேட்டு, அமோனியா அமோனியம் நைட்ரேட்டு, அமோனியம் சல்பேட்டு, கார்பன் கருப்பு, குளோரின், ஐதரோகுளோரிக் அமிலம், ஐதரசன், ஐதரசன் பெராக்சைடு நைட்ரிக் அமிலம், நைட்ரசன், ஆக்சிசன், பாசுபாரிக் அமிலம், சோடியம் கார்பனேட்டு, சோடியம் குளோரேட்டு, சோடியம் ஐதராக்சைடு, சோடியம் சிலிகேட்டு, சோடியம் சல்பேட்டு, கந்தக அமிலம் மற்றும் டைட்டானியம் டை ஆக்சைடு போன்றவை உச்சத்திலுள்ள கனிம வேதியியல் சேர்மங்கள் ஆகும். கனிம வேதியியல் சேர்மங்கள் உரங்கள் தயாரிக்கப் பயன்படுகின்ற்ன என்பது மற்றுமொரு முக்கியமான பயனாகும்.
விளக்கக் கனிம வேதியியல்[தொகு]
சேர்மங்களின் பண்புகளின் அடிப்படையில் கனிமச் சேர்மங்களை வகைப்படுத்தி ஆய்வது விளக்கக் கனிம வேதியியல் பிரிவு ஆகும். தனிம வரிசை அட்டவணையில் ஒரு தனிமம் பெற்றிருக்கும் இடத்தை அடிப்படையாகக் கொண்டும், அதாவது உயர் அணு எடை கொண்ட தனிமம் என்ற அடிப்படையிலும் இவ்வகைப்பாட்டின் ஒருபகுதி அமைகிறது. கட்டமைப்பு ஒற்றுமையின் அடிப்படையிலும் சில தனிமங்கள் குழுக்களாகப் பகுக்கப்படுகின்றன. அசேதன சேர்மங்களைப் படிக்கும் போது, பெரும்பாலும் கனிம வேதியியலின் வெவ்வேறு வகைப்பாடுகளை எதிர்கொள்ள வேண்டியுள்ளது. ஒரு கரிம உலோகச் சேர்மம் அதன் ஒருங்கிணைப்பு வேதியியல் அடிப்படையில் வகைப்படுத்தப்படுகிறது. சில ஆர்வமூட்டும் திட நிலைப் பண்புகளை இவை வெளிப்படுத்துகின்றன. பலவகை வகைப்பாடுகள் இங்கு தரப்படுகின்றன.
அணைவுச் சேர்மங்கள்[தொகு]
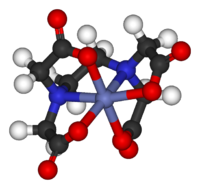
பாரம்பரிய அணைவுச் சேர்மங்களில் H2O, NH3, Cl−, மற்றும் CN− போன்ற முதன்மைக்குழு அணுக்களின் ஈனிகளுடன் உலோகங்கள் இணை எலக்ட்ரான்களுடன் பிணைக்கப்பட்டிருக்கும். நவீன அணைவுச் சேர்மங்களில் அநேகமாக அனைத்து கரிம மற்றும் கனிமச் சேர்மங்களும் ஈனிகளாக பயன்படுத்தப்படுகின்றன. வழக்கமாக 3-13 தொகுதிகளில் இடம்பெற்றிருக்கும் உலோகங்களும், மாறுபக்க-இலாந்தனைடுகளும், மாறுபக்க-ஆக்டினைடுகளும் மட்டுமே உலோகங்களாக கருதப்படும். ஆனால் நிச்சயமாக வோறொரு கண்ணோட்டத்தில் எல்லா வேதிச் சேர்மங்களையுமே அணைவுச் சேர்மங்களாகக் கருதமுடியும்.
அணைவுச் சேர்மங்களின் முப்பரிமாண வேதியியல் வெர்னர் கொள்கையின் குறிப்பின்படி பலமாக உள்ளது. [Co((OH)2Co(NH3)4)3]6+ இன் இரண்டு எதிருருக்களை பிரிக்கும் தொடக்கக்கால வெர்னரின் கொள்கையில் கரிமச் சேர்மங்களில் சமச்சீர்மை உள்ளார்ந்ததாக இல்லை. இந்த சிறப்பம்சத்தில் பெருமூலக்கூறு ஒருங்கிணைப்பு வேதியியல் கூறுகள் உட்பொதிந்துள்ளன [3]
- எடுத்துக்காட்டுகள்: [Co(EDTA)]−, [Co(NH3)6]3+, TiCl4(THF)2.
முதன்மைக் குழு சேர்மங்கள்[தொகு]
தனிமவரிசை அட்டவனையில் உள்ள ஐதரசன் தவிர்த்த 1,2 மற்றும் 13-18 தொகுதிகளைச் சேர்ந்த தனிமங்கள் இவ்வினத்தில் இடம்பெறுகின்றன. பெரும்பாலும் ஒரே மாதிரியான வினைத்திறனைப் பெற்றிருப்பதால் 3 வது தொகுதியிலுள்ள (Sc, Y, மற்றும் La) தனிமங்களும் 12 வது தொகுதியிலுள்ள (Zn, Cd, மற்றும் Hg) தனிமங்களும் பொதுவாக இவ்வினத்தில் சேர்க்கப்படுகின்றன.[4].
வேதியியல் தொடங்கிய காலந்தொட்டே அடிப்படை கந்தகம் மற்றும் வடிகட்ட இயன்ற வெண் பாசுபரசு போன்ற முதன்மைக் குழு சேர்மங்கள் அறியப்பட்டிருந்திருக்கின்றன. ஆக்சிஜன் மீதான பரிசோதனைகளை மேற்கொண்ட இலவாய்சியர் மற்றும் சோசப் பிரீசிட்லி இருவரும் முக்கியமான ஈரணுக்கொண்ட வாயுவை அடையாளம் கண்டதுமட்டுமின்றி விகிதவியல் விகிதங்களின்படி சேர்மங்கள் மற்றும் அவற்றின் வினைகளை விவரிக்கின்ற ஒரு புதிய வழியையும் திறந்து வைக்க காரணமாயினர்.
1900 களின் முற்பகுதியில் கார்ல் போசு மற்றும் பிரிட்சு ஏபர் இருவரும் வினையூக்கியாக இரும்பைப் பயன்படுத்தி அமோனியாவை தொகுப்பு முறையில் தயாரித்தனர். நடைமுறையில் சேர்மங்களை தயாரித்தலுக்கு ஓர் உந்துதலையும், ஓர் ஆழமான முக்கியத்துவத்தையும் இத்தொகுப்பு முறை தயாரிப்பு மனிதகுலத்திற்கு அளித்தது. SiO2, SnCl4, மற்றும் N2O. போன்றவை குறிப்பிடத்தகுந்த முதன்மைத் தொகுதி சேர்மங்களாகும். கரிமத் தொகுதிகளைக் கொண்டிருப்பதால் பல முதன்மைத் தொகுதி சேர்மங்கள் கரிம உலோகங்கள் என்று வகைப்படுத்தப்படுகின்றன. உதாரணம்: B(CH3)3). டி. என். ஏ வில் பாசுபேட்டாக இயற்கையிலும் முதன்மை தொகுதி சேர்மங்கள் காணப்படுவதால் இவற்றை உயிர்கனிம சேர்மங்கள் என்றும் வகைப்படுத்தலாம். ஐதரசன் ஈனிகள் இல்லாத ஃபுலரின், கார்பன் நானோகுழாய், இரட்டை கார்பனாக்சைடு போன்ற கரிமச் சேர்மங்களையும் கனிமச் சேர்மங்கள் எனலாம்.
- உதாரணங்கள்: டெட்ராகந்தக டெட்ராநைட்ரைடு (S4N4), டைபோரேன் (B2H6), சிலிக்கோன் மற்றும் ஃபுலரின் C60
இடையுலோகச் சேர்மங்கள்[தொகு]
தனிமவரிசை அட்டவணையில் தொகுதி 4 முதல் 11 வரையில் இடம்பெற்றுள்ள தனிமங்களின் சேர்மங்கள் இடையுலோகச் சேர்மங்கள் எனப்படுகின்றன. தொகுதி 3 இலிருந்து 12 வரை இடம்பெற்றுள்ள தனிமங்களின் சேர்மங்களும் சில சந்தர்ப்பங்களில் இடையுலோகச் சேர்மங்கள் என்ற குழுவுடன் சேர்க்கப்படுகின்றன. இருந்தாலும் இவை முதன்மைக் குழு சேர்மங்களாகவும் கருதப்படுகின்றன.
இடையுலோகச் சேர்மங்கள் அணைவு வேதியியலில் பெருமளவு தொடர்பு கொண்டுள்ளன, தைட்டானியம் தனிமம் நான்முகி புறவெளி அமைப்பையும், சில நிக்கல் அணைவுகள் சதுர தளப் புறவெளி அமைப்பையும் கோபால்ட் தனிமம் எண்முகி புறவெளி அமைப்பையும் வெளிப்படுத்துகின்றன. ஈமோகுளோபின் எனப்படும் இரத்தச் சிவப்பு அணுவில் இடம்பெற்றுள்ள இரும்பைப் போல பல்வேறு இடையுலோகங்கள் உயிரின முக்கியத்துவம் பெற்றுள்ளன.
- உதாரணங்கள்: இரும்பு பென்டாகார்பனைல், தைட்டானியம் டெட்ராகுளோரைடு, சிசுபிளாட்டின்
கரிம உலோகச் சேர்மங்கள்[தொகு]
பொதுவாக கரிம உலோகச் சேர்மங்கள் M-C-H குழுவைப் பெற்றிருக்கும் [5]. இவ்வினத்தில் இடம்பெறும் உலோகம் (M) முதன்மைத் தொகுதி உலோகமாக அல்லது இடைநிலைத் தொகுதி உலோகமாக இருக்கலாம். உலோகக் கார்பனைல்கள் மற்றும் உலோக ஆல்க்காக்சைடுகள் போன்ற கொழுபில் கரையும் சேர்மங்களையும் கரிம உலோகச் சேர்மங்கள் என்ற வகைப்பாட்டில் இணைத்துக் கொள்ளும் வகையில் இவ்வகைப்பாட்டிற்கான வரையறைகள் தளர்த்தப்பட்டுள்ளன.
கரிம உலோகச் சேர்மங்கள் முக்கியமான ஒரு சிறப்பு வகைச் சேர்மங்களாகக் கருதப்படுகின்றன. ஏனெனில் கரிம ஈனிகள் நீராற்பகுப்பு அல்லது ஆக்சிசனேற்றத்தினால் பாதிக்கப்படுகின்றன. பாரம்பரிய வெர்னர் வகை அணைவுகளைக் காட்டிலும் கரிம உலோகச் சேர்மங்கள் அதிசிறப்பு தயாரிப்பு முறைகளை அத்தியாவசியமாகக் கொண்டுள்ளன.
செயற்கை முறைத் தயாரிப்புகள், குறிப்பாக கரைசலில் குறைந்த ஒருங்கிணைப்புக் சக்தி கொண்ட அணைவுகள் ஐதரோ கார்பன்கள், H2, மற்றும் N2 போன்ற வலிமை குறைந்த ஈனிகளுடன் ஒருங்கிணைப்பை வெளிப்படுத்துகின்றன. ஏனெனில் ஏதோ ஒரு வகையில் இவை பெட்ரோ வேதிப்பொருட்கள் ஆகும். கரிம உலோக சேர்மங்கள் பெரிதும் தொழிற்சாலைகளுடன் தொடர்பிலிருக்கும் சேர்மங்களாகக் காணப்படுகின்றன.
- உதாரணங்கள்: பெர்ரோசின், மாலிப்டினம் எக்சாகார்பனைல்
கொத்துச் சேர்மங்கள்[தொகு]
கொத்துச் சேர்மங்களை அனைத்து வகைப் பகுப்பு வேதிச்சேர்மங்களிலும் காணமுடியும். பொதுவாக ஏற்றுக்கொள்ளப்பட்ட வரையறையின் படி, ஒரு கொத்துச் சேர்மம் என்பது, குறைந்தபட்சம் மூன்று அணுக்கள் நேரடியாக ஒன்றுகொன்று முக்கோண வடிவில் பிணைக்கப்பட்டிருக்க வேண்டும். ஆனால் உலோகத்துடன் உலோகம் பிணைக்கப்பட்ட ஈருலோக அணைவுகள் இவ்வகைச் சேர்மங்களுக்கு ஏற்புடையதாகும். தூய கனிம அமைப்புகள், கரிம உலோக வேதியியல், முதன்மைக்குழு வேதியியல், மற்றும் உயிர் கனிமவேதியியல் பிரிவுகளில் கொத்துகள் தோன்றுகின்றன. பெரிய கொத்துகளுக்கும் பெரிய திண்மங்களுக்கும் இடையிலான வேறுபாடுகள் நாளுக்குநாள் அதிகரித்து தெளிவில்லாமல் உள்ளது.
நானோ அறிவியல் அல்லது நானோ தொழில்நுட்பத்தின் வேதியியல் அடிப்படையாக இந்த இடைமுகம் கருதப்படுகிறது. கேட்மியம் செலீனைடின் கொத்துகளை ஆய்வு செய்யும்போது குறிப்பாக குவாண்டம் அளவு விளைவுகள் தொடர்பான ஆய்வுகள் தோன்றுகின்றன. எனவே, ஒரு மூலக்கூறுக்கும் திண்மத்திற்கும் இடையில் பிணைந்துள்ள, வினையிடைப் பண்புள்ள அணுக்களின் அணியை பெரிய கொத்துகள் என்று வரையறுக்கிறார்கள்.
- உதாரணங்கள்: Fe3(CO)12, B10H14, [Mo6Cl14]2−, 4Fe-4S
உயிர்க்கனிம சேர்மங்கள்[தொகு]
வரையறைகளின்படி உயிர்க்கனிம சேர்மங்கள் இயற்கையில் தோன்றுபவையாகும். ஆனால் இவற்றின் துணைப்பிரிவுகளில் மனித இனத்தால் உருவாக்கப்படும் மாசுபடுத்திகள் (மெத்தில் மெர்க்குரி), மருந்துகள் (சிசுபிளேட்டின்) போன்றவை உள்ளடங்குகின்றன [6].
உயிர் வேதியியலின் பல அம்சங்களை உயிர்க்கனிம வேதியியல் உள்ளடக்கியுள்ளது. டிஎன்ஏ வில் உள்ள பாசுபேட்டு, உயிரியல் பெருமூலக்கூறுகள் போன்ற ஈனிகளைப் பெற்றுள்ள உலோக அணைவுகள், இயூமிக் அமிலம் கடோலினியம் அணைவுச் சேர்மங்கள் போன்றவற்றை உயிர்கனிம வேதியியல் உள்ளடக்கியுள்ளது.
பாரம்பரியமாக சுவாசித்தலுடன் தொடர்புடைய எலக்ட்ரான் மற்றும் புரதங்களில் ஆற்றல் மாற்றம் ஆகியவற்றின் மீது இத்துறை கவனம் செலுத்துகிறது. நோய் கண்டறிதல், சிகிச்சையளிக்கும் முறைகள் போன்ர செயல்களுக்குப் பயன்படும் அத்தியாவசியமான மற்றும் அத்தியாவசியமற்ற தனிமங்களைக் குறித்த ஆய்வுகள் முதலியவை மருத்துவக் கனிம வேதியியலுடன் தொடர்பு கொண்டவையாகும்.
- உதாரணங்கள்: ஈமோகுளோபின், மெத்தில் மெர்க்குரி, கார்பாக்சிபெப்டிடேசு
திண்மநிலைச் சேர்மங்கள்[தொகு]
முக்கியமான இப்பிரிவில் கட்டமைப்பு [7], பிணைப்பு, பொருட்களின் இயற்பியல் பண்புகள், போன்றவற்றின் மீது கவனம் செலுத்தப்படுகிறது. திண்மங்களுடைய துணை அலகுகளுக்கிடையில் நிகழும் வேதியியல் இடைவினைகளைப் புரிந்து கொள்வதற்காக நடைமுறையில், படிகவரைவியல் திட நிலை கனிம வேதியியல் போன்ற பிரிவுகள் பயன்படுத்திக் கொள்ளப்படுகின்றன. உலோகங்களும் அவற்றின் உலோகக் கலவைகளும் திண்மநிலை வேதியியலில் இடம்பெறுகின்றன. சுருங்கிய பொருளியற்பியல், கனிமவியல் மற்றும் பொருளறிவியல் முதலானவை உயிர்கனிம வேதியியலுடன் தொடர்புள்ள பிற துறைகளாகும்.
- உதாரணங்கள்:சிலிக்கன் சிப்புகள், சியோலைட்டுகள், YBa2Cu3O7
கோட்பாட்டு கனிம வேதியியல்[தொகு]
கனிம வேதியியல் பிரிவில் ஒரு மாற்று கண்ணோட்டம் அணுவின் போர் மாதிரிக்குப் பின் தொடங்கியது. கோட்பாட்டு வேதியியலின் கருவிகள் மற்றும் மாதிரிகளையும், கணக்கீட்டு வேதியியலையும் பயன்படுத்தி. மூலக்கூறுகளின் எளிய பிணைப்புகள் மற்றும் சிக்கலான பிணைப்புகள் குறித்த இக்கண்ணோட்டம் விரிவடைந்தது. பன்னிலை எலக்ட்ரான்களுக்கான துல்லியமான குவாண்டம் பொறிமுறை விளக்கங்கள் கனிம வேதியியலில் கடினமாகும். இந்தச் சவாலின் காரணமாக மூலக்கூறு சுற்றுப்பாதை கோட்பாடு மற்றும் ஈனி புலக்கோட்பாடு உட்பட பல அரை அளவியல் அல்லது அரை அனுபவ அணுகுமுறைகள் தோன்றின. இவற்றிற்கு இணையாக மறுபக்கம் அடர்த்தி சார்புக் கோட்பாடு உள்ளிட்ட தோராய கணக்கீட்டு முறைகளும் ஆராயப்பட்டன.
கோட்பாடுகளைத் தவிர்த்து இத்துறையின் வளர்ச்சிக்கு தரம் மற்றும் அளவு மிகவும் முக்கியமாகும். எடுத்துக்காட்டாக அறை வெப்பநிலையில் CuII2(OAc)4(H2O)2 கிட்டத்தட்ட எதிர்காந்தமாகும். ஆனால் மூலக்கூறில் இரண்டு இணையில்லா எலக்ட்ரான்கள் உள்ளதாக படிகப் புலக்கோட்பாடு தெரிவிக்கிறது. இணைகாந்தம், எதிர்காந்தம் இரண்டிற்குமிடையிலான பொருத்தமின்மை காரணமாக காந்தப் பிணைப்பு மாதிரிகள் வளர்ச்சியடைந்தன. இவ்வளர்ச்சியின் விளைவாக புதிய காந்தப் பொருட்களும் புதிய தொழில்நுட்பங்களும் வளர்ச்சியடைந்தன.
தரக் கோட்பாடுகள்[தொகு]
தரக் கோட்பாட்டு விளைவுகளால் கனிம வேதியியல் பெரும் பயனடைந்துள்ளது. இத்தகைய தரக் கோட்பாடுகளை எளிதாக கற்றுக் கொள்ள குவாண்டம் கோட்பாடு குறித்த சிறிய பின்னணி இருந்தால் போதுமானதாகும். முதன்மைக்குழு சேர்மங்களுக்குள் இவற்றின் கட்டமைப்பைப்பற்றி வலுவளவு ஓட்டு இலத்திரன் சோடிகளின் தள்ளுகைக் கொள்கை வலிமையாக எடுத்துரைக்கிறது. NH3 இன் பட்டைக்கூம்பு கட்டமைப்பிற்கும் ClF3 இன் T- வடிவக் கட்டமைப்பிற்குமான விளக்கத்தை இக்கொள்கை அளித்தது. இடைநிலை உலோகங்கள் உருவாக்கும் எளிய அணைவுச் சேர்மங்களின் காந்தத்தன்மையைப் புரிந்துகொள்ள படிகப்புலக் கோட்பாடு உதவுகிறது. [FeIII(CN)6]3− இல் ஒரேயொரு இணையில்லா எலக்ட்ரானும் [FeIII(H2O)6]3+ இல் ஐந்து இணையில்லா எலக்ட்ரான்களும் இருப்பதற்கான காரணத்தை படிகப்புலக் கோட்பாடு விளக்கியது. கட்டமைப்பு மற்றும் வினைத்திறனை மதிப்பீடு செய்வதற்கு, மூலக்கூறுகளின் மைய அணுவிலுள்ள எலக்ட்ரான்களின் எண்ணிக்கை, இணைதிறன் எலக்ட்ரான்களின் எண்ணிக்கையில் மூலக்கூறுகளை வகைப்படுத்த கவனம் செலுத்தும் முறை, குறிப்பாக சக்திவாய்ந்த பண்புசார் அணுகுமுறை தொடக்கம் கண்டது.
மூலக்கூற்றுச் சமச்சீர்மையும் குலக் கோட்பாடும்[தொகு]
கனிம வேதியியலில் மூலக்கூறு சமச்சீர்மைக் கோட்பாடு ஒரு மையக் கட்டமைப்பாக உள்ளது [8] இடக்குழு சமச்சீர்மையின் அடிப்படையில் மூலக்கூறுகளின் வடிவங்களைப் பற்றி கணிதவியலின் குலக் கோட்பாடு விவரிக்கிறது. குழு கோட்பாடு காரணமாகிறது மேலும், தத்துவார்த்த கணக்கீடுகள் மற்றும் காரணங்களைக் கண்டறிதல், தெளிவுபடுத்தல் போன்றவற்றை செயல்படுத்தவும் குலக் கோட்பாடு உதவுகிறது.
அதிர்வு அல்லது மின்னணுக்களின் சமச்சீர் பண்புகளைப் பொறுத்து நிறமாலையியல் அம்சங்கள் ஆராயப்பட்டு விவரிக்கப்பட்டுள்ளன.
அதிர்வு மற்றும் மின்னணு நிறமாலையின் எண்களையும் ஈர்ப்பையும் முன்கணித்துச் சொல்லும் வாய்ப்பை, சமச்சீர்மையின் சாதாரணநிலை, மற்றும் கிளர்வுநிலைப் பண்புகள் தொடர்பான அறிவு அளிக்கிறது. பதிலீட்டு உலோகக் கார்பனையில் அணைவுச் சேர்மங்களில் உள்ள C-O அதிர்வுகளின் எண்ணிக்கையை முன்கணித்தல் குலக் கோட்பாட்டின் உன்னதமான பயனாகும்.
வெப்ப இயக்கவிலும் கனிம வேதியியலும்[தொகு]
வேதி வினைகளுக்கும் ஆற்றலுக்குமிடையான தொடர்புகளில் கவனம் செலுத்துவது கனிம வேதியியலின் அளவறி ஆய்வின் மற்றொரு அணுகுமுறையாகும். இந்த அணுகுமுறை முற்றிலும் பாரம்பரிய, அனுபவ அணுகுமுறையாக இருந்தாலும் ஒரு பயனுள்ள முறையாகவே உள்ளது. ஆக்சிசனேற்ற ஒடுக்க செயல்திறன், அமிலத்தன்மை, நிலை மாற்றங்கள் போன்ற விரிவான கோட்பாடுகள் வெப்ப இயக்கவியலில் இடம்பெற்றுள்ளன. நேரடியாக உணர முடியாத எலக்ட்ரான் நாட்டம் போன்ற சில தொடக்க செயல்முறைகளின் ஆற்றலை மதிப்பிடப் பயன்படுத்தப்படும் பார்ன் – ஏபர் சுழற்சிமுறை கனிம வேதியியல் வெப்ப இயக்கவியலின் சிறப்புவாய்ந்த ஒரு கோட்பாடு ஆகும்.
வழிமுறைக் கனிம வேதியியல்[தொகு]
வேதி வினைகளின் வினை வழிமுறையில் கவனம் செலுத்தும் போக்கு தற்பொழுது பிரபலமடைந்து வரும் முக்கியமான மற்றும் வளர்ந்து வரும் அம்சமாகும். வினைகளின் ஈடுபடும் வெவ்வேறு வகையான சேர்மங்களின் வினைவழிமுறைகள் விரிவாக ஆராயப்படுகின்றன.
முதன்மைக் குழு தனிமங்களும் இலந்தனைடுகளும்[தொகு]

, S4N4 ஒரு பிரதானக் குழுத் தனிமம்]]
முதன்மைக்குழுத் தனிமங்களில் 13-18 குழுவைச் சேர்ந்த சேர்மங்களின் வினை வழிமுறைகள் கரிம வேதியியலில் விவாதிக்கப்படுகின்றன.
C, N, O மற்றும் F தனிமங்களைவிட கனமான தனிமங்கள் பெரும்பாலும் எண்ம விதியில் முன் கணிக்கப்பட்ட எலக்ட்ரான்களைக் காட்டிலும் அதிக எலக்ட்ரான்களுடன் சேர்ந்து சேர்மங்களாக உருவாகின்றன. மீ இணைதிறன் மூலக்கூறுகள் என்ற பெயரில் வெளியிடப்பட்ட ஒரு கட்டுரையில் இதற்கான விளக்கம் கொடுக்கப்பட்டுள்ளது. இச்சேர்மங்களுடைய வேதிவினைகளின் வினை வழிமுறைகள் கரிமச் சேர்மங்களின் வினைவழிமுறையிலிருந்து வேறுபடுகின்றன. கார்பனைவிட இலேசான தனிமங்களும் (B, Be, Li) அலுமினியம் மற்றும் மக்னீசியம் தனிமங்களும் பெரும்பாலும் எலக்ட்ரான் பற்றாக்குறை கட்டமைப்புகளாக கார்போ நேரயனிகளை ஒத்த அமைப்புடன் உருவாகின்றன. இத்தகைய எலக்ட்ரான்-குறைபாடுள்ள இனங்கள் துணைப் பாதைகள் வழியாக வினைபுரிய முனைகின்றன. இலாந்தனைடுகளின் வேதியியல் அலுமினிய வேதியலுடன் பல அம்சங்களில் ஒன்றுபடுகிறது.
இடைநிலை உலோக அணைவுகள்[தொகு]
இடைநிலை உலோகங்களின் வினைவழி முறைகள் முதன்மைக்குழு உலோகங்களின் வினைவழி முறைகளிலிருந்து வேறுபடுத்தப்பட்டு தனியாக விவாதிக்கப்படுகின்றன[9]. பிணைப்பில் ஈடுபடும் டி ஆர்பிட்டால்களின் வினைவழிமுறைப் பாதைகளில் கடுமையாக ஆதிக்கம் செலுத்துகிறது. ஈனிகளின் பதிலீடு மற்றும் பிரிகைகளும் வழிப்பாதை மற்றும் வீதங்கள் போன்ற நடைமுறைகளிலும் அணைவுக்கூட்டு மற்றும் அணைவுப் பிரிகை செயல்பாடுகளிலும் இவ்வாதிக்கம் நிகழ்கிறது.
அணைவுச்சேர்மங்களின் இயக்க நிலைமாற்றமே இத்தகைய இடைநிலை உலோக வேதியியலின் பூரணத்துவமான அம்சம் ஆகும். முன்னோடி அணைவுச்சேர்மங்களில் [M(H2O)6]n+: தனி மற்றும் பிணைக்கப்பட்ட தண்ணீர் பரிமாற்றத்தின் மூலம் இது விளக்கப்பட்டுள்ளது.
[M(H2O)6]n+ + 6 H2O* → [M(H2O*)6]n+ + 6 H2O
இங்கு H2O* உதாரணமாக H217O ஆகக் கருதப்படுகிறது.
தண்ணீர் பரிமாற்றத்தின் வீதம் தனிமவரிசை அட்டவணை முழுவதும் மாறுபடுகிறது. இலந்தனைடு அணைவுச்சேர்மங்கள் உயர் எல்லையையும் இரும்பு (III) இனங்கள் குறைவான எல்லையையும் கொண்டுள்ளன.
இடைநிலை உலோகங்களில் ஏற்ற-ஒடுக்க வினைகள் பரவலாகக் காணப்படுகிறது. இரண்டு வகையான ஏற்ற-ஒடுக்க வினைகள் இங்கு முக்கியத்துவம் பெறுகின்றன. ஆக்சிசனேற்ற கூட்டுவினைகள்/குறைத்து நீக்கல் வினைகள் போன்ற அணு மாற்ற வினைகள் ஒரு வகையாகும். எலக்ட்ரான் மாற்ற வினைகள் மற்றொரு வகை வினைகளாகும். அடிப்படை ஏற்ற ஒடுக்க வினை என்பது தன் பரிமாற்ற வினையில் தொடங்குகிறது. ஆக்சிசனேற்றி ஒன்றும் ஒடுக்கியொன்றும் வினையில் ஈடுபட்டு வலுவிழக்கின்ற வினையை கருதலாம். உதாரணமாக, பெர்மாங்கனேட்டும் ஒரு எலக்ட்ரான் குறைந்த மாங்கனேட்டும் வினையில் ஒரு எலக்ட்ரானை பரிமாறிக் கொள்கின்றன.
[MnO4]− + [Mn*O4]2− → [MnO4]2− + [Mn*O4]−
ஈனி தொகுதிகளில் வினைகள்[தொகு]
ஒருங்கிணைந்த ஈனிகளின் வினைகள் தனிநிலை ஈனிகளின் வினையிலிருந்து வேறுபடுகின்றன. உதாரணமாக [Co(NH3)6]3+ வில் அமோனியா ஈனிகளின் அமிலத்தன்மை NH3 உடன் ஒப்பிடுகையில் அதிகமாகும். உலோக நேர்மின் அயனிகளுடன் பிணைக்கப்பட்ட ஆல்க்கீன்கள் மின்னணு மிகு பொருட்களுடன் தீவிரமாக வினையில் ஈடுபடுகின்றன. ஆனால், பொதுவாக ஆல்க்கீன்கள் அவ்வாறு ஈடுபடுவதில்லை. பெரிய மற்றும் தொழிற்துறை ரீதியாக முக்கியமானதாகக் கருதப்படும் வினையூக்கி, உலோகங்களுடன் பிணைதல் மூலம் கரிம அணுக்கூறுகளின் வினைத்திறனை மாற்றுகிறது. ஒருபடித்தான வினையூக்கம் கரைசல்களிலும், பலபடித்தான வினையூக்கம் வளிமங்கள் அல்லது கரைந்த தளப்பொருட்களிலும் தோன்றுகிறது. பாரம்பரியமாக ஒருபடித்தான வினையூக்கம் கரிம உலோக வேதியியலிலும், பலபடித்தான வினையூக்கம் மேற்பரப்பு வேதியலிலும் ஆராயப்படுகின்றன. ஆனால் இரண்டின் அடிப்படைக் கனிம வேதியியல் பண்புகளும் ஒன்றாகும். இடைநிலை உலோகங்கள் தனித்துவத்துடன் CO, H2, O2, மற்றும் C2H4 சிறிய மூலக்கூறுகளுடன் வினைபுரிகின்றன.
கனிமச் சேர்மங்களின் சிறப்பியல்பாக்கம்[தொகு]
கனிம வேதியியலில் பல்வேறு வகையான தனிமங்கள் காணப்படுவதால், இவற்றிலிருந்து உருவாகும் பலவகை வழிப்பொருட்களும் பலவிதமான பண்புகளை வெளிப்படுத்துகின்றன. இதனால் கனிம வேதியியலும் பல்வேறு வகையான பகுப்பாய்வு முறைகளுடன் தொடர்பு கொள்ள வேண்டியதாகிறது. பழைய பகுப்பு முறைகள் கரைசல்களின் மின்கடத்துப் பண்பு, உருகுநிலை, கரைதிறன், அமிலத்தன்மை போன்ற ஒட்டுமொத்த பண்புகளை ஆய்வு செய்தன. குவாண்டம் கோட்பாடு போன்ற நவீன வளர்ச்சிகளின் விளைவாக புதிய கருவிகள் தோற்றுவிக்கப்பட்டு கனிம மூலக்கூறுகள் மற்றும் திண்மங்களின் மின்வேதியியல் பண்பு குறித்த ஆய்வுகள் வளர்ந்தன. கருத்தியல் கோட்பாடுகளின் உள்ளார்ந்த புரிதலை அதிகரிக்க நவீன அளவீடுகள் உதவின. உதாரணமாக, இரு மைய பிணைப்பை மீத்தேனின் ஒளி எலக்ட்ரான நிறமாலை விளக்கியது. கார்பனுக்கும் ஐதரசனுக்கும் இடையில் கணிக்கப்பட்ட இரண்டு எலக்ட்ரான் பிணைப்புகளை விளக்க இணைதிறன் பிணைப்புக் கோட்பாட்ட்டல் இயலவில்லை. இதனால் மூலக்கூற்று ஆர்பிட்டல் கோட்பாடு வளர்ச்சியடைந்தது. பொதுவான சில கனிமவேதியியல் தொழில்நுட்பங்கள்.
- எக்சு கதிர் படிகவியல்: மூலக்கூறுகளின் முப்பரிமாண அமைப்பை உறுதி செய்யும் தொழில் நுட்பம்.
- இரட்டை முனைவாக்க குறுக்கீட்டு ஒளி அளவியல்: மூலக்கூறுகளின் மேற்பரப்பு வடிவங்களை உறுதி செய்யும் தொழில் நுட்பம்.
- நிறமாலையியல் வடிவங்கள்:
- புற ஊதா-கட்புலண் நிறமாலையியல்: பல கனிமச் சேர்மங்கள் வண்ண மையமாக இருப்பதால் வரலாற்று முக்கியத்துவம் மிக்க ஒரு தொழில் நுட்பம்.
- அணுக்கரு காந்த ஒத்ததிர்வு நிறமாலையியல்: 11B, 19F, 31P, மற்றும் 195Pt போன்ற காந்த ஒத்ததிர்வு அணுக்கள் முக்கியத்துவமான சேர்மங்களின் பண்புகள் மற்றும் கட்டமைப்பை விளக்குகின்றன.
- அகச்சிவப்பு நிறமாலையியல்: கார்பனைல் ஈனிகளின் ஈர்ப்பு தொடர்பான ஆய்வுகளுக்கு உதவுகிறது.
- அணுக்கரு எலக்ட்ரான் இரட்டை ஒத்ததிர்வு: இணைகாந்த இனங்களின் மூலக்கூற்று அமைப்பையும் மின்னணு அமைப்பையும் ஆய்வு செய்கின்ற காந்த ஒத்ததிர்வு முறை.
- மாசுபவர் நிறமாலையியல்: மாசுபவர் விளைவின் அடிப்படையில் இயங்கும் ஒரு தொழில்நுட்பம்.
- இணைகாந்த எலக்ட்ரான் சுழற்சி: இணைசேரா எலக்ட்ரான்களை ஆய்வு செய்கின்ற நுட்பம்.
- மின்வேதியியல்: மின்பகுப்பு, மின்கலம் ஆகிவற்றுக்கு அடிப்படையான வேதிவினைகளை மின்வேதியியல் ஆய்கின்றது.
செயற்கை கனிம வேதியியல்[தொகு]
இயற்கையில் தூய்மையான நிலையில் கனிமவேதியியல் பொருட்கள் கிடைத்தாலும் பெரும்பாலான கனிம வேதியியல் பொருட்கள் செயற்கை முறைகளில் வேதித் தொழிற்சாலைகளில் தயாரிக்கப்படுகின்றன. வினையின் ஈடுபடும் வேதிப்பொருட்களின் ஆவியாகும் தன்மை அல்லது கரைதிறன் அடிப்படையில் இச்செயற்கை முறைகள் வகைப்படுத்தப்படுகின்றன[10]. கரையக்கூடிய கனிமச் சேர்மங்கள் கரிமத் தொகுப்பு வினைகளின் மூலமாகத் தயாரிக்கப்படுகின்றன. காற்றுடன் வினைபுரியக்கூடிய உலோகங்களைக் கொண்ட சேர்மங்கள் சிலெங்கு வரிசை அல்லது ஒளிர் பெட்டி முறைகளில் தயாரிக்கப்படுகின்றன. இவ்வாறாக, வினைபடு பொருட்களின் தன்மைக்கு ஏற்ப செயற்கைத் தயாரிப்பு முறைகளும் மாறுபடுகின்றன.
மேற்கோள்கள்[தொகு]
- ↑ "Careers in Chemistry: Inorganic Chemistry". American Chemical Society.
- ↑ "Facts & Figures Of The Chemical Industry” Chemical and Engineering News, July 10, 2006.
- ↑ Lehn, J. M. (1995). Supramolecular Chemistry: Concepts and Perspectives. Weinheim: VCH. பன்னாட்டுத் தரப்புத்தக எண்:3-527-29311-6.
- ↑ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ). Butterworth–Heinemann. பன்னாட்டுத் தரப்புத்தக எண்:0080379419.
- ↑ Elschenbroich, C.; Salzer, A. (1992). Organometallics: A Concise Introduction (2nd ). Weinheim: Wiley-VCH. பன்னாட்டுத் தரப்புத்தக எண்:3527281649.
- ↑ S. J. Lippard; J. M. Berg (1994). Principles of Bioinorganic Chemistry. Mill Valley, CA: University Science Books. பன்னாட்டுத் தரப்புத்தக எண்:0-935702-73-3. https://archive.org/details/ost-chemistry-bioinch.
- ↑ Wells, A.F. (1984). Structural Inorganic Chemistry. Oxford: Clarendon Press. https://archive.org/details/structuralinorga0000well_m8i1.
- ↑ Cotton, F. A. (1990). Chemical Applications of Group Theory (3rd ). New York: John Wiley & Sons. பன்னாட்டுத் தரப்புத்தக எண்:978-0471510949. https://archive.org/details/isbn_9780471510949.
- ↑ R. G. Wilkins (1991). Kinetics and Mechanism of Reactions of Transition Metal Complexes (2nd ). Wiley-VCH. பன்னாட்டுத் தரப்புத்தக எண்:3-527-28389-7.
- ↑ Girolami, G. S.; Rauchfuss, T. B.; Angelici, R. J. (1999). Synthesis and Technique in Inorganic Chemistry (3rd ). Mill Valley, CA: University Science Books. பன்னாட்டுத் தரப்புத்தக எண்:978-0935702484. https://archive.org/details/synthesistechniq0000giro.
