தயோபாசுபேட்டு
தயோபாசுபேட்டுகள் (Thiophosphates) என்பவை PS
4−xO3−
x (x = 0, 1, 2, அல்லது 3) என்ற பொது மூலக்கூற்று வாய்ப்பாட்டால் விவரிக்கப்படும் வேதியியல் சேர்மங்களும் எதிர்மின் அயனிகளுமாகும். தொடர்புடைய வழிப்பொருட்களில் கரிமக்குழுக்கள் ஒன்று அல்லது பல O அல்லது S உடன் இணைக்கப்பட்டிருக்கும். பாசுபோரோதயோயேட்டுகள் என்ற பெயராலும் இவற்றை அழைக்கலாம். தயோபாசுபேட்டுகளின் கட்டமைப்பில் பாசுபரசு(V) நான்முகி மையங்கள் இடம்பெற்றுள்ளன[1].
கரிமதயோபாசுபேட்டுகள்[தொகு]
கரிமபாசுபரசு வகை சேர்மங்களின் ஒரு துணைப்பிரிவாக கரிமதயோபாசுபேட்டுகள் வகைப்படுத்தப்படுகின்றன. இவை கனிமதயோபாசுபேட்டுகளின் கட்டமைப்புடன் தொடர்பு கொண்டவையாக உள்ளன. இவற்றின் பொதுவான கரிமதயோபாசுபேட்டுகளின் பொதுவாய்ப்பாடு (RO)3−xRxPS ஆகும். தொடர்புடைய இதர சேர்மங்களில் வாய்ப்பாட்டிலுள்ள RO ஆனது RS ஆல் இடப்பெயர்ச்சி செய்யப்படுகிறது. பலதயோபாசுபேட்டுகள் பூச்சிக்கொல்லிகள் தயாரிப்புக்கு பயன்படுத்தப்படுகின்றன. சில தயோபாசுபேட்டுகள் மருத்துவத்திலும், சில எண்ணெய்களில் கூட்டுசேர் பொருளாகவும் பயன்படுகின்றன [1]
-
துத்தநாக டையால்கைல்டைதயோபாசுபேட்டு, ஓர் எண்ணெய் கூட்டுசேர் பொருள்.[2]
-
பாசுபோரோதயோயேட்டுகள், மருத்துவ சிகிச்சை.
-
அமிபோசிடைன், புற்றுநோய் சிகிச்சை.
-
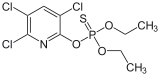
குளோர்பைரிபோசு, ஒரு பிரபல பூச்சிக்கொல்லி .
-
மாலாதயோன்]], ஒரு பிரபல பூச்சிக்கொல்லி
.
ஓலிகோநியூக்ளியோடைடு பாசுபோரோதயோயேட்டுகள் என்பவை ஓலிகோநியூக்ளியோடைடுகளின் திருத்தப்பட்ட வகை சேர்மங்களாகும். இவற்றின் பாசுபரசு மையத்திலுள்ள ஆக்சிசன் அணுக்களில் ஒன்று கந்தகத்தால் இடப் பெயர்ச்சி செய்யப்பட்டிருக்கும். மரபுபிழை சிகிச்சைகளுக்கு இவையே அடிப்படையாகும். பாமிவிர்சென் (விட்ராவென்), ஆப்லிமெர்சென், அலிகாபோர்சென், மிபோமெர்சென் (கைனாம்ரோ) போன்ற மருந்துகள் இதற்கு உதாரணங்களாகும் [3].
கனிமதயோபாசுபேட்டுகள்[தொகு]
எளிய தயோபாசுபேட்டுகள் [PS4−xOx]3−என்ற வாய்ப்பாட்டைக் கொண்டுள்ளன. இந்த மூவெதிர்மின் அயனிகளை உயர் pH அமிலக்கார அளவுகளில் மட்டுமே அறியப்படுகின்றன. இல்லையெனில் இவை புரோட்டானேற்ற வடிவில் [HnPS4−xOx](3−n)−என்ற அயனிகளாகக் காணப்படுகின்றன.
மோனோதயோபாசுபேட்டுகள்[தொகு]

மோனோதயோபாசுபேட்டு என்பது [PO3S]3− என்ற ஒரு எதிர்மின் அயனியாகும். இது C3v சீர்மையைக் கொண்டுள்ளது. சோடியம் மோனோதயோபாசுபேட்டு (Na3PO3S) உப்பு பொதுவாகக் காணப்படும் ஓர் உப்பாகும். உயிர்வேதியியலில் பாசுபேட்டை ஒத்த ஓர் சேர்ம்மாக ஆராய்ச்சியில் மோனோதயோபாசுபேட்டு பயன்படுத்தப்படுகிறது. மோனோதயோபாசுபேட்டு எசுத்தர்கள் உயிர்வேதியியல் வினைப்பொருளாக படியெடுத்தல் ஆய்வுகளில் பயன்படுத்தப்படுகின்றன [4], பதிலீட்டு குறுக்கீடு மதிப்பீடுகள் சிலசமயங்களில் மோனோதயோபாசுபேட்டுகளை CH3O)2POS− போன்ற எசுத்தர்கள் எனக்குறிப்பிடுகின்றன [5].
டைதயோபாசுபேட்டுகள்[தொகு]
டைதயோபாசுபேட்டுகள் [PO2S2]3− என்ற மூலக்கூற்று வாய்ப்பாட்டால் குறிக்கப்படுகின்றன. இவை C2v சீர்மையைக் கொண்டுள்ளன. சோடியம் டைதயோபாசுபேட்டு உப்பு பொதுவாகக் காணப்படும் ஓர் உப்பாகும். இது நிறமற்ற உப்பாகும். பாசுபரசு பெண்டாசல்பைடும் சோடியம் ஐதராக்சைடும் வினைபுரிவதால் இச்சேர்மம் உண்டாகிறது:[6]
- P2S5 + 6 NaOH → 2 Na3PO2S2 + H2S + 2 H2O
பேரியம்டைதயோபாசுப்பேட்டுடன் கந்தக அமிலத்தைச் சேர்த்து சூடுபடுத்தினால் டைதயோபாசுபாரிக் அமிலம் உருவாகிறது.
- Ba3(PO2S2)2 + 3 H2SO4 → 3 BaSO4 + 2 H3PO2S2
இரண்டு Na3PO2S2 மற்றும் குறிப்பாக H3PO2S2 சேர்மங்களும் நீராற்பகுத்தலால் பாதிக்கப்பட்டு அவற்றின் மோனோதயோ வழிப்பொருள்களாக மாறுகின்றன.
டிரை மற்றும் டெட்ராதயோபாசுபேட்டுகள்[தொகு]
டிரைதயோபாசுபேட்டு என்பது [POS3]3−, என்ற ஒரு எதிர்மின் அயனியாகும். இது C3v symmetry சீர்மையைக் கொண்டுள்ளது. டெட்ராதயோபாசுபேட்டு [PS4]3− என்ற எதிர்மின் அயனியாகும். இது Td சீர்மையில் உள்ளது.
PxSy: இருபடி தயோபாசுபேட்டுகளும் பாலிதயோபாசுபேட்டுகளும்[தொகு]
எண்ணற்ற இருபடி தயோபாசுபேட்டுகளும் பாலிதயோபாசுபேட்டுகளும் அறியப்படுகின்றன. இந்த எதிர்மின் அயனிகளைக் கொண்டுள்ள சேர்மங்கள் திண்மநிலை மின்கலன்களில் இவற்றின் வேகமான அயனிக்கடத்தல் பண்பிற்காகப் பயன்படுத்தப்படுகின்றன. இருபடிதயோபாசுபேட்டுகள் P-O ஒத்த எதிர்மின் அயனிகளைப் போல விரிவான பன்முகத்தன்மையை பெற்றிருக்கவில்லை. ஆனால் கட்டமைப்பில் இவை ஒத்துள்ளன. உதாரணமாக P என்பது 4 ஒருங்கிணைவுகளைக் கொண்டுள்ளது. P−S−P இணைப்புகள் மற்றும் P−P பிணைப்புகள் உருவாகின்றன. ஒரே வித்தியாசம் என்னவெனில் அயனிகளில் இரண்டு அல்லது அதற்கு மேற்பட்ட கந்தக அணுக்கலைக் கொண்ட பாலிசல்பைடு கூறுகள் இருக்கும். ஆனால் P−O எதிர்மின் அயனிகளில் வினைத்திறன் மிக்க −O−O−, பெராக்சோ, அலகு மட்டும் இருக்கும்.
- PS−
3 அயனி நைட்ரேட்டு அயனியை ஒத்தது ஆகும், NO−
3. (PO−
3 ஒத்த அயனி ஏதுமில்லை); டெட்ராபீனைலார்சோனியம் உப்பாக தனித்துப் பிரிக்கப்பட்டுள்ளது.[7] - PS3−
4 அயனி PO3−
4 இன் கந்தகம் ஒத்த அயனி மற்றும் PO3−
4 போன்றது, நான்முகி. - P
2S4−
7 என்பது பைரோதயோபாசுபேட்டு அயனியாகும். இதில் இரண்டு மூலைகளும் PS4 நான்முகிகளை பகிர்கின்றன. பைரோபாசுபேட்டை இவை ஒத்தவையாகும்.[8] - P
2S4−
10 அயனியை இரண்டு PS4 நான்முகிகள் ஒரு டைசல்பைடு இணைப்பு அல்லது ஒரு பைரோதயோபாசுபேட்டு இணைப்பால் இணைக்கப்பட்டது போல காணமுடியும். −S− பாலமானது −S4− பாலத்தால் இடப்பெயர்ச்சி செய்யப்பட்டிருக்கும்.[9] - P
2S2−
6 அயனி இரண்டு நான்முகிகள் ஒரு முனையை பகிர்ந்து கொள்ளும் கட்டமைப்பால் ஆக்கப்பட்டுள்ளது. எனவே இந்தக் கட்டமைப்பு ஐசோஎலக்ட்ரானிக் அலுமினியம் குளோரைடு (Al2Cl6) இருமத்தை ஒத்திருக்கிறது. மாறாக ஆக்சிசன் ஒத்த டைமெட்டாபாசுபேட்டு P
2O2−
6 அயனி எதுவும் அறியப்படவில்லை. மெட்டாபாசுபேட்டுகள் சங்கிலி அல்லது வளையங்களால் ஆன பல்லுருவ கட்டமைப்பில் உள்ளன.[8] - P
2S2−
8 மற்றும் P
2S2−
10 இரண்டும் P
2S2−
6 அயனியுடன் தொடர்பு கொண்டுள்ளன. ஆனால் அவற்றின் இரண்டு −S− பாலங்களும் −S−S− ஆல் P
2S2−
8 அயனியிலும் −S−S−S− ஆல் P
2S2−
10 அயனியிலும் இடப்பெயர்ச்சி செய்யப்பட்டுள்ளன.[10] - P2S4−
6 அயனி நீர்-நிலைப்புத்தன்மை உள்ள உப்புகளாக உருவாகிறது.[11] இந்த எதிர்மின் அயனி ஈத்தேன்- போன்ற கட்டமைப்பில் உள்ளது. இது P−P பிணைப்பால் ஆக்கப்பட்டுள்ளது. இதனுடைய முறையான ஆக்சிசனேற்ற நிலை +4 ஆகும். ஐப்போடைபாசுபேட்டு அயனியும் ஐப்போபாசுபாரிக் அமிலமும் ஆக்சிசன் ஒத்த சேர்மங்களாகும். *P
3S3−
9 அயனி ஆறு உறுப்பு P3S3 வலையத்தைக் கொண்டுள்ளது. திரவ அமோனியாவில் P4S10 வினைபுரிந்து அமோனியா உப்பை உருவாக்குகிறது.[12] PS3+ உச்சி நீக்கப்பட்ட P4S10 அடமண்டேன் கட்டமைப்பு கொண்டதாகவும் இதைக் காண முடியும். - P
4S4−
8 அயனி ஒரு சதுர P4 வளையத்தைக் கொண்டுள்ளது,[7] P
5S5−
10 அயனி ஒரு P5 வளையத்தைக் கொண்டுள்ளது. மற்றும் P
6S6−
12 அயனி ஒரு P6 வளையத்தையும் கொண்டுள்ளது.[10]. இந்த (PS−
2)
n வளைய எதிர்மின் அயனிகள் +3 ஆக்சிசனேற்ற நிலையிலுள்ள பாசுபரசுசை கொண்டுள்ளன. ஆர்சனைட்டுகளில் ஆர்சனிக்(III) அயனியைப் போல இவை முக்கோணங்களல்ல என்பது குறிப்பிடத்தக்கது. ஆனால் இது இரண்டு பிணைப்புகள் மற்ற பாசுபரசு அணுக்களுக்கும், இரண்டு பிணைப்புகள் கந்தக அணுக்களுக்கும் பிணைந்துள்ள ஒரு நான்முகியாகும். P
6S6−
12 எதிர்மின் அயனியானது P
6O6−
12 வளைய எதிர்மின் அயனியை ஒத்த்தாகும்.[13] - P
4S2−
2 என்பது பொதுவாக ஒரு வண்ணத்துப்பூச்சி வடிவ அயனியாகும். SP(P2)PS. இரண்டு P−S பிணைப்புகள் ஒரு P−P பிணைப்பால் இடப்பெயர்ச்சி செய்யப்பட்ட P4 மூலக்கூறாகக் காணமுடியும்.[14] - P
7S3−
3 என்பது சல்பிடோ எப்டாபாசுபேட்டு தொகுதி அயனியாகும்.[7]
மேற்கோள்கள்[தொகு]
- ↑ 1.0 1.1 J. Svara, N. Weferling, T. Hofmann "Phosphorus Compounds, Organic" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2006. எஆசு:10.1002/14356007.a19_545.pub2
- ↑ H. Spikes "The history and mechanisms of ZDDP" Tribology Letters, Vol. 17, No. 3, October 2004. எஆசு:10.1023/B:TRIL.0000044495.26882.b5.
- ↑ Kurreck, J., "Antisense technologies. Improvement through novel chemical modifications", European Journal of Biochemistry 2003, 270, 1628-1644.எஆசு:10.1046/j.1432-1033.2003.03555.x
- ↑ Lorsch JR; Bartel DP; Szostak JW (1995). "Reverse transcriptase reads through a 2′–5′ linkage and a 2′-thiphosphate in a template". Nucleic Acids Res. 23 (15): 2811–2814. doi:10.1093/nar/23.15.2811. பப்மெட்:7544885. பப்மெட் சென்ட்ரல்:307115. http://nar.oxfordjournals.org/cgi/content/abstract/23/15/2811.
- ↑ "A thiophosphate bridged platinum–zinc hetero-bimetallic complex: [(Me2PhP)2Pt{OSP(OR)2}2ZnCl2". J. Chem. Soc., Chem. Commun.: 1036–1038. 1990. http://www.rsc.org/publishing/journals/article.asp?doi=C39900001036.
- ↑ R. Klement "Phosphorus" in Handbook of Preparative Inorganic Chemistry, 2nd Ed. Edited by G. Brauer, Academic Press, 1963, NY. Vol. 1., p. 571.
- ↑ 7.0 7.1 7.2 Greenwood, Norman N.; Earnshaw, Alan (1984). Chemistry of the Elements. Oxford: Pergamon Press. பக். 509–510. பன்னாட்டுத் தரப்புத்தக எண்:0-08-022057-6. http://books.google.co.nz/books?id=OezvAAAAMAAJ&q=0-08-022057-6&dq=0-08-022057-6&source=bl&ots=m4tIRxdwSk&sig=XQTTjw5EN9n5z62JB3d0vaUEn0Y&hl=en&sa=X&ei=UoAWUN7-EM6ziQfyxIDoCQ&ved=0CD8Q6AEwBA.
- ↑ 8.0 8.1 Phosphorus: Chemistry, Biochemistry and Technology, Sixth Edition, 2013, D.E.C. Corbridge, CRC Pres, Taylor Francis Group, ISBN 978-1-4398-4088-7
- ↑ Aitken, Jennifer A.; Canlas, Christian; Weliky, David P.; Kanatzidis, Mercouri G. (2001). "[P2S10]4−: A Novel Polythiophosphate Anion Containing a Tetrasulfide Fragment". Inorganic Chemistry 40 (25): 6496–6498. doi:10.1021/ic010664p. பன்னாட்டுத் தர தொடர் எண்:0020-1669.
- ↑ 10.0 10.1 Holleman, A. F.; Wiberg, E. (2001), Inorganic Chemistry, San Diego: Academic Press, pp. 734–735, ISBN 0-12-352651-5
- ↑ Gjikaj, Mimoza; Ehrhardt, Claus (2007). "New Hexachalcogeno–Hypodiphosphates of the Alkali Metals: Synthesis, Crystal Structure and Vibrational Spectra of the Hexathiodiphosphate(IV) Hydrates K4[P2S6]•4 H2O, Rb4[P2S6]•6 H2O, and Cs4[P2S6]•6 H2O". Zeitschrift für anorganische und allgemeine Chemie 633 (7): 1048–1054. doi:10.1002/zaac.200600339. பன்னாட்டுத் தர தொடர் எண்:0044-2313.
- ↑ Wolf, G.-U.; Meisel, M. (1982). "Beiträge zur Chemie von Phosphorverbindungen mit Adamantanstruktur. VII[1]. Über Darstellung und Eigenschaften von Nonathio-cyclotriphosphat". Zeitschrift für anorganische und allgemeine Chemie 494 (1): 49–54. doi:10.1002/zaac.19824940106. பன்னாட்டுத் தர தொடர் எண்:0044-2313.
- ↑ Ebert, M.; Nassler, J. (1989). "The Ring Acid, H6P6O12 and Ring Acid, H4P4O10 and Their Salts". Phosphorus, Sulfur, and Silicon and the Related Elements 41 (3–4): 462. doi:10.1080/10426508908039741. பன்னாட்டுத் தர தொடர் எண்:1042-6507.
- ↑ Rotter, Christiane; Schuster, Michael; Karaghiosoff, Konstantin (2009). "An Unusual Binary Phosphorus−Tellurium Anion and Its Seleno- and Thio- Analogues: P
4Ch2−
2 (Ch = S, Se, Te)". Inorganic Chemistry 48 (16): 7531–7533. doi:10.1021/ic901149m. பன்னாட்டுத் தர தொடர் எண்:0020-1669.

![துத்தநாக டையால்கைல்டைதயோபாசுபேட்டு, ஓர் எண்ணெய் கூட்டுசேர் பொருள்.[2]](http://upload.wikimedia.org/wikipedia/commons/thumb/7/7f/Zn%28dtp%292.png/160px-Zn%28dtp%292.png)


![மாலாதயோன்]], ஒரு பிரபல பூச்சிக்கொல்லி](http://upload.wikimedia.org/wikipedia/commons/thumb/0/0c/Malathion.png/160px-Malathion.png)