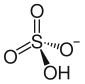
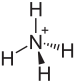அமோனியம் பைசல்பேட்டு
| |||

| |||

| |||
| பெயர்கள் | |||
|---|---|---|---|
| ஐயூபிஏசி பெயர்
அமோனியம் ஐதரசன் சல்பேட்டு
| |||
| இனங்காட்டிகள் | |||
| 7803-63-6 | |||
| ChemSpider | 23057 | ||
| யேமல் -3D படிமங்கள் | Image | ||
| பப்கெம் | 16211166 | ||
| வே.ந.வி.ப எண் | WS990000 | ||
SMILES
| |||
| பண்புகள் | |||
| (NH4)HSO4 | |||
| வாய்ப்பாட்டு எடை | 115.11 கி/மோல் | ||
| தோற்றம் | வெண்மையான திண்மம் | ||
| அடர்த்தி | 1.78 கி/செ.மீ3 | ||
| உருகுநிலை | 147 °C (297 °F; 420 K) | ||
| நன்றாகக் கரையும் | |||
| other solvents-இல் கரைதிறன் | மெத்தனாலில் கரையும் insoluble in அசிட்டோனில் கரையாது. | ||
| தீங்குகள் | |||
| பொருள் பாதுகாப்பு குறிப்பு தாள் | External MSDS | ||
| தொடர்புடைய சேர்மங்கள் | |||
| ஏனைய எதிர் மின்னயனிகள் | அமோனியம் தயோசல்பேட்டு அமோனியம் சல்பைட்டு அமோனியம் சல்பேட்டு அமோனியம் பெர்சல்பேட்டு | ||
| ஏனைய நேர் மின்அயனிகள் | சோடியம் பைசல்பேட்டு பொட்டாசியம் பைசல்பேட்டு | ||
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |||
| | |||
| Infobox references | |||
அமோனியம் பைசல்பேட்டு (Ammonium bisulphate) வெண்மையான (NH4)HSO4. என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட ஒரு கனிம வேதியியல் சேர்மமாகும். படிகத் திண்மமான இச்சேர்மம் அமோனியம் ஐதரசன் சல்பேட்டு என்ற பெயராலும் அழைக்கப்படுகிறது. கந்தக அமிலம், அமோனியாவால் பாதிநடுநிலையாக்கம் செய்யப்பட்டு அமோனியம் பைசல்பேட்டு விளைபொருளாக உருவாகிறது.
தயாரிப்பு[தொகு]
அசிட்டோன் சயனோவைதரின் பாதை வழியாக மெத்தில் மெத்தாகிரைலேட்டிலிருந்து பொதுவாக ஓர் உடன் விளைபொருளாக அமோனியம் பைசல்பேட்டு உருவாகிறது[1]
சல்பாமிக் அமிலத்தின் நீர்த்தக் கரைசலை நீராற்பகுப்பு வினைக்கு உட்படுத்தியும் அமோனியம் பைசல்பேட்டு தயாரிக்கலாம். இம்முறையில் மீத்தூய்மையான உப்பு கிடைக்கிறது.
H3NSO3 + H2O → [NH4]+[HSO4]−
மேலும், அமோனியம் சல்பேட்டை வெப்பச் சிதைவு செய்தும் அமோனியம் பைசல்பேட்டு தயாரிக்க முடியும்.
(NH4)2SO4 → (NH4)HSO4 + NH3
பயன்கள்[தொகு]
அமோனியம் பைசல்பேட்டுடன் மேலும் அமோனியாவைச் சேர்த்து நடுநிலையாக்கம் செய்வதால் அமோனியம் சல்பேட்டு என்ற பயனுள்ள உரம் கிடைக்கிறது. கந்தக அமிலத்திற்கு மாற்றாக சோடியம் பைசல்பேட்டு பொதுவாகப் பயன்படுத்தப்பட்டாலும், வலிமை குறைந்த மாற்றாக அமோனியம் பைசல்பேட்டு பயன்படுத்தப்படுகிறது.
மேற்கோள்கள்[தொகு]
- ↑ William Bauer, Jr. "Methacrylic Acid and Derivatives" in Ullmann's Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim. எஆசு:10.1002/14356007.a16_441.