அக்ரிலிக் அமிலம்
| |

| |
| பெயர்கள் | |
|---|---|
| ஐயூபிஏசி பெயர்
Prop-2-enoic acid
| |
| வேறு பெயர்கள்
அக்ரோலீயிக் அமிலம்
எத்திலீன்கார்பாக்சிலிக் அமிலம் புரொப்பீன் அமிலம் புரொப்பியானிக் அமிலம் வைனைல்பார்மிக் அமிலம் | |
| இனங்காட்டிகள் | |
| 79-10-7 | |
| ChEBI | CHEBI:18308 |
| ChEMBL | ChEMBL1213529 |
| ChemSpider | 6333 |
| DrugBank | DB02579 |
| EC number | 201-177-9 |
| யேமல் -3D படிமங்கள் | Image Image |
| KEGG | D03397 |
| பப்கெம் | 6581 |
| வே.ந.வி.ப எண் | AS4375000 |
SMILES
| |
| UNII | J94PBK7X8S |
| பண்புகள் | |
| C3H4O2 | |
| வாய்ப்பாட்டு எடை | 72.06 g·mol−1 |
| தோற்றம் | clear, நிறமற்ற நீர்மம் |
| மணம் | acrid[2] |
| அடர்த்தி | 1.051 g/mL |
| உருகுநிலை | 14 °C (57 °F; 287 K) |
| கொதிநிலை | 141 °C (286 °F; 414 K) |
| Miscible | |
| ஆவியமுக்கம் | 3 மி.மி.பாதரசம்[2] |
| காடித்தன்மை எண் (pKa) | 4.25[3] |
| பிசுக்குமை | 1.3 cP at 20 °C (68 °F) |
| தீங்குகள் | |
| முதன்மையான தீநிகழ்தகவுகள் | அரிக்கும் (C), சுற்றுச்சூழலுக்கு அபாயமானது (N) |
| பொருள் பாதுகாப்பு குறிப்பு தாள் | MSDS |
| R-சொற்றொடர்கள் | R10 R20/21/22 R35 R50 |
| S-சொற்றொடர்கள் | S26 S36/37/39 S45 S61 |
| தீப்பற்றும் வெப்பநிலை | 68 °C (154 °F; 341 K) |
Autoignition
temperature |
429 °C (804 °F; 702 K) |
| வெடிபொருள் வரம்புகள் | 2.4%-8.02%[2] |
| அமெரிக்க சுகாதார ஏற்பு வரம்புகள்: | |
அனுமதிக்கத்தக்க வரம்பு
|
none[2] |
பரிந்துரைக்கப்பட்ட வரம்பு
|
TWA 2 ppm (6 மி.கி/மீ3) [தோல்][2] |
உடனடி அபாயம்
|
N.D.[2] |
| தொடர்புடைய சேர்மங்கள் | |
| ஏனைய எதிர் மின்னயனிகள் | அக்ரிலேட்டு |
| கார்பாக்சிலிக் அமிலம் தொடர்புடையவை |
அசிட்டிக் அமிலம் புரொப்பியானிக் அமிலம் லாக்டிக் அமிலம் 3-ஐதராக்சிபுரொப்பியானிக் அமிலம் மலோனிக் அமிலம் பியூட்டரிக் அமிலம் குரோடோனிக் அமிலம் |
| தொடர்புடைய சேர்மங்கள் | அல்லைல் ஆல்ககால் புரொப்பியானால்டிகைடு அக்ரோலின் மெத்தில் அக்ரிலேட்டு |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
| | |
| Infobox references | |
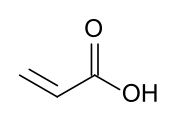
அக்ரிலிக் அமிலம்(Acrylic acid) என்பது CH2=CHCO2H என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட ஒரு கரிம வேதியியல் சேர்மமாகும். மிகவும் எளிமையான நிறைவுறாத கார்பக்சிலிக் அமிலமான இச்சேர்மத்தின் ஐயுபிஏசி பெயர் புரொப்-2-ஈனாயிக் அமிலம் என்பதாகும். இச்சேர்மத்தில் வைனைல் தொகுதியானது கார்பாக்சிலிக் அமில நுனியில் நேரடியாகச் சேர்ந்துள்ளது. இதுவொரு நிறமற்ற நெடியற்ற நீர்மம் ஆகும். அக்ரிலிக் அமிலம் நீர், ஆல்ககால், ஈதர் மற்றும் குளோரோஃபார்ம் முதலியவற்றில் எளிதில் கரையக்கூடியது ஆகும். ஒவ்வொரு ஆண்டும் ஆயிரம் கிலோடன்களுக்கு மேல் இது உற்பத்தி செய்யப்படுகிறது[4].
தயாரிப்பு[தொகு]
எத்திலீன் மற்றும் பெட்ரோல் தயாரிக்கும் போது உடன்விளைபொருளாகத் தோன்றும் புரொப்பிலீனை வளிம நிலையில் ஆக்சிசனேற்றி முதலில் அக்ரோலின் என்ற பொருளைப் பெறவேண்டும். பின்னர் இதனை 300 0 செல்சியசு வெப்பநிலையில் மாலிப்டினம்-வனேடியம் [5]கலவை முன்னிலையில் ஆக்சிசனேற்றம் செய்து அக்ரிலிக் அமிலம் தயாரிக்கலாம்.
- CH2=CHCH3 + 1.5 O2 → CH2=CHCO2H + H2O
அக்ரிலிக் அமிலமும் அதன் எசுத்தர்களும் வணிக ரீதியாக முக்கியத்துவம் கொண்டவை என்பதால் பல்வேறு தயாரிப்பு முறைகள் பின்பற்றப்பட்டன. ஆனால், நாளடைவில் சுற்றுச்சூழல் மற்றும் பொருளாதார காரணங்களை முன்னிட்டு பெரும்பாலான முறைகள் தடைசெய்யப்பட்டுவிட்டன. முற்காலத்தில் அசிட்டிலீனை ஐதரோ கார்பாக்சிலேற்றம் செய்து அக்ரிலிக் அமிலம் தயாரித்தார்கள்.
- HCCH + CO + H2O → CH2=CHCO2H
இவ்வினையில் அசிட்டிலீன், கார்பன் ஓராக்சைடு, நீர் ஆகிய மூன்றையும் சேர்த்து நிக்கல் வினையூக்கியின் முன்னிலையில் உயர் அழுத்தத்தில் இவை வினைப்படுத்தப்பட்டன. புரொப்பீனை அமோனியாக்சிசனேற்றம் செய்யும் பொழுது உண்டாகும் அக்ரிலோநைட்ரிலை நீராற்பகுப்பு செய்தும் அக்ரிலிக் அமிலம் தயாரிக்கலாம். அமோனியம் வழிப்பொருட்களும் உடன் விளைவதால் இம்முறை நிறுத்தப்பட்டது. எத்தனோன் மற்றும் எத்திலீன் சயனோவைதரின் [4] கொண்டு தயாரிக்கும் முறைகளும் தடை செய்யப்பட்டன. டௌ இரசாயன நிறுவனம் மற்றும் அவர்களின் பங்குதாரர்களான ஓபிஎக்சு உயிர்தொழில்நுட்பவியல் நிறுவனத்தார் இணைந்து சர்க்கரையை நொதித்தலுக்கு உட்படுத்தி அக்ரிலிக் அமிலம் தயாரிப்பதற்கான முன்னோடியான ஐதராக்சிபுரொப்பியானிக் அமிலம் [6]தயாரிக்கும் முயற்சியில் ஈடுபட்டுள்ளனர். இதன் மூலம் பசுமைக்குடில் வாயு விளைவுகளைக் குறைக்கலாம் என்று நம்பப்படுகிறது[7]
வினைகள் மற்றும் பயன்கள்[தொகு]
அக்ரிலிக் அமிலம், கார்பாக்சிலிக் அமிலத்துடன் வினைபுரிகிறது. ஆல்ககாலுடன் வினைபுரியும் பொழுது தொடர்புடைய எசுத்தர்களை உருவாக்குகிறது. எசுத்தர்கள் மற்றும் அக்ரிலிக் அமிலத்தின் உப்புகள் பொதுவாக அக்ரிலேட்டுகள் (புரொப்பியனேட்டுகள்) எனப்படுகின்றன. மெத்தில், பியூட்டைல், ஈத்தைல் மற்றும் 2-எத்திலெக்சில்-அக்ரிலேட்டு என்பவை மிகப்பொதுவான ஆல்கைல் எசுத்தர்களாகும். அக்ரிலிக் அமிலம் மற்றும் அதனுடைய எசுத்தர்கள் தமக்குள் இணைந்து (பல்லக்ரிலிக் அமிலமாக மாறும் வினை) அல்லது அவற்றின் ஒருபடி சேர்மங்களுடன் (அக்ரிலமைடுகள், அக்ரிலோநைட்ரைல், வைனைல் சிடைரின் மற்றும் பியூட்டாடையீன்) அவற்றின் இரட்டைப் பிணைப்புகளில் வினைபுரிந்து ஓரின ஒருபடிகள் அல்லது இணை பலபடிகளை உருவாக்குகின்றன. இவை பல்வேறு நெகிழிகள் தயாரிப்பில் பயன்படுகின்றன.
பாதுகாப்பு[தொகு]
அக்ரிலிக் அமிலம் தோலை எரிக்கும் தன்மை கொண்டதும் எரிச்சலுடையதும் சுவாசித்தால் நச்சுத்தன்மை உடையதும் ஆகும்.
மேற்கோள்கள்[தொகு]
- ↑ Merck Index, 11th Edition, 124.
- ↑ 2.0 2.1 2.2 2.3 2.4 2.5 "NIOSH Pocket Guide to Chemical Hazards #0013". National Institute for Occupational Safety and Health (NIOSH).
- ↑ Dippy, J.F.J.; Hughes, S.R.C.; Rozanski, A. (1959). "none". J. Chem Soc.: 2492.
- ↑ 4.0 4.1 Takashi Ohara, Takahisa Sato, Noboru Shimizu, Günter Prescher Helmut Schwind, Otto Weiberg, Klaus Marten, Helmut Greim "Acrylic Acid and Derivatives" in Ullmann's Encyclopedia of Industrial Chemistry 2003, Wiley-VCH, Weinheim. எஆசு:10.1002/14356007.a01_161.pub2 10.1002/14356007.a01_161.pub2
- ↑ அறிவியல் களஞ்சியம், தொகுதி 1, தமிழ்ப் பல்கலைக்கழகம், தஞ்சாவூர், பக்கம் 19 , அக்ரிலிக் அமிலம்
- ↑ Sweet Deal: Dow and Partner Cook up Sugar-to-Acrylic Plan. Durabilityanddesign.chi om. Retrieved on 2012-05-24.
- ↑ Better Bugs to Make Plastics, Technology Review, September 20, 2010, retrieved January 9, 2012. Technologyreview.com (2010-09-20). Retrieved on 2012-05-24.
