பேரியம் அசிட்டேட்டு
| |
| பெயர்கள் | |
|---|---|
| ஐயூபிஏசி பெயர்
பேரியம் அசிட்டேட்டு
| |
| வேறு பெயர்கள்
பேரியம் டையசிட்டேட்டு
| |
| இனங்காட்டிகள் | |
| 543-80-6 | |
| Abbreviations | Ba(OAc)2 |
| ChemSpider | 10515 |
| EC number | 208-849-0 |
| யேமல் -3D படிமங்கள் | Image |
| பப்கெம் | 10980 |
| வே.ந.வி.ப எண் | AF4550000 |
SMILES
| |
| UNII | FBA31YJ60R |
| பண்புகள் | |
| C4H6BaO4 | |
| வாய்ப்பாட்டு எடை | 255.42 g·mol−1 |
| தோற்றம் | வெண்மையான திண்மம் |
| மணம் | மணமற்றது |
| அடர்த்தி | 2.468 g/cm3 (நீரிலி) 2.19 g/cm3 (ஒற்றை நீரேறி) |
| உருகுநிலை | 725 °C (1,337 °F; 998 K) |
| 55.8 g/100 mL (0 °C) 72 கி/100மி.லி (20 °செல்சியசு) | |
| கரைதிறன் | எத்தனால் கரைப்பானில் சிறிதளவு கரையும் |
| கட்டமைப்பு | |
| படிக அமைப்பு | நாற்கோணகம் |
| தீங்குகள் | |
| முதன்மையான தீநிகழ்தகவுகள் | உட்கொள்வதால் தீங்குண்டு |
| Lethal dose or concentration (LD, LC): | |
LD50 (Median dose)
|
921 mg/kg (oral, rat) |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
| | |
| Infobox references | |
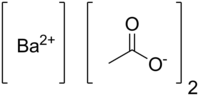
பேரியம் அசிட்டேட்டு (Barium acetate) Ba(C2H3O2)2 என்ற மூலக்கூறு வாய்பாடுடன் கூடிய பேரியம் மற்றும் அசிட்டிக் அமிலத்தின் உப்பு ஆகும்.
தயாரிப்பு[தொகு]
பேரியம் கார்பனேட்டுடன் அசிட்டிக் அமிலத்தை வினைபுரியச் செய்வதன் மூலமாக பொதுவாக பேரியம் அசிட்டேட்டு தயாரிக்கப்படுகிறது[2].
கரைசல் நிலையில் மேற்கொள்ளப்படும் இவ்வினையில் பேரியம் அசிட்டேட்டு படிகமாக வெளிவருகிறது. பேரியம் கார்பனேட்டுக்கு மாற்றாக இவ்வினையில் பேரியம் சல்பைடையும் பயன்படுத்த முடியும்.
இங்கும் கரைப்பான் ஆவியாக்கப்பட்டு பேரியம் அசிட்டேட்டு படிகமாக்கப்படுகிறது.
பண்புகள்[தொகு]
வெண்மை நிறத் துகள்களாக காணப்படும் பேரியம் அசிட்டேட்டு 0 பாகை செல்சியசு வெப்பநிலையில் அதிக அளவு கரைதிறன் பெற்றுள்ளது. அதாவது 100 கிராம் தண்ணீரில் 55.8 கிராம் அளவு பேரியம் அசிட்டேட்டைக் கரைக்க முடியும். பேரியம் அசிட்டேட்டைச் சூடுபடுத்தினால் அது பேரியம் கார்பனேட்டாக சிதைவடைகிறது.
வினைகள்[தொகு]
பேரியம் அசிட்டேட்டைக் காற்றில் சூடுபடுத்தினால் அது பேரியம் கார்பனேட்டாக சிதைவடைகிறது. மேலும் இது கந்தக அமிலம், ஐதரோ குளோரிக் அமிலம் மற்றும் நைட்ரிக் அமிலம் போன்ற அமிலங்களுடன் வினைபுரிந்து முறையே சல்பேட்டு, குளோரைடு மற்றும் நைட்ரேட்டுகளைக் கொடுக்கிறது.
பயன்கள்[தொகு]
பேரியம் அசிடேட்டு நெசவுத் தொழிலில் நெசவுத் துணிகளில் அச்சிடும் போது நிறமூட்டியாகவும், வண்ணப்பூச்சுகள் , மெருகூட்டிகளில் மற்றும் உயவு எண்ணெய்களில் உலர்த்தியாகவும் பயன்படுத்தப்படுகிறது. வேதியியலில், மற்ற அசிட்டேட்டுகள் தயாரிக்கவும் மற்றும் கரிமத் தொகுப்பு வினைகளில் வினையூக்கியாகவும் பயன்படுத்தப்படுகிறது. மேலும்,பேரியம் அசிடேட்டு உயிரைக் கொல்லும் ஒரு வலிமையான நஞ்சாகவும் இருக்கிறது.
மேற்கோள்கள்[தொகு]
- ↑ [1], JT Baker
- ↑ Barium acetate பரணிடப்பட்டது 2009-06-28 at the வந்தவழி இயந்திரம், hillakomem.com, retrieved 30 June 2009
உசாத்துணை நூல்கள்[தொகு]
- I. Gautier-Luneau; A. Mosset (1988). "Crystal structure of anhydrous barium acetate". Journal of Solid State Chemistry 73 (2): 473–479. doi:10.1016/0022-4596(88)90133-8. Bibcode: 1988JSSCh..73..473G.
| அசிட்டேட்டுகள் | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| AcOH | He | ||||||||||||||||||
| LiOAc | Be(OAc)2 BeAcOH |
B(OAc)3 | AcOAc ROAc |
NH4OAc | AcOOH | FAc | Ne | ||||||||||||
| NaOAc | Mg(OAc)2 | Al(OAc)3 ALSOL Al(OAc)2OH Al2SO4(OAc)4 |
Si | P | S | ClAc | Ar | ||||||||||||
| KOAc | Ca(OAc)2 | Sc(OAc)3 | Ti(OAc)4 | VO(OAc)3 | Cr(OAc)2 Cr(OAc)3 |
Mn(OAc)2 Mn(OAc)3 |
Fe(OAc)2 Fe(OAc)3 |
Co(OAc)2, Co(OAc)3 |
Ni(OAc)2 | Cu(OAc)2 | Zn(OAc)2 | Ga(OAc)3 | Ge | As(OAc)3 | Se | BrAc | Kr | ||
| RbOAc | Sr(OAc)2 | Y(OAc)3 | Zr(OAc)4 | Nb | Mo(OAc)2 | Tc | Ru(OAc)2 Ru(OAc)3 Ru(OAc)4 |
Rh2(OAc)4 | Pd(OAc)2 | AgOAc | Cd(OAc)2 | In | Sn(OAc)2 Sn(OAc)4 |
Sb(OAc)3 | Te | IAc | Xe | ||
| CsOAc | Ba(OAc)2 | Hf | Ta | W | Re | Os | Ir | Pt(OAc)2 | Au | Hg2(OAc)2, Hg(OAc)2 |
TlOAc Tl(OAc)3 |
Pb(OAc)2 Pb(OAc)4 |
Bi(OAc)3 | Po | At | Rn | |||
| Fr | Ra | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |||
| ↓ | |||||||||||||||||||
| La(OAc)3 | Ce(OAc)x | Pr | Nd | Pm | Sm(OAc)3 | Eu(OAc)3 | Gd(OAc)3 | Tb | Dy(OAc)3 | Ho(OAc)3 | Er | Tm | Yb(OAc)3 | Lu(OAc)3 | |||||
| Ac | Th | Pa | UO2(OAc)2 | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | |||||
